锂离子电池正极材料LiNi1/3Co1/3Mn1/3O2的制备及其电化学性能
李奇峰, 朱华丽, 刘平礼, 张 磊, 谢 添, 陈召勇
(长沙理工大学 物理与电子科学学院,湖南 长沙 410004)
Ohzuku等[1]报道层状结构的LiNi1/3Co1/3Mn1/3O2(1)是一种可以替代LiCoO2的正极材料。 1综合了LiCoO2, LiNiO2和 LiMnO2的优点,具有较低的成本、较低的毒性、良好的热稳定性和较高的比容量(>160 mAh·g-1)[1~3]。
目前,对1的研究主要集中在高截止电压下循环性能的改性研究,改性手段主要集中在阳离子掺杂[4]、阴离子掺杂[5]和表面包覆[6]。但是以上改性手段的工艺条件苛刻且制备产物中元素的存在状态有待更深入的研究。文献[7]通过优化合成工艺条件以实现1的改性是一种有效的改性手段。采用高温固相法热处理工艺制备1,具有操作简单、易于产业化的特点。1的电化学性能不仅与煅烧温度、煅烧时间和锂的用量有关,还与前躯体的种类以及后处理工艺、锂源的种类有密切的关系。
本文通过化学共沉淀法制备前躯体Ni1/3Co1/3Mn1/3(OH)2(2),以Li2CO3为锂源,2在空气气氛中经过高温热处理工艺制备了高结晶度的锂离子电池正极材料1。正交试验确定最佳工艺条件为:20.3 mol,n(Li) ∶n(2)=1.2 ∶1.0,于950 ℃反应13 h。用循环伏安曲线研究了1的电化学性能,结果表明,在2.7 V~4.6 V,电流密度16 mA·g-1时,1的首次放电比容量为203.4 mAh·g-1;经16 mA·g-1循环2次,32 mA·g-1循环9次,80 mA·g-1循环20次后放电比容量为164.1 mAh·g-1。
1 实验部分
1.1 仪器与试剂
Netzsch STA409PC型综合热分析仪;Rigaku D /MAX 2000/PC型X-射线衍射仪(XRD);Philips Quanta 200型扫描电镜(SEM);Land电池测试仪(2.7 V~4.6 V, 0.1 C倍率)。
2,河南科隆新能源有限公司制备(Ni 21.63 wt%, Co 21.44 wt%, Mn 19.66 wt%); Li2CO3(≥99.9%)。
1.2 1的制备
1的制备流程见图1。
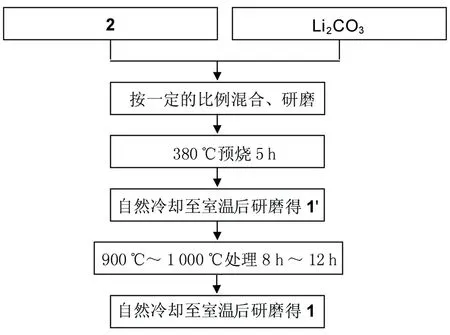
图1 1的制备流程图Figure 1 Synthesis flow chart of 1
1.3 1的电化学性能测试
正极极片中以1(0.85 g)为活性物质,乙炔黑为导电剂,聚偏氟乙烯(PVDF)为粘结剂[m(1)∶m(乙炔黑) ∶m(PVDF)=85 ∶10 ∶5],金属铝箔作为集流体,金属锂片作为对电极,美国Celgard 2400为隔膜,1 mol·L- 1LiPF6/碳酸乙烯酯/碳酸二甲酯(体积比1 ∶1 ∶1) 为电解液,在真空手套箱内装配成模拟电池。通过电池测试仪进行充放电测试。
2 结果与讨论
2.1 热重分析
为了探索2与Li2CO3制备1的反应机理以及确定合理的烧成条件,20.3 mol,按q=n(Li2CO3)∶n(2)=0.6进行配料,经研磨混匀后进行热重分析,结果见图2。由图2可见,整个反应过程中的失重主要分为2个阶段:
(1) 在100 ℃~375 ℃,质量损失为7.66%,可能由2分解成(Ni1/3Co1/3Mn1/3)3O4尖晶石相引起[8],可能发生的反应见Scheme 1。与DTA曲线上332 ℃处的吸热峰相对应。
(2) 在375 ℃~800 ℃, 15.84%的失重归结为1的形成,可能发生的反应见Scheme 2。文献[9]说明DTA曲线上700 ℃处的吸热峰由Li2O-Li2CO3的熔化引起。
(3) 在800 ℃以上则几乎无重量损失,说明在此温度下1已经完全生成。
综上所述, 2在200 ℃开始分解。由图3(1′的XRD谱图)可知,在380 ℃时,已有部分1的主晶相开始形成。在800 ℃以上则主要是材料层状结构不断趋于完善,结晶度不断提高。采用两段热处理工艺来合成1。首先在380 ℃保温5 h,形形成1的粗晶,同时有利于保持前躯体的形貌,然后在850 ℃~950 ℃进行晶化处理,使材料的结晶度提高,层状结构发育完善。

Temperature/℃图2 2和Li2CO3的混合物的热重曲线Figure 2 TG-DTA curves for the mixture of2 and Li2CO3

Scheme1


Scheme2

2θ/(°)图3 1′的XRD谱图Figure 3 XRD spectrum of 1′

表 1 正交试验设计与结果*Table 1 The design and result of orthogonal experiment
*20.3 mol,温度(A/℃),配锂量[B:n(Li)∶n(Li+Co+Mn],保温时间(C/h),首次放电容量(D/mAh·g-1)
2.2 正交试验优选制备1的条件
2(0.3 mol),选择煅烧温度、煅烧时间、碳酸锂用量(q)作为考查因素,每个因素3个水平,以首次放电容量为考查指标。按正交表L9(34)设计试验,确定最佳合成条件。正交试验设计与结果见表1。由表1可见,各因素影响反应的次序为:C>A>B,即煅烧时间对1的首次放电容量影响最大,煅烧温度次之,q的影响最小。以首次放电容量为指标的1的最佳制备条件为C1A2B2。
2(0.3 mol),q=1.2,于950 ℃煅烧13 h制得1,用于测定结构与电化学性能。
2.3 1的晶体结构与形貌
1的XRD谱图见图4。由图4可见,没有明显杂相存在,衍射峰尖锐且分裂明显,说明材料结晶度较高、物相单一、层状结构发育良好,经检索确定该材料的结构为α-NaFeO2结构。通常采用I003/I104和c/a作为评价1晶体结构的指标。当c/a值>4.899时,(006)/(102), (108)/(110)两组衍射峰才会分裂[10],这两组峰的分裂程度越大,层状结构越完整。I003/I104定义为Rm,反应材料中阳离子混排的程度。对于1, Li+(r=0.76 Å)位于3a位,过渡金属离子[Ni2+(r=0.69 Å), Co3+(r=0.54 Å),Mn4+(r=0.53 Å)]位于3b位,由于Ni2+与Li+的半径差值更小,部分Ni2+可能占据Li+的位置,这种现象称为阳离子混排。当Rm值<1.2时,说明材料中的阳离子混排现象很严重[11]。此外,(I006+I102)/I101(Ro)也可以表征材料的层状结构,Ro越小层状结构越完整[12,13]。当c/a在4.97~4.98[2,12,14~16,18~23], Rm在1.3~1.7[2,12,14~17,19~23], Ro在0.4左右[2,14~16]时,材料拥有较高的放电容量。在优化条件下制备的1的c/a, Rm和Ro分别为1.394 2,0.461 5和4.977 1,由此推测1具有良好的电化学性能。

2θ/(°)图4 1 的XRD谱图Figure 4 XRD spectrum of 1
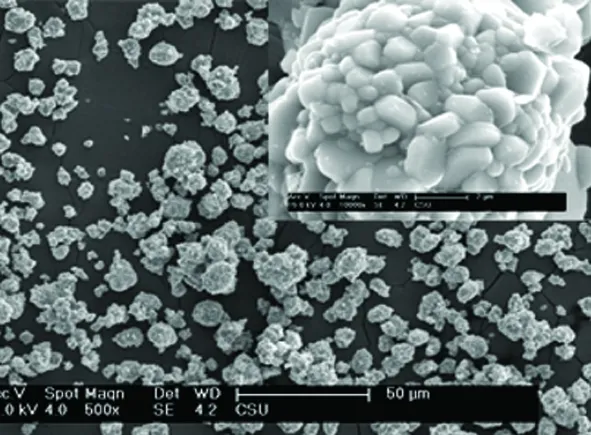
1

2图5 1和2 的SEM照片Figure 5 SEM photos of 1 and 2
图5为1和2的SEM照片。由图5可知,1基本保持了2的球形形貌,在热处理过程中,在2与碳酸锂的界面上发生固相反应,生成1新的物相,主要是通过Li+扩散到前躯体中发生反应,同时部分过渡金属离子(Ni, Co, Mn)扩散到碳酸锂中,直至反应完成。在后续热处理过程中一次粒子长大,颗粒表面的粒子由于内部粒子生长过程中的产生的应力使表面的粒子脱离表面,团聚成新的二次粒子。从而,使产物的粒度分布更加均匀,但是,由于球形颗粒的上脱落了一些表面粒子,使得产物的球形度变差。因此,在制备1的过程中确定合理的煅烧条件很重要。
2.4 1的电化学性能
1的首次充放电曲线见图6。由图6可见,工作电压由开路电压迅速升到3.75 V左右,然后慢慢的升到截止电压4.6 V。这种现象与文献[1]报道的相类似。充放电曲线平滑且没有平台,这说明了在充放电过程中没有形成与尖晶石有关的物相[22]。1的首次放电容量为203.4 mAh·g-1,首次不可逆容量为52.1 mAh·g-1。这可能是由于在电极表面形成SEI膜和在首次循环过程中电解液没有充分浸润电极材料[24]以及材料中的锂镍混排导致了材料的首次不可逆容量的损失。
图7为1在不同电流密度下的循环性能。经0.1 C循环2次, 0.2 C循环9次, 0.5 C循环20次的放电容量为164.1 mAh·g-1。引起容量损失的原因可能是:(1)电解液的分解,因为截止电压已超过了电解液的分解电压[10];(2)材料的导电率较差,造成的极化导致容量的衰减。
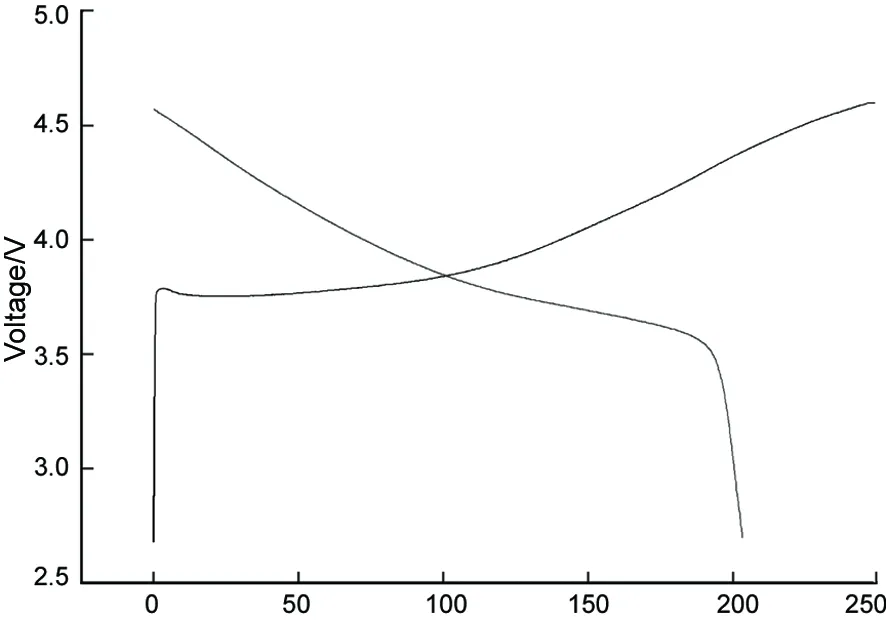
Discharge capacity/mAh·g-1图6 1首次充放电曲线Figure 6 The initial charge-discharge curves of 1

Discharge capacity/mAh·g-1图7 1在2.7 V~4.6 V的循环性能图Figure 7 Cycling performance of 1 under 2.7 V~4.6 V
3 结论
通过正交试验优化了以前躯体2和碳酸锂为原料的热处理工艺条件,即反应温度为950 ℃,反应时间为13 h,配锂量为n(Li) ∶n(2)=1.2。在该条件下制备的1基本上保持了前躯体球形形貌的特点,粒度分布均匀,且具有完整的层状结构、较小的阳离子混排度及合适的晶胞参数,使其拥有良好的电化学性能,首次放电容量为203.4 mAh·g-1,经0.1 C循环2次,0.2 C循环9次,0.5 C循环20次的放电容量为164.1 mAh·g-1。
致谢:感谢湖南省重点学科建设项目对本论文工作的资助!
[1] Tsutomu Ohzuku, Yoshinari Makimura. Layered lithium insertion material of LiCo1/3Ni1/3Mn1/3O2for lithium-ion batteries[J].Chemistry Letters,2001,30(7):642-643.
[2] A M A Hashem, A E Abdel-Ghany, A E Eid,etal. Study of the surface modification of LiCo1/3Ni1/3Mn1/3O2cathode material for lithium ion battery[J].Journal of Power Sources,2011,196(20):8632-8637.
[3] Chitturi Venkateswar Rao, Arava Leela Mohana Reddy, Yasuyuki Ishikawa. LiCo1/3Ni1/3Mn1/3O2-graphene composite as a promising cathode for lithium-ion batteries[J].ACS Appl Mater Interfaces,2011,3(8):2966-2972.
[4] Ling Liu, Kening Sun, Naiqing Zhang,etal. Improvement of high-voltage cycling behavior of Li(Ni1/3Co1/3Mn1/3)O2cathodes by Mg,Cr,and Al substitution[J].J Solid State Electrochem,2009,13(9):1381-1386.
[5] G H Kim, J H Kim, S T Myung,etal. Improvement of high-voltage cycling behavior of surface-modified LiNi1/3Co1/3Mn1/3O2cathodes by fluorine substitution for Li-ion batteries[J].Journal of the Electrochemical Society,2005,152(9):A1707- A1713.
[6] Tae Eun Hong, E D Jeong, S R Baek,etal. Nano SIMS characterization of boron- and aluminum-coated LiNi1/3Co1/3Mn1/3O2cathode materials for lithium secondary ion batteries[J].Journal of Applied Electrochemistry,2012,42(1):41-46.
[7] Li Zhang, Peixin Zhang, Zhenzhen Fan,etal. Synthesis of LiNi1/3Co1/3Mn1/3O2composite powders by solid state reaction[J].Advanced Materials Research,2011,158:262-272.
[8] S Jouanneau, J R Dahn Preparation. Structure,and thermal stability of new NixCo1~2xMnx(OH)2(0≤x≤1/2) phases[J].Chem Mater,2003,15(2):495-499.
[9] Anders Lundblad, Bill Bergman. Synthesis of LiCoO2starting from carbonate precursors Ⅰ.The reaction mechanisms[J].Solid State Ionics,1997,96(3-4):173-181.
[10] K M Shaju, G V Subba Rao, B V R Chowdari. Performance of layered Li(Ni1/3Co1/3Mn1/3)O2as cathode for Li-ion batteries[J].Electrochimica Acta,2002,48(2):145-151.

[12] Xiaoyu Zhang, W J Jiang, A Mauger,etal. Minimization of the cation mixing in Li1+x(NMC)1-xO2as cathode material[J].Journal of Power Sources,2010,195(5):1292-1301.
[13] J N Reimers, E Rossen, C D Jones,etal. Structure and electrochemistry of LixFeyNi1-yO2[J].Solid State lonics,1993,61(4):335-344.
[14] Xiaoyu Zhang, A Mauger, Qi Lu,etal. Synthesis and characterization of LiNi1/3Mn1/3Co1/3O2by wet-chemical method[J].Electrochimica Acta,2010,55(22):6440-6449.
[15] Yanhuai Ding, Ping Zhang, Deshu Gao. Synthesis and electrochemical properties of layered Li[Ni1/3Co1/3Mn1/3]0.96Ti0.04O1.96F0.04as cathode material for lithium-ion batteries[J].Journal of Alloys and Compounds,2008,456(1-2):344-347.
[16] Shunyi Yang, Xianyou Wang, Quanqi Chen,etal. Effects of complexants on [Ni1/3Co1/3Mn1/3]CO3morphology and electrochemical performance of LiNi1/3Co1/3Mn1/3O2[J].Journal of Solid State Electrochemistry, 2012,16(2):481-490.
[17] R Santhanam, B Rambabu. High rate cycling performance of Li1.05Ni1/3Co1/3Mn1/3O2materials prepared by sol-gel and co-precipitation methods for lithium-ion batteries[J].Journal of Power Sources,2010,195(13):4313-4317.
[18] Nupur Nikkan Sinha, N Munichandraiah. High rate capability of porous LiNi1/3Co1/3Mn1/3O2synthesized by polymer template route[J].Journal of The Electrochemical Society,2010,157(6):647-653.
[19] Zhen-Dong Huang, Xian-Ming Liu, Sei-Woon Oh,etal. Microscopically porous, interconnected single crystal LiNi1/3Co1/3Mn1/3O2cathode material for Lithium ion batteries[J].J Mater Chem,2011,21(29):10777-10784.
[20] S H Park, C S Yoon, S G Kang,etal. Synthesis and structural characterization of layered Li[Ni1/3Co1/3Mn1/3]O2cathode materials by ultrasonic spray pyrolysis method[J].Electrochimica Acta,2004,49(4):557-563.
[21] Shunyi Yang, Xianyou Wang, Xiukang Yang,etal. Influence of Li source on tap density and high rate cycling performance of spherical Li[Ni1/3Co1/3Mn1/3]O2for advanced lithium-ion batteries[J].Journal of Solid State Electrochemistry,2012,16(3):1229-1237.
[22] Yu-Shi He, Zi-Feng Ma, Xiao-Zhen Liao,etal. Synthesis and characterization of submicron-sized Li[Ni1/3Co1/3Mn1/3]O2by a simple self-propagating solid-state metathesis method[J].Journal of Power Sources,2007,163(2):1053-1058.
[23] Zhaorong Chang, Zhongjun Chen, FengWu,etal. The synthesis of Li(Ni1/3Co1/3Mn1/3)O2using eutectic mixed lithium salt LiNO3-LiOH[J].Electrochimica Acta,2009,54(26):6529-6535.
[24] Zhaoxiang Wang, Yucheng Sun, Liquan Chen,etal. Electrochemical characterization of positive electrode material LiNi1/3Co1/3Mn1/3O2and compatibility with electrolyte for Lithium-ion batteries[J].Journal of The Electrochemical Society,2004,151(6):A914-A921.

