细胞因子对人食道鳞癌细胞的体外杀伤作用
贺 伟 刘玉侠(长春医学高等专科学校,吉林 长春 30003)
免疫治疗已成为恶性肿瘤继手术、化疗、放疗后第四大治疗方式。细胞因子诱导的杀伤(CIK)细胞因体外增殖速度快、抗肿瘤活性强、抗瘤谱广、可以调节并增强机体的免疫功能等优势逐渐成为研究的热点〔1〕。本实验通过体外诱导培养CIK细胞对人食道鳞癌细胞(ESCC)Ecap-109的体外杀伤活性。
1 材料与方法
1.1 试剂及主要仪器 IMDM培养基,GIBCO公司;IFN-γ,上海凯茂生物医药有限公司;IL-1α,Peprotech公司;CD3Ab,RD公司;IL-2,北京四环生物制药有限公司;FCS,天津TBD公司;MTT购自 Sigma;抗人 CD3-FITC,抗人 CD16、CD56-PE,BD 公司。ESCC Ecap-109购于上海生物细胞研究所。超净工作台,上海金帆空气净化工程公司;低温高速离心机,CO2恒温细胞培养箱,美国科峻公司;全自动酶标仪,芬兰雷勃公司。
1.2 外周血单核细胞的分离、培养 用淋巴细胞分离液分离人外周血单核细胞,计数细胞数为1×106/ml,加入细胞培养瓶,放入37℃,5%CO2培养箱培养。
1.3 CIK细胞的诱导、培养 将分离培养的外周血单核细胞加入 IFN-γ 1 000 U/ml,CD3Ab 100 ng/ml,IL-1α 1 000 U/ml,IL-2 1 000 U/ml,3 d后换液,同时补加IL-2。
1.4 CIK细胞表型的测定 将诱导培养的CIK细胞用FITC标记的CD3Ab、PE标记的CD16、CD56Ab标记CIK细胞,用流式细胞仪测定CD3+CD16+CD56+细胞的表达。
1.5 Ecap-109细胞的培养 将Ecap-109用含10%IMDM的培养基培养至对数生长期,用0.25%胰酶消化后离心洗涤,调细胞数为5×104/ml,接种到96孔细胞培养板。
1.6 CIK细胞对Ecap-109杀伤活性测定 将培养的CIK细胞调细胞数为2.5×106/ml和1.25×106/ml,按以下设计加入到已接种Ecap-109的细胞培养板内,每组设6复孔。Ecap-109对照组、CIK1对照组(2.5×106/ml);CIK2对照组(1.25×106/ml);CIK1+Ecap-109组(50∶1);CIK2+Ecap-109组(25∶1);培养24 h。培养结束前4 h加入MTT,用酶标仪在292 nm处 测 OD 值。 杀 伤 活 性 =
1.7 统计学方法 应用SPSS16.0软件进行t检验。
2 结果
2.1 CIK细胞表型测定结果 CD3+CD16+CD56+表达为74.3%。见图1。
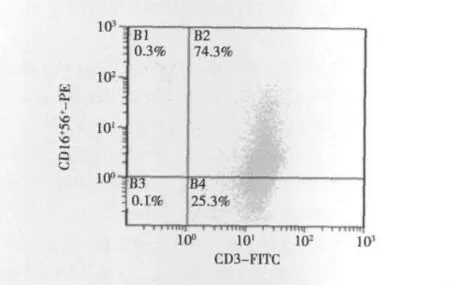
图1 CIK表型测定结果
2.2 CIK细胞对Ecap-109细胞杀伤活性 随着CIK细胞数量的增加,对肿瘤细胞的杀伤力更强(50∶1>25∶1,P<0.05)。见表1。
表1 CIK细胞对Ecap-109细胞杀伤活性(n=6,±s)

表1 CIK细胞对Ecap-109细胞杀伤活性(n=6,±s)
与CIK2+Ecap-109组比较:1)P<0.05
组别 OD值 杀伤率(%)0.694±0.024 -CIK1组 1.495±0.039 -CIK2组 1.031±0.020 -CIK1+Ecap-109组 1.532±0.0931) 94.81±3.901)CIK2+Ecap-109组Ecap-109组1.180±0.059 78.26±8.57
3 讨论
目前研究较多的抗肿瘤免疫效应细胞主要包括淋巴因子激活的杀伤(LAK)细胞〔2〕、肿瘤浸润淋巴细胞(TIL)〔3〕、抗CD3抗体激活的杀伤细胞(CD3AK)〔4〕、CIK等,但 LAK细胞、TIL等的抗肿瘤活性较低,限制了其在临床的应用〔5〕。
CIK细胞是将人外周血单核细胞在体外用多种细胞因子共同培养一段时间后获得的一群异质细胞。由于该种细胞同时表达CD3和CD56两种膜蛋白,故又被称为NK细胞样T淋巴细胞,兼具有T淋巴细胞强大的抗瘤活性和NK细胞的非MHC限制性杀瘤优点。应用CIK细胞被认为是新一代抗肿瘤过继细胞免疫治疗的首选方案。
CIK细胞同时表达多种细胞因子受体,且多项体内模型显示,CIK细胞经静脉回输体内后可以迁移至肿瘤部位。在肿瘤局部,CIK细胞可以发挥细胞毒作用,控制肿瘤的生长。与其他抗肿瘤效应细胞相比CIK细胞具有体外增殖速度快、抗肿瘤活性强、抗瘤谱广、毒性作用小等优点〔1,6〕。此外,CIK 细胞还可以调节并增强机体的免疫功能〔7〕。因此,CIK细胞过继性免疫治疗逐渐成为实体肿瘤或血液系统肿瘤治疗的新选择,逐渐成为研究的热点。本实验表明CIK细胞对肿瘤细胞的强大杀伤力。表明在临床应用时CIK细胞要达到一定的细胞数量,以保证治疗效果。
1 Hontscha,Borck Y,Zhou H,et al.Clinical trials on CIK cells:first report of the international registry on CIK cells(IRCC)〔J〕.J Cancer Res Clin Oncol,2011;137(2):305-10.
2 Rosenberg S.Lymphokine-activated killer cells:a new approach to immunotherapy of cacer〔J〕.J Natl Cancer Inst,1985;75(4):595-603.
3 Rosenberg SA,Spiess P,Lafreniere R.A new approach to the adoptive immunotherapy of cancer with tumor-infiltrating lymphocytes〔J〕.Science,1986;233(4770):1318-21.
4 Yun YS,Hargrove ME,Ting CC.In vivo antitumor activity of anti-CD3 induced activated killer cells〔J〕.Cancer Res,1989;49(17):4770-4.
5 Shablak A,Hawkins RE,Rothwell DG,et al.T cell-based immunotherapy of metastatic renal cell carcinoma:modest success and future perspective〔J〕.Clin Cancer Res,2009;15(21):6503-10.
6 Sehmidt-Wolf IG,Negrin RS,Kiem HP,et al.Use of a SCID mouse/human lymphoma model to evaluate cytokine-induced killer cells with potent antitumor cell activity〔J〕.J Exp Med,1991;174(1):139-49.
7 Sehmidt-Wolf IG,Lefterova P,Nehta BA,et al.Phenotypic characterization and identification of effector cells involved in tumor cell recognition of cytokine-induced killer cells〔J〕.Exp Hematol,1993;21(13):1673-9.

