全自动生化分析仪试剂添加方式对实验结果的影响
林 霞(江苏省盐城市射阳县人民医院检验科 224300)
对于续添同一批次的试剂,目前绝大多数实验室一般的做法是:要么把瓶内剩余试剂丢掉,更换同厂家同批号新的一瓶;要么把瓶内剩余试剂倒进新的一瓶里;要么在剩余试剂中再添加一些新试剂[1]。本实验选择化学比色类、酶法类、免疫比浊类等不同类型生化试剂,从各项目检测结果日间变异、监测终止时结果偏差等方面,就全自动生化分析仪同一批次试剂的3种添加方式对实验结果影响进行探讨。
1 材料与方法
1.1 材料 人基质定值质控血清由美国贝克曼库尔特(Beckman Coulter)公司生产(批号 M774301);罗氏(Roche)公司生产cfas校准品(批号181937)用于丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)、肌酐(Cr)、总蛋白(TP)、钙(Ca)项目校准;脂蛋白[LP(a)]、载脂蛋白 A1(ApoA1)、超敏C反应蛋白(hs-CRP)由原试剂生产厂家各项目试剂盒配套校准液校准。
1.2 仪器与试剂 仪器为东芝TOSHIBA120全自动生化分析仪。试剂采用日本关东化学株式会社生产的ALT和AST试剂;ALP由宁波普瑞生物技术公司生产;TP试剂由上海荣盛生物药业有限公司生产;Cr和Ca试剂由上海执诚生物技术有限公司生产;LP(a)、ApoA1、hs-CRP检测试剂盒由英国RANDOX Laboratories有限公司生产。
1.3 方法
1.3.1 本组选择的实验项目包含了化学比色类:碱性苦味酸法Cr、ALP、TP和Ca;酶法类ALT、AST;免疫比浊类LP(a)、ApoA1、hs-CRP等不同反应类型。
1.3.2 进行仪器的每日维护 比色杯的检查,查看清洗液、供水情况,样品针、试剂针清洗,擦搅拌棒等。
1.3.3 所有实验参数均按仪器和试剂盒说明书设置,本实验试剂严格按照试剂盒质量外观检查后添加,如发现工作液色泽改变,有异物出现或混浊,说明试剂已经变质或被污染应丢弃[2]。试剂添加量均在试剂瓶口下10mm,以防试剂盘高速运转时飞溅到其他试剂瓶中而影响测试结果。
1.3.4 将仪器使用后剩余的少量试剂连瓶丢掉,代之以未开封的同厂家同批号试剂,为第1组;取一瓶同厂家同批号的新鲜试剂,将仪器使用剩余的原试剂倒入其中,再放入仪器,为第2组;往仪器使用中原试剂瓶内添加同厂家同批号的新鲜试剂,为第3组。
1.3.5 开始检测前,先进行室内质控血清测定,同时采用正常值和异常值两个浓度,由英国RANDOX公司生产,637UN和467UE质控血清的测定结果均在±2s范围之内。
1.3.6 根据需要,第1个月按第1种方法添加仪器内使用中试剂,第2个月按第2种方法添加仪器内使用中试剂,第3个月按第3种方法添加仪器内使用中试剂。添加试剂后,分别对以上项目校准空白后进行测定,每个项目质控样本测定22次。
1.4 统计学处理 使用EXCEL软件统计,以监测时间(d)为横轴、测定值为纵轴,绘制3种不同添加试剂方法时分别测得各项目结果的趋势图;统计各项目的、s和CV;以室内质控血清定值为靶值,计算各项目在监测终止时结果的偏差;组间比较用方差分析,组间两两比较q检验(SNK法)。本实验所有数据经SPSS13.0统计软件处理,P<0.05为差异有统计学意义。
2 结 果
2.1 3种添加试剂方法检测质控样本9个生化项目所得结果的比较 3种添加试剂方法检测9个生化项目,结果均存在日间趋势性变化,监测终止时的结果与室内质控血清定值(靶值)相比较也都存在偏差。第1组各项目的日间变异和监测终止时的结果偏差较其余两组小,3组间 ApoA1、LP(a)、Hs-CRP日间变异和监测终止时的结果偏差相差极微。见表1。
2.2 组间9个生化指标检测结果的比较 3组总变异经F检验后有差异有统计学意义(P<0.05)的项目,再进行组间两两比较。见表2。ApoA1、LP(a)、hs-CRP 3种添加方法不进行组间两比较,且不同添加试剂方法检测结果间差异无统计学意义(P>0.05);Cr、ALP、TP、Ca、ALT、AST在第1组的检测结果与第2、3组比较,差异均具有统计学意义(P<0.05),而第2、3组结果比较,差异无统计学意义(P>0.05)。
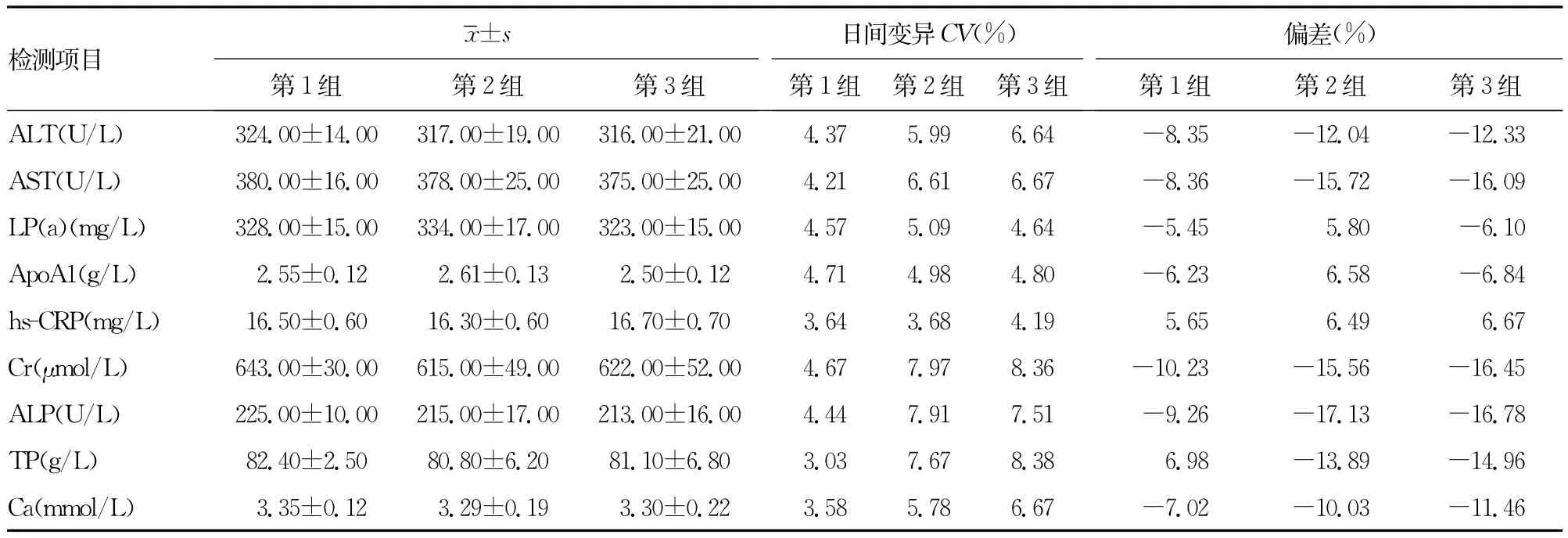
表1 4种添加试剂方法9个生化项目检测结果的比较
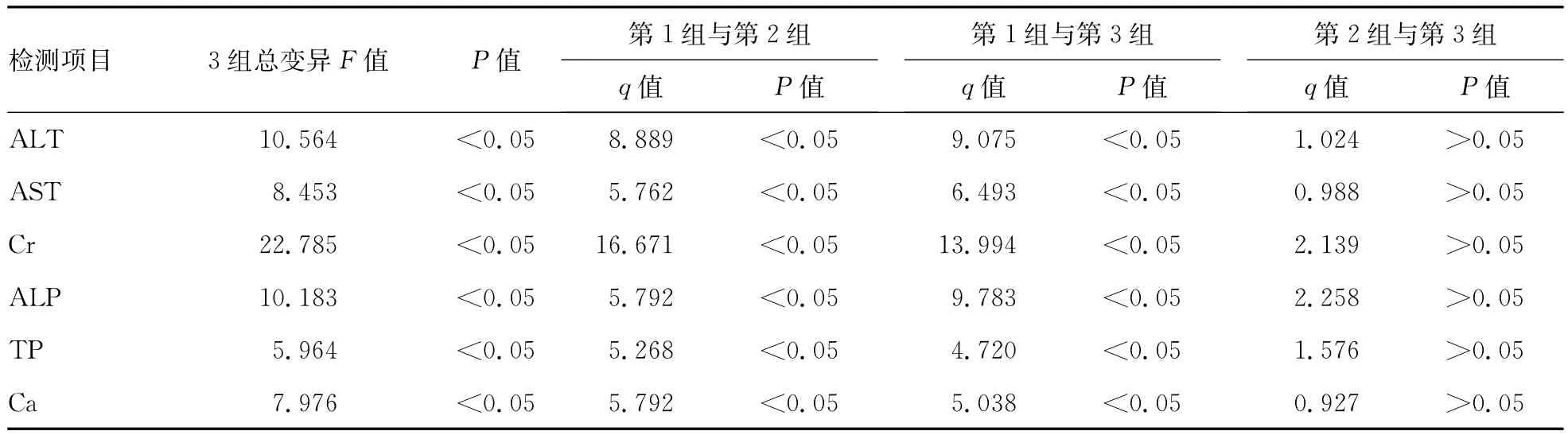
表2 9个生化指标检测结果三组间的比较
3 讨 论
3.1 本组选择的实验项目包含了化学比色类(Cr、ALP、TP、Ca)、酶法类(ALT、AST)、免疫比浊类[LP(a)、ApoA1、Hs-CRP]等不同反应类型的试剂,且所选择项目均具有开瓶稳定性较差或试剂使用率较低的特点,其目的是为了观察易污染和使用频率不同的常规项目在3种不同添加试剂方法过程中的变化情况。为了保证实验条件的一致性,添加试剂后均在校准空白后测定质控结果。
3.2 化学比色类ALP、TP、Ca和Cr用不同方式添加试剂时结果差异有统计学意义(P<0.05),其中ALP、TP的试剂pH为碱性,开瓶后试剂会吸收空气中的CO2,使试剂本身的pH值下降,检测结果发生偏离,因此应了解试剂的特性,及时对部分项目进行校准[2]。Ca和Cr在本实验的结果与曾平等[1]的结论相同,这可能与两者的测定方法有关,因为测定Ca需要在强碱性环境中进行,空气中的酸性物质(如CO2等)易破坏试剂中的碱性环境(东芝生化分析仪试剂孔是敞开的)。因此试剂很容易与空气接触,从而使试剂的pH发生改变,导致结果差异[3]。碱性苦味酸法肌酐(Cr)试剂组分中NaOH由于长时间暴露于空气中易吸收CO2,使其溶液浓度逐渐降低。NaOH浓度是Jaffe反应中影响光谱吸收的重要因素,所以试剂存放须校准和做质控后,质控测定结果在规定的允许范围内才能使用[4-6]。
3.3 ALT、AST测定是典型的酶法反应类型,试剂成分中的NADH、ONPG稳定性较差,易在空气中氧化,而NADH降解将造成检验结果低值升高而高值偏低[5]。
3.4 LP(a)、ApoA1、Hs-CRP是典型的免疫比浊法检测项目,其试剂主要有效成分为抗血清,即蛋白质类物质,其试剂价格较为昂贵,一些临床实验室这些项目的临床样本量较小,因此试剂使用率低;虽本实验显示试剂添加方法对其结果影响甚微,但日间变异和在监测终止时结果偏差仍存在,可能是由于试剂含蛋白质成分,易被微生物污染,如试剂开瓶后在试剂仓中存放时间过长也会影响检测结果。就目前有的试剂方法学来讲,还达不到人们所要求的试剂开瓶后在仪器内放很长时间不需要定标。
3.5 3种不同添加试剂方法以第1种方法最好,没有新旧试剂的混合,但是很浪费,每次至少要丢掉十几到几十人份的试剂,成本增加。后两种方法虽然节约,但试剂瓶里新旧试剂混淆,随着时间延长或许里面还有1周甚至1个月前的试剂而影响检测结果。
3.6 建议上机使用开封后不稳定的试剂而标本量又比较少时,最好选用小剂量试剂瓶上机,用大瓶上机时尽可能正确估计第2天试剂用量,以免造成新旧试剂的叠加次数太多,定期更换试剂瓶,另外加试剂后最好校标和做质控一次,并应进行校准后验证。
3.7 一般每个试剂瓶内由于试剂针不能吸完,或多或少都会留有几毫升的试剂,为节约起见,最好的做法是将每个批号的剩余试剂留起来妥善保存,待一定数量后混在一起,重新定标后检测。
3.8 有些实验室和试剂厂家一直共同关注如何有效延缓试剂开瓶后的衰变过程,提高试剂开瓶稳定性[7]。目前有通过改良试剂组分或在试剂中添加稳定剂来提高试剂稳定性的报道,已有部分实验项目取得较为显著的效果[8-10]。但此类解决方案多具有项目局限性,且改变试剂成分是否会对检测的性能造成影响,尚需进行大量评价实验来证实。国内亦有通过改良试剂瓶,减少试剂与流动空气接触的先例,但该方法是否适用于所有自动生化分析仪机型也有待于进一步探讨[7]。
3.9 本实验选择检测美国贝克曼库尔特公司生产人基质定值质控血清(批号:M774301),它是高浓度值,那么3种添加试剂方法对中、低浓度的检测结果的影响怎样?是否与本实验结论相同?还需进行大量实验来评价。
[1] 曾平,刘运双,罗军,等.全自动生化分析仪试剂添加方法对试验结果的影响[J].国际检验医学杂志,2006,27(8):759-760.
[2] 张仲全.全自动生化分析仪试剂存在的问题及解决方法[J].中国民族民间医药,2009,18(12):71-72.
[3] 罗侃,崔有宏.临床化学方法学评价[M].北京:兰州大学出版社,1996.
[4] 韩志钧.临床化学常用项目自动分析法[M].沈阳:辽宁科学技术出版社,2005:998-1000.
[5] 王箴.化工辞典[M].北京:化学工业出版社,2000:98-99.
[6] 康格非,巫向前.临床生物化学和生物化学检验[M].北京:人民卫生出版社,1999.
[7] 邓建平,朱海波.改良试剂瓶提高生化试剂开瓶稳定性的应用研究[J].现代检验医学杂志,2010,25(1):91-94.
[8] 胡望平,周长邵,王丹,等.肌酐试剂稳定性的改进[J].现代检验医学杂志,2003,18(2):33-33.
[9] 肖少林,魏曼梅,胡望平.改进肌酐试剂稳定性的方法[J].检验医学与临床,2007,4(8):759-760.
[10] 袁水斌,邓荣春,张友权,等.稳定型总蛋白(TP)试剂的研制[J].江西医学检验,2006,24(2):124-126.

