固相萃取-高效液相色谱测定地表水中丙烯酰胺
王 燕,龙加洪,许雄飞,瞿白露,莫 婷
(长沙市环境监测中心站,湖南长沙410001)
丙烯酰胺为白色透明片状晶体,易溶于水,强极性,不易去除。可通过被污染的水体由消化系统进入人体,对人体具有神经毒性、生殖毒性,并会对人大脑以及中枢神经系统造成损害[1]。丙烯酰胺已被证实可能与多种癌症有关联[2-3],世界卫生组织(WHO)对聚丙烯酰胺使用时的投加量做出了严格限制,即每升水中投加量不得超过1mg[4]。我国对其在饮用水及饮用水源地中的水质标准限定为0.5 μg/L[5-6]。目前,食品行业对于丙烯酰胺的测定方法研究深入,一是将样品溴化衍生化后用气质联用测定,二是固相萃取后高效液相色谱-质谱法[7-8]。环境监测部门采用的是国际上常用的溴化衍生方法[9-10],即将丙烯酰胺转化为2,3-二溴丙酰胺后,再进行气相色谱测定[6]。现有文献[11]将该方法的衍生化条件优选,提高了方法的稳定性。上述各种方法中,溴化衍生化耗时耗力,且溴化条件难以把握、样品基体干扰复杂;而固相萃取高效液相色谱-质谱法多用于食品行业,目前环境监测部门液相色谱质谱联用仪普及不广泛,故固相萃取高效液相色谱-质谱法在水质分析中的应用实现也相对困难。本文综合考虑,选用固相萃取-液相色谱法对地表水及饮用水中丙烯酰胺的测定进行探讨,选择适合的固相萃取小柱,优化固相萃取条件、确定方法检出限,通过准确度、精密度等试验,建立水中丙烯酰胺新的测定方法。
1 实验部分
1.1 仪器和试剂
1.1.1 仪器
液相色谱仪日本岛津LC-20AT,配有二极管阵列(PDA);液相色谱柱Shim-Pack VP-ODS 150mm×4.6mm,5μm;
固相萃取仪Auto Trace(美国Caliper);氮吹仪OA-SYS(美国);
固相萃取柱CARB(500mg);
1.1.2 试剂
丙烯酰胺标准溶液(1 000μg/mL,CH3OH);甲醇色谱纯试剂;超纯水。
1.2 液相色谱条件
流动相:V(甲醇):V(纯水)=20:80,柱流速0.3mL/min,甲醇输液泵压力3.6MPa,柱温40℃,PDA波长扫描范围190~250nm;进样量20uL。
1.3 样品采集
采集样品时,将样品缓缓注入500mL棕色玻璃瓶中,直到少量样品溢出,加盖并用锡箔纸密封。尽快分析,如不能及时分析,应将样品储存于4℃冰箱中保存。
1.4 样品处理
1.4.1 固相萃取柱的活化:用10mL甲醇和10mL超纯水依次对固相柱进行活化。
1.4.2 样品加载:将样品澄清后,以1.0mL/min的速度加载500mL于固相柱上,流出液弃去。
1.4.3 固相萃取柱的洗脱:用10mL甲醇以1.0mL/min的速度分3次洗脱(第1次3mL,第2次4mL,第3次3mL),收集流出液于氮吹瓶中,备用。
1.4.4 洗脱液的浓缩:将以上洗脱液在45℃水浴条件下用氮吹仪浓缩至1mL,定容至2mL待测。
2 结果与讨论
2.1 固相萃取柱和洗脱剂的确定
考虑到丙烯酰胺为亲水性极性有机物,选择固相萃取柱时传统的C18反相柱是不可取的,只能考虑物理吸附富集柱。本实验比较了活性碳柱(CARB)、EPS专用柱和多孔性硅藻土柱的处理效果,加标水样质量浓度为0.5μg/L和1.0μg/L时,多孔性硅藻土、EPS专用柱和CARB的加标回收率如表1,根据实验结果选择CARB作为最终前处理固相萃取柱。

表1 固相萃取柱选择实验结果
固相萃取洗脱剂有很多种,实验室常用的有甲醇、丙酮、乙酸乙酯等。丙酮在液相色谱上的出峰时间与丙烯酰胺接近,对其定性定量造成严重干扰;乙酸乙酯没有甲醇极性强,对丙烯酰胺洗脱效率不高,实验结果如图1,故选择甲醇作为洗脱剂。

图1 洗脱条件选择
2.2 加载样品速度的选择
对500mL质量浓度为1.0μg/L的加标水样进行样品加载速度比较,0.5mL/min和1.0mL/min的富集效率接近,分别为64%和62%,2.0mL/min的富集效率明显降低为41%,5.0mL/min的富集效率为10%,很不满意,结果如图2。综合考虑回收率和耗时,选择1.0mL/min的样品加载速度。
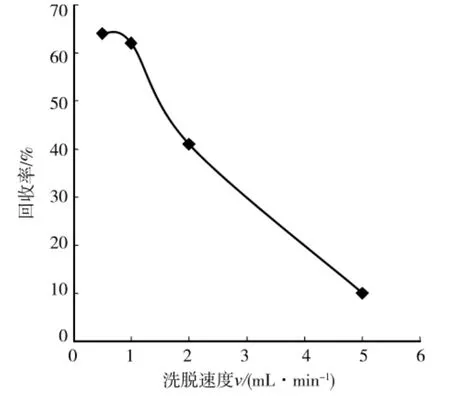
图2 洗脱速度选择
2.3 洗脱条件选择
活性碳柱粒度较其他柱子大,且孔隙小而密。因此在洗脱时速度不宜过快,否则影响回收率。多个活性碳柱的洗脱速度比较,速度在0.5~1.0mL/min时,回收率满意,速度超过1.0mL/min回收率明显降低。洗脱剂甲醇用量也直接影响回收率的高低,分别比较用量为5,8,10,20mL的甲醇洗脱,结果表明用量过低回收率无法满足要求,当用量为10mL以上回收率满意,实验结果如图1。综合考虑最终确定洗脱速度为1.0mL/min,甲醇洗脱量为10mL分3次完成(第1次3mL,第2次4mL,第3次3mL)。
由于丙烯酰胺是亲水性极强的物质,在洗脱过程中未加入吹干程序,直接将含水洗脱液在45℃水浴下缓慢通氮气吹至1mL左右定容待测。这是为了避免目标物的损失。
2.4 标准曲线和方法检测限
配制丙烯酰胺质量浓度分别为0.10,0.25,0.50,0.75,1.00μg/mL 的标准溶液经色谱分析后,以标液质量浓度为横坐标,以标液响应值为纵坐标得标准曲线线性回归方程y=71 779.1x+286.8,r=0.999 1,结果表明在0.10~1.00μg/mL的质量浓度范围内线性相关性良好。
重复测定8次低含量丙烯酰胺加标样品计算标准偏差,取3倍s值为检测限(LOD)[12]。经计算本方法LOD为0.2μg/L。
2.5 实际样品测定、样品加标回收率和精密度
由于地表水中实际样品的丙烯酰胺均未检出,故选取加标量为0.5μg的实际样品连续测定8次,色谱图如图3。对所得结果进行分析,通过表2可知,本方法的加标回收率、日内和日间重复性符合环境监测技术要求。
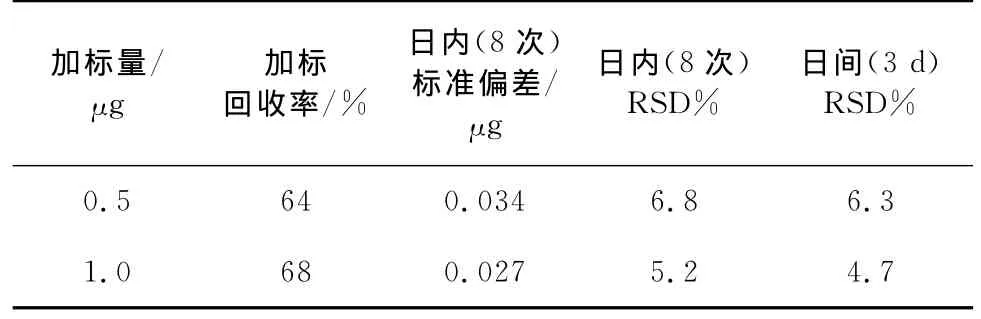
表2 加标回收率、重复性实验结果
3 结论
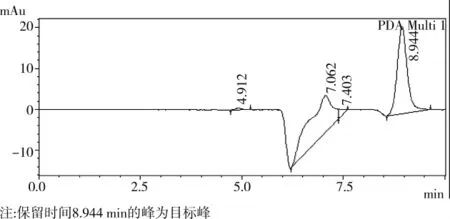
图3 标准品色谱图
本方法采用CARB固相萃取柱对水质样品进行前处理,再通过高效液相色谱仪分析测定。通过验证实验可知,本方法检出限为0.2μg/L,加标回收率64%~68%,8次重复测定相对标准偏差低于6.8%,结果完全满足环境监测分析评价要求。因此本方法可应用于地表水中丙烯酰胺的分析检测。综合其操作简便、准确可靠等优点,可为今后复杂水质样品中丙烯酰胺测定研究工作的深入开展提供技术支持。
[1]程 雷,孙宝国,宋焕禄,等.食用香精香料的安全性评价现状及发展趋势[J].食品科学,2010,31(21):409-412.
[2]丁茂柏.科学评估丙烯酰胺危害[J].中国职业医学,2007,34(1):61-64.
[3]宋 雁.食品中丙烯酰胺对健康的影响[J].卫生研究,2005,34(2):241-243.
[4]陈 玲,陈 皓.固相存取-高效液相色谱联用仪分析水中的痕量丙烯酰胺[J].色谱,2003,21(5):534.
[5]国家环境保护总局.GB 3838-2002地表水环境质量标准[S].北京:中国环境科学出版社,2002.
[6]中华人民共和国卫生部.GB/T 5750.8-2006生活饮用水标准检验方法[S].北京:中国标准出版社,2007.
[7]安徽省产业质量监督检验所,国家农业标准化与监测中心.GB/T5009.204-205食品中丙烯酞胺含量的测定方法气相色谱-质谱(GC-MS)法[S].北京:中国标准出版社,2005.
[8]ANDRZEJEWSKID,ROACHJ,GAYM,et al.Analysis of coffee for the prisince of acrylamide by LC-MS/MS[J].Journal of Agricultural and Food Chemistry,2004,52(7):1 996-2 002.
[9]Takata K,Okamoto T.The biological degradability of acrylamide monomer[J].Kankyo Kagaku,1991,1(3):559.
[10]Smith E A,Oehme F W.Liquid chromatographic determination of acrylamide monomer in natural and polluted aqueous environments[J].J Chromatogr Sci,1993,31(5):192.
[11]杨丽莉,王美飞,胡恩宇,等.水中丙烯酰胺气相色谱测定方法研究[J].中国环境监测,2012,28(1):46-48.
[12]ARMBRUSTER D,TILLMAN M,HUBBS L.Limit of detection(LOD)limit of quantitation (LOQ):comparison of the empirical and the statistical methods exemplified with GC-MS assays of abused drug[J].Clinical Chemistry,1994,40(7):1 233-1 238.

