白枪杆的化学成分研究(Ⅰ)Δ
谭兴起,郭良君,郑巍,谭昌恒(1.解放军第85医院,上海 010;.解放军第98医院,浙江 湖州 1000;.中国科学院上海药物研究所新药研究国家重点实验室,上海 010)
白枪杆(Fraxinus malacophylla Hemsl.)为木犀科梣属植物,是我国特有植物,分布于广西、云南[1]。其味苦、涩,性寒,具有清热、利尿、通便的功效,主治膀胱炎、膀胱结石、小便不利、便秘、疟疾、高烧鼻衄等症。《科学的民间药草》记载白枪杆的根皮、树皮、树叶均有显著的解热作用。临床试验结果表明,白枪杆根皮对急性和慢性间日疟是特效的治疗剂,对恶性疟疾和四日疟也有效[2]。然而,关于该植物的化学成分研究还较少,《中药大辞典》中记载白枪杆树皮含新宁碱、鞣质、树脂、糖类、香豆素等[2];He ZD等[3]曾从白枪杆中分离得到过两个裂环烯醚萜葡糖苷化合物。为了更进一步地寻找白枪杆中活性成分,笔者对白枪杆树皮80%的乙醇提取物进行了化学成分研究。
1 材料
1.1 仪器
UV-1型三用紫外分析仪(上海顾村电光仪器厂);201D型升降恒温水油浴锅(杭州惠创仪器设备有限公司);SHB-ⅢA型循环水式多用真空泵(上海预康科教仪器设备有限公司);RE-201D型减压旋转蒸发仪(杭州惠创仪器设备有限公司);BSZ-100型自动部分收集器(上海沪西分析仪器有限公司);DRX-400 MHz型核磁共振(NMR)仪(德国Bruker公司);ZAB-ZF型质谱(MS)仪(英国VG公司)。
1.2 试剂
氯仿、甲醇、乙醚、石油醚、乙酸乙酯、硫酸、冰醋酸均为分析纯,乙醇为医用95%乙醇,水为自制蒸馏水;薄层层析用硅胶粉(200~300目)和薄层层析用硅胶板均购自烟台江友硅胶开发有限公司。
1.3 药材
白枪杆树皮于2011年4月采自云南蒙自县,经解放军第98医院药械科郭良君副主任药师鉴定其来源为木犀科植物白枪杆(F.malacophylla Hemsl.)。
2 提取与分离
取白枪杆干燥树皮15kg,用80%乙醇浸泡7天,连续浸泡3次,合并浸出液,回收蒸干;浸膏用水加热溶解,滤过,分别用石油醚、氯仿、正丁醇萃取,每个批次萃取3次,分别蒸干萃取液,得到石油醚、氯仿、正丁醇部分。本试验对正丁醇部分进行分离。将正丁醇部分用大孔树脂经10%、20%、30%的乙醇溶液梯度洗脱,分别合并浓缩,得到10%、20%、30%三部分,再综合运用硅胶、凝胶等色谱手段按以下方法对这三部分的化学成分进行分离纯化,得到化合物1~10。
10%部分经氯仿-甲醇及氯仿-甲醇-水系统梯度洗脱。氯仿-甲醇(15∶1,V/V)洗脱部分经处理得到3个化合物:经甲醇重结晶得到化合物9;再经70%甲醇凝胶纯化,得到化合物4和化合物8。氯仿-甲醇(30∶1→40∶1,V/V)洗脱部分经甲醇(略带水)重结晶得到白色晶体,即化合物7。氯仿-甲醇-水(7∶1∶1,V/V/V)洗脱部分先后经甲醇、氯仿-甲醇(1∶1,V/V)凝胶纯化,得到化合物2和化合物3。
20%部分经氯仿-甲醇系统梯度洗脱。氯仿-甲醇(10∶1,V/V)洗脱部分经甲醇凝胶纯化,再用氯仿-甲醇(10∶1,V/V)重结晶,得到略黄色晶体,即化合物1;氯仿-甲醇(5∶1,V/V)洗脱部分经甲醇凝胶纯化,再用氯仿-甲醇(5∶1,V/V)重结晶,得到化合物10。
30%部分经氯仿-甲醇系统梯度洗脱。氯仿-甲醇(10∶1,V/V)洗脱部分经甲醇-水(7∶3,V/V)凝胶纯化,得到化合物6,再经硅胶用氯仿-甲醇系统梯度洗脱[氯仿-甲醇(20∶1→15∶1→10∶1,V/V)],得到化合物5。
各化合物的化学结构式见图1。
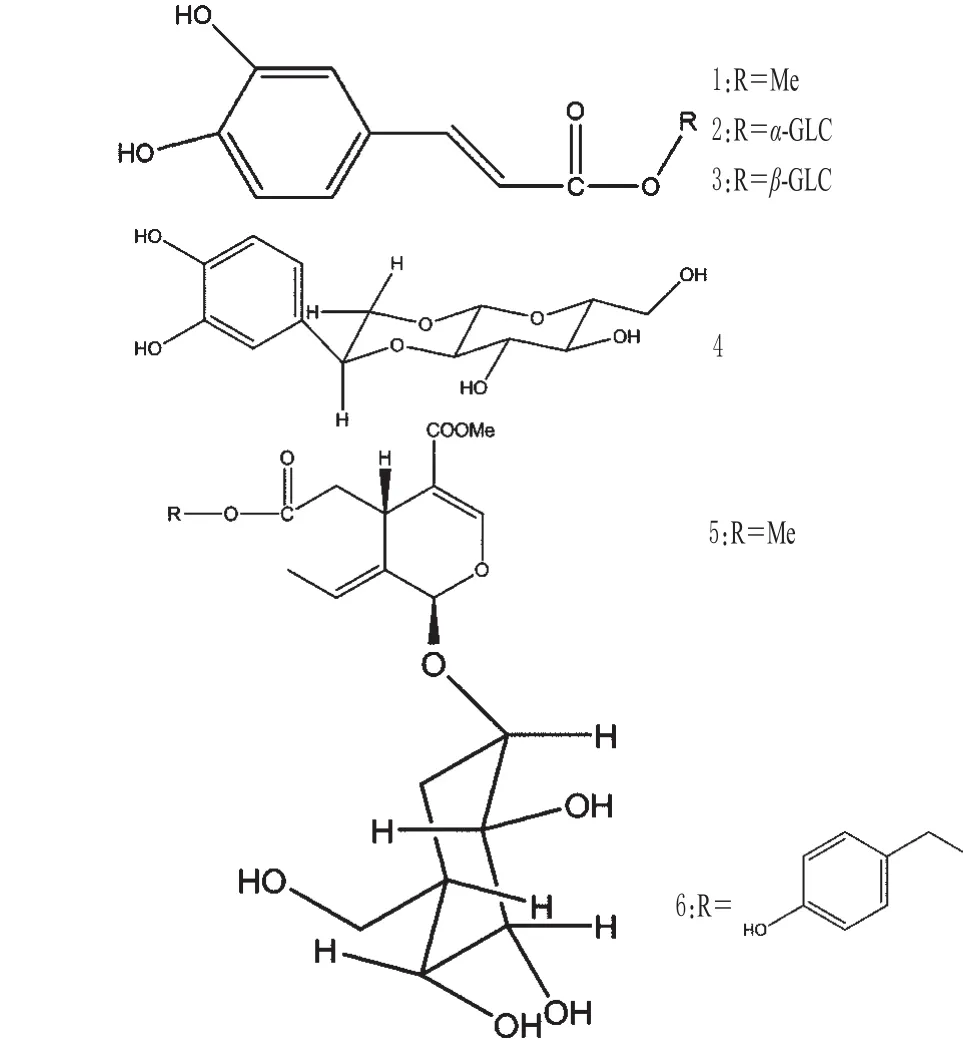
图1 化学结构式Fig 1 Chemical structure
3 结构鉴定
化合物1:淡黄色晶体,熔点为161~163℃,分子质量为194,分子式为C10H10O4。LC-MS(液质联用):193(M-H)-;163(M-MeO)+。1H-NMR(400 MHz,DMSO)δ:3.72(3H,s,—OCH3),7.17(1H,d,J=2.0 Hz,H-2),6.87(1H,d,J=7.8 Hz,H-5),7.03(1H,dd,J=7.8,2.0 Hz,H-6),6.27(1H,d,J=16.0 Hz,8-H),7.54(1H,d,J=16.0 Hz,9-H)。13C-NMR(100 MHz,DMSO)δ:127.6(C-1),115.2(C-2),146.3(C-3),148.7(C-4),115.3(C-5),122.5(C-6),145.9(C-7),116.0(C-8),167.8(C-9),51.5(—OCH3)。以上数据与文献[4]报道基本一致,故鉴定该化合物为咖啡酸甲酯。
化合物2:浅黄色粉末,分子质量为342,分子式为C15H18O9。LC-MS:365(M+Na)+,707(2M+Na)+;341(M-H)-。参考文献[5],可以判断13C-NMR数据有一个α-D-葡萄吡喃糖单元。结合文献[6]可知,Glc-1位的化学位移95.79提示被酯化。通过归属数据,推断该化合物为1-O-咖啡酰基-α-D-葡萄吡喃糖。化合物2、3的NMR数据见表1。
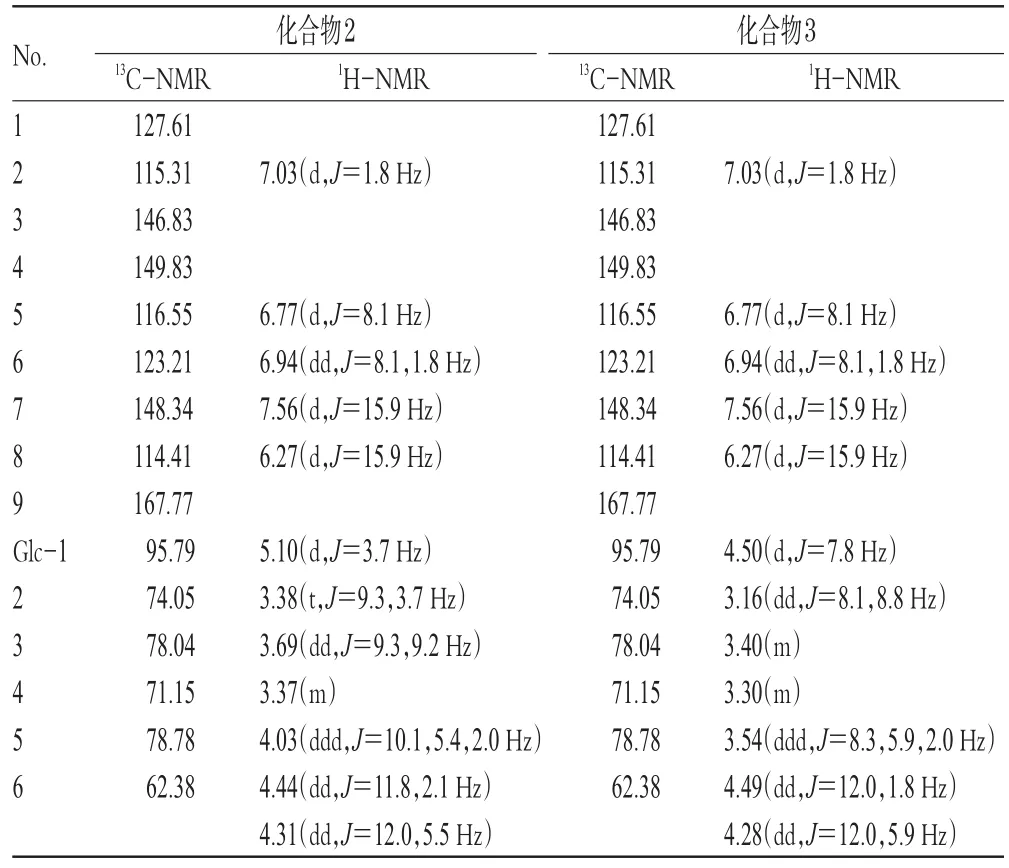
表1 化合物2、3的NMR数据Tab 1 NMR data of compound 2,3
化合物3:淡黄色粉末,分子质量为342,分子式为C15H18O9。LC-MS:365(M+Na)+,707(2M+Na)+;341(M-H)-。具体碳氢信号归属见表1。光谱数据与文献[6]报道一致,故鉴定该化合物为1-O-咖啡酰基-β-D-葡萄吡喃糖。
化合物4:白色结晶(甲醇),熔点为104~105℃,分子质量为314,分子式为C14H18O8。ESI-MS(电喷雾电离质谱):337(M+Na)+,651(2M+Na)+。化合物4的NMR数据见表2。以上数据与文献[7]对照基本一致,故鉴定该化合物为存额阿塔斯德A。
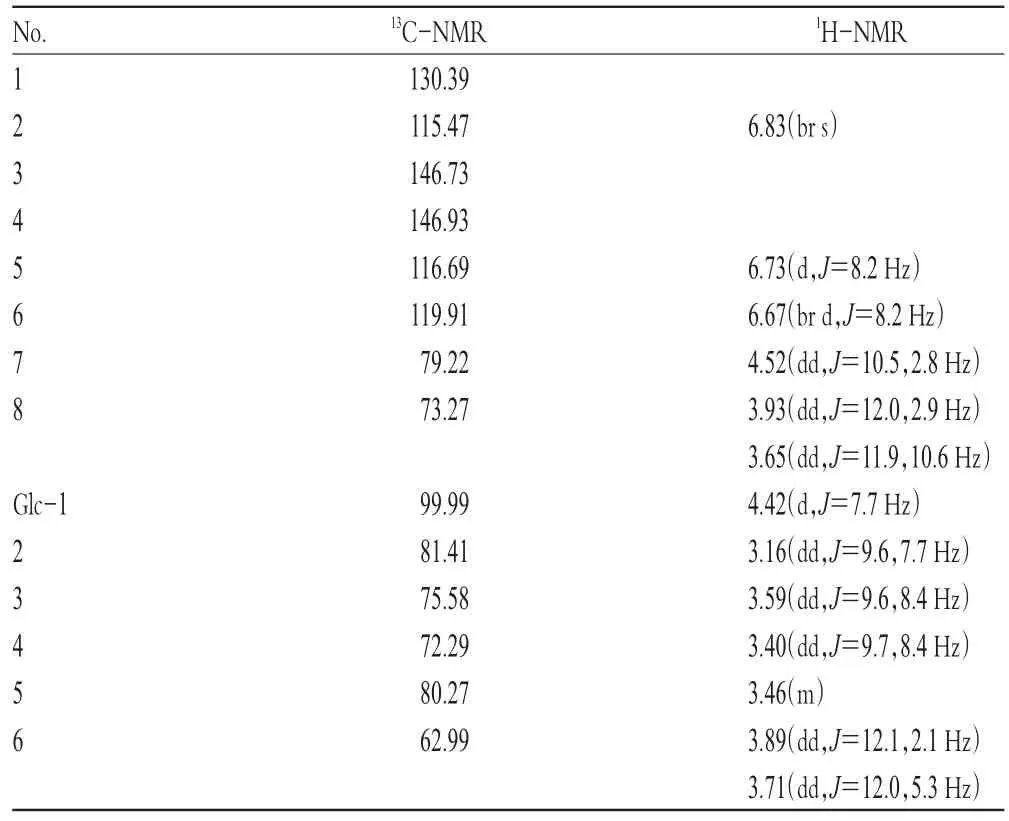
表2 化合物4的NMR数据Tab 2 NMR data of compound 4
化合物5:白色粉末,分子质量为418,分子式为C18H26O11。 ESI-MS:441(M+Na)+。1H-NMR(400 MHz,DMSO)δ:1.78(3H,d,J=7.2 Hz,H-10),2.41(1H,m,H-6b),2.68(1H,dd,J=3.6,14.8 Hz,H-6a),3.42(3H,s,H-7,—OCH3),3.83(3H,s,H-11,—OCH3),3.92(1H,d,J=5.2 Hz,H-5),4.72(1H,d,J=7.6hz,H-Glc端基),5.94(1H,s,H-1),6.15(1H,s,H-8),7.48(1H,s,H-3)。13C-NMR(100 MHz,DMSO)δ:92.9(C-1),153.1(C-3),108.2(C-4),30.1(C-5),40.1(C-6),172.1(C-7),122.1(C-8),129.4(C-9),13.1(C-10),166.2(C-11),51.2(C-11,—OCH3),51.4(C-7,—OCH3)。以上数据与文献[8]报道基本一致,故鉴定该化合物为7,11-二甲酯油苷。
化合物6:白色粉末,熔点为147~148℃,分子质量为524,分子式为 C25H32O12。LC-MS:547(M+Na)+;569(M+HCOO-)-。1H-NMR(400 MHz,CD3OD)δ:Aglycone:5.90(1H,s,H-1),7.51(1H,s,H-3),4.10(1H,m,H-5),2.42(1H,dd,J=9.3,14.1 Hz,H-6α),2.81(1H,dd,J=4.4,14.1 Hz,H-6β),6.08(1H,q,J=7.0 Hz,H-8),1.64(3H,d,J=7.1 Hz,H-10),3.71(3H,s,—OCH3);Phenylethyl:4.21(2H,t,J=7.0 Hz,H-1′),2.82(2H,t,J=7.0 Hz,H-2′),7.05(2H,d,J=8.3 Hz,H-4′,8′),6.71(2H,d,J=8.4 Hz,H-5′,7′);Glucose:4.80(1H,d,J=7.7 Hz,H-1″),3.20~3.35(4H,H-2″~5″)。13C-NMR(100 MHz,CD3OD)δ:Aglycone:95.6(C-1),155.6(C-3),109.8(C-4),32.3(C-5),41.7(C-6),173.7(C-7),125.4(C-8),130.9(C-9),14.1(C-10),169.1(C-11),52.4(—OCH3);Phenylethyl:67.4(C-1′),35.6(C-2′),130.5(C-3′),131.5(C-4′,8′),116.8(C-5′,7′),157.6(C-6′);Glucose:101.3(C-1″),75.2(C-2″),78.4(C-3″),72.0(C-4″),78.9(C-5″),63.2(C-6″)。以上数据与文献[9]报道一致,故鉴定该化合物为(8Z)-橄榄苦苷。
化合物7:白色结晶(甲醇),熔点为225~227℃,分子质量为 180,分子式为C6H12O6。1H-NMR(400 MHz,CD3OD)δ:3.18(1H,dd,J=9.1 Hz,H-2),3.40(2H,dd,J=2.7,9.9 Hz,H-4,6),3.54(2H,t,J=9.7 Hz,H-1,3),4.12(1H,t,J=2.7 Hz,H-5),4.40~4.50(6H,m,6×OH)。13C-NMR(100 MHz,CD3OD)δ:73.8(C-4,6),75.0(C-l,3),74.8(C-2),77.0(C-5)。以上数据与文献[10]报道一致,故鉴定该化合物为肌醇。
化合物8:白色结晶,熔点为104~105℃,分子质量为110,分子式为 C6H6O2。1H-NMR(400 MHz,CD3OD)δ:7.65(2H,s,—OH),6.84(2H,m,H-3,6),6.56(2H,m,H-4,5)。13C-NMR(100 MHz,CD3OD)δ:143.5(C-1,2),121.7(C-3,6),125.4(C-4,5)。以上数据与文献[11]报道基本一致,故鉴定该化合物为邻苯二酚。
化合物9:白色粉末,分子质量为208,分子式为C8H16O6。ESI-MS:231(M+Na)+,439(2M+Na)+。1H-NMR(400 MHz,CD3OD)δ:1.21(3H,t,J=8.1 Hz,—CH3),3.88(2H,m,J=8.1 Hz,—CH2—),3.81(2H,m),3.52(1H,m,—OH),3.35(3H,m,3×OH),4.81(1H,d,J=7.0 Hz)。13C-NMR(100 MHz,CD3OD)δ:112.0(C-l),80.2(C-2),75.9(C-3),83.9(C-4),70.1(C-5),64.7(C-6),63.6(—CH2—),15.5(—CH3)。以上数据与文献[12]报道基本一致,故鉴定该化合物为α-乙基-D-呋喃葡糖苷。
化合物10:黄色不定形粉末,分子质量为178,分子式为C7H14O5。13C-NMR(100 MHz,CDCL3)δ:103.0(C-1),74.2(C-2),73.9(C-3),75.3(C-4),72.7(C-5),18.4(C-6),57.5(—OCH3)。以上数据与文献[12]报道基本一致,故鉴定该化合物为β-甲基-L-吡喃鼠李糖苷。
4 结论
本研究中,笔者从白枪杆树皮中一共分离鉴定出10个化合物,均为首次从该植物中分离得到,补充了该植物的化学成分数据库,可为进一步了解该植物的特性提供试验依据。
[1]国家中医药管理局《中华本草》编委会.中华本草:第六卷[M].上海:上海科学技术出版社,1999:161-162.
[2]江苏新医学院.中药大辞典:上册[M].上海:上海科学技术出版社,2000:720-721.
[3]He ZD,Shinichi U,Kenichiro I,et al.Secoiridoid glcosides from Fraxinus malacophylla[J].Phytochemistry,1993,35(1):177.
[4]ZhaoXH,Chen DH,SI JY,et al.Studies on the phenolic acid constituents from Chinese medicine“sheng-ma”,rhizome of Cimicifuga foetida L.[J].Yao Xue Xue Bao,2002,37(7):535.
[5]Takahisa N,Takashi K,Hiroshi T,et al.Glucosylation of caffeic acid with Bacillus subtilis X-23 α-amylase and a description of the glucosides[J].J Ferment Bioeng,1995,80(1):18.
[6]滕荣伟,王德祖,杨崇仁.蛇菰的化学成分[J].云南植物研究,2000,22(2):225.
[7]Chang J,Case R.Phenolic glycosides and ionone glycoside from the stem of Sargentodoxa cuneata[J].Phytochemistry,2005,66(23):2752.
[8]Tanahashi T,Takenaka Y,Nagakura N.Five trimeric secoiridoids glucosides from Jasminum polyanthum[J].Phytochemistry,1998,48(2):317.
[9]Machida K,Kaneko A,Hosogai T,et al.Studies on the constituents of Syringa species.X.Five new iridoid glycosides from the leaves of Syringa reticulata(Blume)Hara.[J].Chem Pharm Bull(Tokyo),2002,50(4):493.
[10]冯锋,朱明晓,谢宁.毛冬青化学成分研究[J].中国中药杂志,2008,43(10):732.
[11]王玲玲,刘斌,石任兵.荷叶的化学成分研究[J].天然产物研究与开发,2009,21(3):416.
[12]于德泉,杨峻山.分析化学手册:第7分册[M].2版.北京:化学工业出版社,1999:902.

