对铜的焰色反应与铜丝燃烧法实验的探究
曾应超
摘要:从原子发射光谱的角度,阐述了焰色反应的原理,并通过对铜的焰色反应以及铜丝燃烧法的实验及现象进行分析,指出两者在本质上均为铜的原子发射光谱,同时对进行铜的焰色反应时样品的选择给出了建议。
关键词:原子发射光谱;焰色反应;铜丝燃烧法
文章编号:1005–6629(2013)8–0049–02 中图分类号:G633.8 文献标识码:B
在进行焰色反应知识的教学时,不少教师常会补充介绍铜的焰色反应现象为绿色(铜的焰色反应在高中教材中并未提及),由于在教学中一般并不对焰色反应发生的难易程度进行分析,往往根据焰色反应为元素的性质这一特点,便简单推出铜单质在高中常用的火焰上灼烧时也应产生绿色火焰现象的结论。然而,苏教版《有机化学基础》中提到可用铜丝燃烧法对有机物中的卤素进行定性检测[1]:“将一根纯铜丝加热至红热,蘸上试样,放在火焰上灼烧,如存在卤素,火焰为绿色。”由于该现象与铜的焰色反应现象相同,难免让人产生困惑。下面结合具体实验,对此作一探析。
1 原子发射光谱与焰色反应
1.1 原子发射光谱
当基态原子受到加热或光照的激发,原子外层电子跃迁到较高的激发态,激发态的原子是不稳定的,在很短时间内电子又从高能态回到低能态,同时以光的形式放出多余的能量。原子从某一激发态跃迁回基态,发射出具有一定波长的一条光线,而从其他可能的激发态跃迁回基态以及在某些激发态之间的跃迁都可能发射出具有不同波长的光线,这些光线形成一个系列(谱),称为原子发射光谱[2]。原子发射光谱的产生过程中,样品首先需吸收能量实现原子化(转换为气态原子),然后才能进一步激发并自动退激产生发射光谱。
1.2 焰色反应
焰色反应[3],又称作焰色测试或焰色试验,是一种利用某些金属或它们的化合物在无色火焰上灼烧时会使火焰呈现特征的颜色的特性,实现对相关元素进行定性检测的方法。事实上,焰色反应属于原子发射光谱的范畴,其激发源为无色火焰,当激发态原子跃迁时所发射的光线波长在可见光波长范围内,就会使无色火焰着色,在火焰中观察到这种元素的特征焰色。根据原子发射光谱产生的过程不难发现,不同物质对火焰温度的要求不同,一般情况下,难挥发性物质将很难实现焰色反应,因此,焰色反应用于对碱金属和碱土金属元素进行定性检测较为有效。
2 铜的焰色反应实验及分析
通过对原子光谱数据进行查阅,发现铜的原子发射光谱中,存在波长在绿光波长范围内的特征谱线,因此,铜的焰色反应现象理应产生绿色火焰。为观察铜的焰色反应现象,分别选用酒精灯和酒精喷灯进行实验,实验方案和现象如表1所示。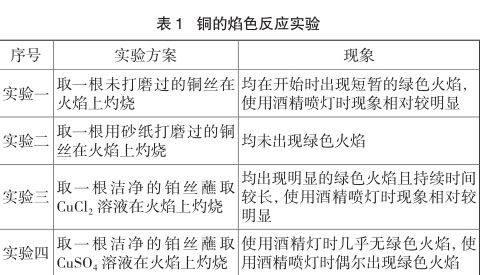
由于焰色反应属于元素的性质,上述实验的现象应该大致相同,然而实验中并未获得预期的结果。原因到底是什么呢?
根据原子发射光谱原理,实现焰色反应的第一步便是样品的原子化,其实现的难易程度与火焰温度以及样品的挥发性有关。从上述实验不难看出,相对而言,火焰温度越高,样品越易挥发,焰色反应现象越明显。由于铜单质和CuO熔沸点均较高,属于难挥发物质,在所选火焰温度下,难以实现原子化,以至“实验二”未出现绿色火焰。CuSO4在高温下易发生分解生成难挥发的CuO,造成“实验四”现象并不理想。那么“实验一”出现短暂的绿色火焰原因是什么呢?笔者以为,必定与铜丝表面附着物或在高温下生成的挥发性铜化合物有关,为验证此推测,进行了如下实验:
[实验五]取一根用砂纸打磨过的铜丝烧至红热后,分别蘸取稀盐酸在酒精灯和酒精喷灯火焰上灼烧,观察现象。
在“实验五”中,观察到明显的绿色火焰且持续时间较长,不难发现,该现象产生的原因在于高温下生成了易挥发的铜的氯化物。因此,“实验一”开始时观察到短暂的绿色火焰现象正是由铜丝表面附着物或高温下生成的挥发性铜化合物引起的。
3 用铜丝燃烧法定性检测有机物中卤素的实验及分析
为验证铜丝燃烧法能否实现对有机物中的卤素进行定性检测,分别选用酒精灯和酒精喷灯进行如下实验:
[实验六]分别取一根用砂纸打磨过的铜丝烧至红热后,蘸取CCl4在酒精灯和酒精喷灯火焰上灼烧,观察现象。
[实验七]分别取一根用砂纸打磨过的铜丝烧至红热后,蘸取1-溴丙烷在酒精灯和酒精喷灯火焰上灼烧,观察现象。
在上述实验中,均观察到明显的绿色火焰且持续时间较长,其中在酒精喷灯火焰上灼烧时现象相对更明显。
由上述“铜的焰色反应”系列实验可知,将纯铜丝烧至红热时,可去除铜丝表面的挥发性铜化合物,避免其造成干扰,同时在铜丝表面生成CuO,此时火焰为无色,再与含卤素的有机物一起灼烧时,便会生成铜的卤化物(与用铜丝蘸取稀盐酸灼烧时类似)。由于铜的卤化物易挥发,在火焰中原子化,引发铜的焰色反应,使火焰呈现绿色,因此可确定有机物中存在卤素,但对于是哪一种具体的元素并不能确定。可见,卤素的存在只是为了生成易挥发的铜的卤化物,便于铜的焰色反应的实现。
4 结论
从以上分析中不难看出,铜丝燃烧法产生绿色火焰的原理与铜的焰色反应原理相同,均为铜的原子发射光谱。由于产生原子发射光谱过程中,样品首先要实现原子化,因此,进行铜的焰色反应时,应选用挥发性较强的铜的卤化物(如CuCl2等),若选用难挥发的铜单质或CuO,则需要蘸取少量卤化物,使之灼烧时转化为易挥发物质,否则,在常规火焰温度下将难以实现,这正是可以利用铜丝燃烧法对有机物中卤素进行定性检测的原因。
参考文献:
[1]王祖浩主编.普通高中化学课程标准实验教科书·有机化学基础[M].南京:江苏教育出版社,2009:7.
[2]周公度,段连运编著.结构化学基础[M].北京:北京大学出版社,1995:87,101.
[3]王祖浩主编.普通高中化学课程标准实验教科书·化学1 [M].南京:江苏教育出版社,2009:22.

