白木香查尔酮合酶(AsCHS1)基因的克隆和生物信息学分析
汪孟曦,李文兰,张争,魏建和,杨云,徐艳红,梁良

[摘要] 目的:对国产沉香的源植物白木香Aquilaria sinensis查尔酮合酶(chalcone synthase,CHS)基因AsCHS1编码区进行克隆,并对其进行生物信息学分析和表达分析。方法:根据已报道的白木香伤害转录组高通量测序结果分析获得1条具有查尔酮合酶保守结构域的CHS基因序列,采用RT-PCR技术,以不同伤害时间白木香木质部混合样品总RNA为模板克隆得到白木香AsCHS1的基因编码区序列,并对AsCHS1蛋白进行理化性质、蛋白二级结构及三维结构预测分析。另外,采用qRT-PCR方法,以组蛋白(histones)为内参对AsCHS1基因在伤害胁迫下的表达模式进行分析。结果:序列分析表明,所克隆的AsCHS1基因编码区开放阅读框(opening reading frame, ORF)长为1 194 bp,编码397个氨基酸残基,命名为AsCHS1。qRT-PCR实验证明该基因表达量在伤害后12 h最大,说明该基因能够在早期响应伤害胁迫。结论:白木香AsCHS1基因的编码区序列的分离克隆为进一步研究AsCHS1蛋白在白木香中黄酮合成途径中的功能及表达调控奠定基础。
[关键词] 查尔酮合酶;白木香;黄酮合成
国产沉香为瑞香科植物白木香Aquilaria sinensis(Lour.)Gilg含树脂的木材。作为我国传统中药,沉香有具行气止痛、温中止呕、纳气平喘的功效,用于胸腹胀闷疼痛、胃寒呕吐呃逆、肾虚气逆喘急[1]。沉香为极珍贵芳香类药材,因其产量低、价格高,远远不能满足市场的需求。沉香叶的资源丰富,探讨沉香叶代替沉香药材的可行性是沉香研究开发中的一个重要研究方向。通过对沉香叶提取物的化学成分及药理研究,沉香叶中含有多糖、黄酮、苷类及酚类等化学成分[2-6],具有镇静、抗炎、止血、抗肿瘤、抗氧化等药理作用[7]。其中,黄酮类物质,如芫花素、木樨草素等均具有药理活性[8]。合成黄酮类化合物的关键酶之一是查尔酮合成酶(CHS)。通过研究查尔酮合成酶基因的结构,表达方式,在沉香中的黄酮合成和累积等方面,有助于明确白木香沉香中黄酮合成的分子机制,探索利用沉香中CHS基因提高沉香中的黄酮含量的可能性。本研究通过高通量测序获得CHS基因的cDNA全长序列,对其序列特征进行了生物信息学分析,通过荧光定量PCR技术研究该基因在处理不同时间的愈伤组织中的表达及积累情况,为进一步研究沉香中黄酮次生代谢调控机制奠定基础。
1 材料
2010年5月于海南省海口市演丰镇采集三年生栽培白木香A. sinensis茎(次生木质部已完全分化),经中国医学科学院药用植物研究所魏建和研究员鉴定,凭证标本保存于中国医学科学院药用植物研究所海南分所(凭证号2010003)。酒精灯火焰灭菌枝剪,待冷却后全断杆伤害处理2,6,12,24 h后,取全断杆横切面下1 cm厚的茎,剥去树皮后立即用液氮冷冻,存于-80 ℃备用。
大肠杆菌DH Escherichia coli 5α感受态、Taq Plus DNA Polymerase均购自北京天根生化科技有限公司;Total RNA Purification Kit 购于美国LC Science公司; M-MLV RTase cDNA Synthesis Kit,SYBR Premix Ex Taq,pMD19-T载体均为日本宝生物公司产品。本研究所用引物均由上海生工生物工程技术服务有限公司合成。基因测序由上海英潍捷基贸易有限公司完成。
PTC-200型梯度PCR扩增仪(Bio-Rad),Nano-Drop 2000核酸/蛋白定量仪(Thermo),台式高速离心机(Eppendorf),IQ5荧光定量PCR仪(Bio-Rad),凝胶成像系统(Bio-Rad),制冰机(Sanyo),超低温冰箱(Sanyo),高压蒸气灭菌锅(Sanyo)。
2 方法
2.1 白木香CHS基因的搜索和分析
张争等[9]报道了通过高通量测序方法对三年生的白木香伤害转录组进行了测序拼接,并通过与Swissprot、非冗余核酸数据库(Nt)、非冗余的蛋白数据库(Nr)和京都基因与基因组数据库(Kegg)公共数据库(E≤1×10-5)比对获得了注释结果。根据KEGG注释的基因功能信息,对参与次生代谢的序列(按次生代谢物种类) 进行分类。对所有注释信息整理,搜索黄酮类化合物生物合成途径中的关键酶基因。
2.2 白木香总RNA的提取和cDNA合成
取伤害处理的白木香茎,在液氮中研磨,依据LC Science公司Total RNA Purification Kit试剂盒说明书提取总RNA,利用NanoDrop 2000进行含量测定和1%琼脂糖凝胶电泳检测。利用TaKaRa公司的M-MLV RTase cDNA Synthesis Kit试剂盒将白木香总RNA反转录为第一链互补链DNA (cDNA)。反转录的反应条件及程序均按照TaKaRa公司的M-MLV RTase cDNA Synthesis Kit试剂盒说明书进行。
2.3 白木香AsCHS1 基因的克隆
从白木香转录组高通量测序结果中获得1个由7条表达序列标签拼接而成的1 368 bp的序列,经注释分析发现此片段是具有完整开放阅读框的CHS基因,其开放阅读框为1 194 bp,定名为AsCHS1。依据其两端序列利用Primer软件设计一对引物,序列见表1。以白木香总RNA的反转录产物为模板,按照下列体系对白木香的查尔酮合酶基因进行扩增:cDNA 3 μL, 10×Pfu buffer 5 μL,dNTP (2.5 mmol·L-1) 4 μL,Taq Plus (2.5 U·μL-1) 1 μL,10 μmol 引物各1 μL,终体积为50 μL。反应程序:94 ℃预变性2 min,然后进行30个循环,94 ℃ 1 min,55 ℃ 30 s,72 ℃ 1 min,循环结束后72 ℃延伸反应10 min,4 ℃保存。1%的琼脂糖凝胶电泳检测PCR产物,切胶回收。将回收的PCR产物与pMD19-T连接,转化到DH5α菌株,在氨苄抗性平板上进行蓝白斑筛选,再经PCR检测后送上海英潍捷基贸易有限公司测序。
2.4 AsCHS1基因信息学分析
基因的分析工具AsCHS1基因编码蛋白的理化性质预测采用ExPASy Proteomics Server提供的在线工具Protparam (http://www.expasy.ch/tools/protparam.html);采用SWISS-MODEL(http://swissmodel.expasy.org/)进行二级结构分析和结构域的三维建模,氨基酸序列比对利用ClustalW方法进行,通过MEGA 4.0构建Neighbor-joining系统进化树。
2.5 白木香AsCHS1基因在不同伤害处理时间的表达分析
利用实时荧光定量PCR(quantitative real-time PCR,qRT-PCR)的方法检测白木香愈伤组织中CHS基因在其不同伤害处理时间(对照CK,2,6,12,24 h)的表达情况。分析使用SYBR Green I荧光染料法,在qRT-PCR仪上进行。选取白木香Histone基因[10]作为目标基因定量表达的内参基因,引物序列见表1。每个样品设3个重复。反应体系中含有5 μL SYBR Premix Ex Taq酶,上下游引物(10 μmol·L-1) 各0.5 μL,模板(50 mg·L-1) 0.5 μL,ddH2O 3.5 μL,总体10 μL。反应程序:95 ℃预变性3 min;95 ℃变性30 s;59 ℃退火/延伸30 s (每次循环后采集荧光),40个循环;95 ℃变性10 s,65~95 ℃做熔解曲线分析,每个温度以每步0.5 ℃上升,每个温度停留5 s。试验数据通过Excel进行分析,获得AsCHS1基因的相对表达量。
3 结果与分析
3.1 白木香AsCHS1基因筛选
基于序列相似性搜索数据库中的序列信息对未知功能的序列进行注释。对白木香unigenes与核酸和蛋白质数据库(SwissProt,KEGG,Nr,Nt)进行BLASTN程序搜索。搜索结果发现其中1条contig12370,长1 247 bp,由7条reads拼接而成,具有完整的蛋白编码区,并对其进行了研究。
3.2 白木香AsCHS1 基因的克隆
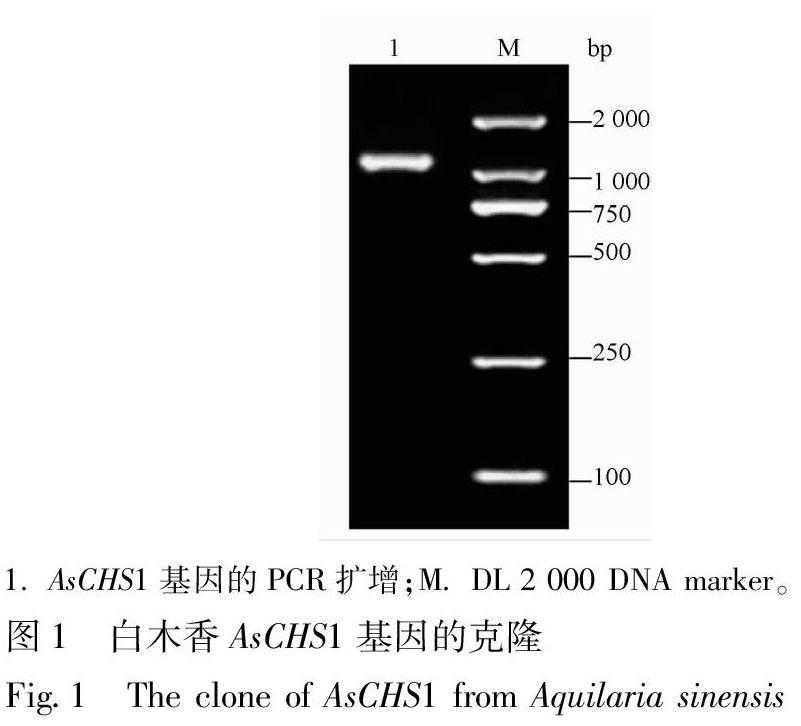
根据高通量测序结果,以白木香的cDNA为模板,利用PCR方法扩增获得1个1 194 bp的基因序列,397个氨基酸,GenBank登陆号JX573534。白木香CHS基因PCR扩增结果见图1。基因命名为AsCHS1,将其连接pMD19-T载体转化到大肠杆菌DH5α,测序结果经NCBI的Blast比对,确定其扩增产物为白木香CHS基因cDNA的片段。
3.3 白木香AsCHS1 基因编码蛋白特性分析
3.3.1 理化性质 白木香AsCHS1基因全长1 194 bp,编码397个氨基酸,利用ExPASy Proteomics Server提供的在线工具Protparam对基因编码蛋白的理化性质进行预测,推测该蛋白的分子式为C1939H3093N521O569S14,相对分子质量为43 kD,等电点pI 6.10;带正电残基(Arg+Lys)为40,负电残基(Asp+Glu)为44。该蛋白的不稳定系数为45.07,脂肪系数为98.87,亲水性系数为0.014。
3.3.2 二级结构及三级建模 二级结构在线预测结果表明,有163个氨基酸参与形成α-螺旋(alpha helix),占所有氨基酸的41.06%,有28个氨基酸参与形成伸展链(extended strand),占总氨基酸的9.57%,另有196个氨基酸参与形成无规则卷曲(random coil),占总氨基酸的49.37%(http://www.predictprotein.org/)。
利用SWISS-MODEL进行三维结构预测[11],通过PyMOL Viewer作图,三维模型见图2。用于建立该模型的氨基酸残基为6~390位,该模型以1cgzA(1.70 A)蛋白[12]为模板,序列同源性为61.8%。
3.4 氨基酸序列比对和基因进化分析
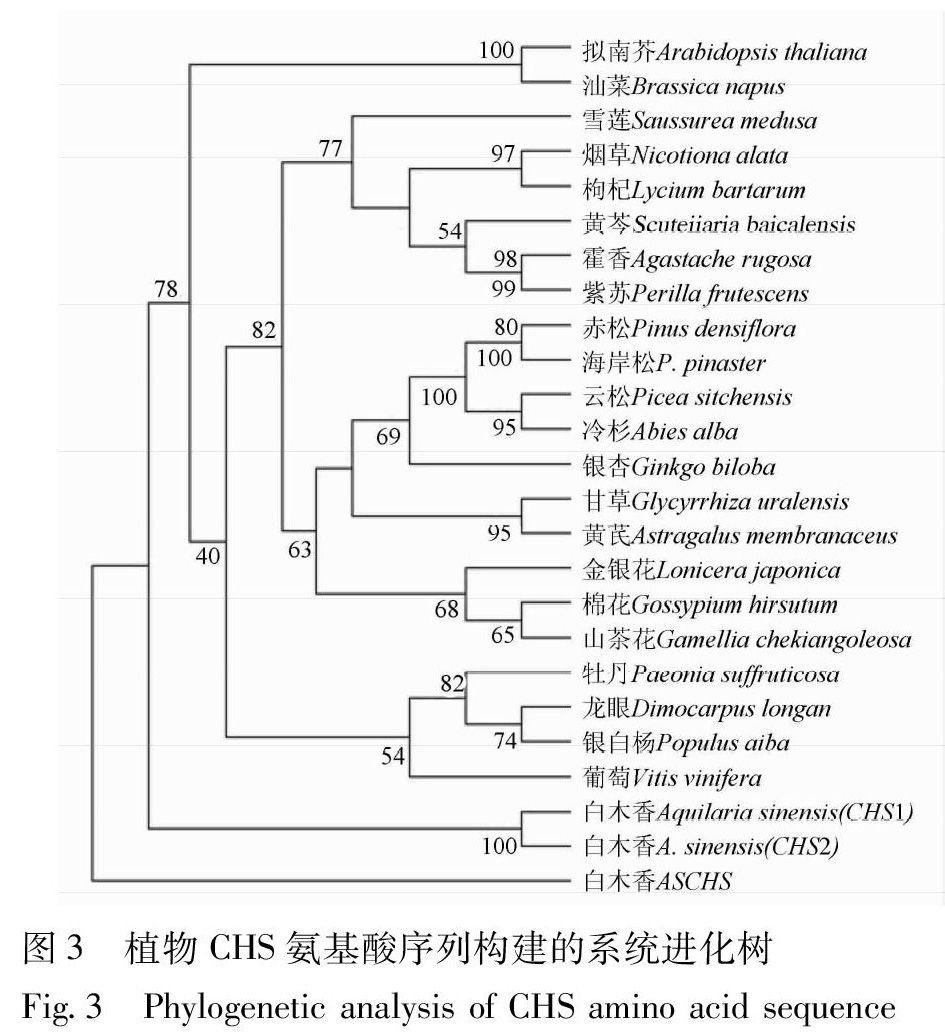
以AsCHS1序列进行Blast在线序列比对,结果表明AsCHS1基因的核苷酸序列与其他植物CHS基因的相似性较高,利用MEGA 4.0软件,采用邻结法(neighbor-joining, NJ)预测的白木香AsCHS1与其他代表性植物的氨基酸序列比对,见图3。结果显示,AsCHS1与已获得的白木香CHS有较高的相似性,与葡萄、拟南芥等植物的CHS蛋白相似性达64%。
3.5 白木香AsCHS1在不同伤害处理时间的表达分析
为研究AsCHS1基因在伤害胁迫下的表达模式,本研究采用qRT-PCR分别检测对照CK及伤害处理2,6,12,24 h后AsCHS1基因的表达情况,结果显示该基因在新鲜愈伤中表达量较低,该基因在伤害处理的24 h内表达水平显著升高,在12 h处基因表达量最高,是对照组表达水平的13.12倍,见图4。
4 讨论
黄酮类化合物是一类天然次生代谢物,广泛存在于植物中。黄酮在植物的色素积累,抗胁迫,抗菌 及细胞发育与分化中起着重要作用,同时还具有广泛的药理作用,如抗炎、抗氧化、抗肿瘤、降血压、保护心脑血管系统等多种生物活性[13]。查尔酮合酶作为黄酮类合成途径中的关键酶,其基因的突变,沉默或过表达会影响黄酮类物质的合成,对其功能和产量产生一定影响。查尔酮合酶基因的表达受植物激素、营养水平、光照、病原菌及机械伤害等的诱导[14]。本实验以伤害处理的白木香为材料成功克隆了AsCHS1基因全长,并采用生物信息学对其二级结构、三级结构等进行了预测,发现该基因编码的蛋白具有查尔酮合酶典型保守结构域,推测AsCHS1蛋白可能在白木香具有催化合成黄酮的作用,为进一步研究AsCHS1在白木香中黄酮合成途径中的功能及鉴定酶活性位点奠定基础。另外,本实验中qRT-PCR结果表明AsCHS1基因的表达受伤害胁迫诱导,其表达量在伤害后12 h最大,这为从分子水平上调控白木香中AsCHS1基因表达量以及提高白木香中黄酮化合物含量提供了基础数据。
[参考文献]
[1] 中国药典.一部[S]. 2010:172.
[2] Chen D, Bi D, Song Y L, et al. Flavonoids from the stems of Aquilaria sinensis[J]. Chin J Nat Med, 2012, 10(4):287.
[3] Qi J, Lu J J, Liu J H, et al. Flavonoid and a rare benzophenone glycoside from the leaves of Aquilaria sinensis [J]. Chem Pharm Bull, 2009, 57(2):134.
[4] Ito T, Kakino M, Tazawa S, et al. Quantification of polyphenols and pharmacological analysis of water and ethanol-based extracts of cultivated agarwood leaves [J]. J Nutr Sci Vitaminol, 2012, 58(2):136.
[5] 冯洁,杨秀伟.白木香叶化学成分的研究[J].中国中药杂志,2012,37(2):230.
[6] Dong C, Song Y L, Nie C X,et al. Chemical constituents from Aquilaria sinensis (Lour.) Gilg [J]. Acta Pharmacol Sin, 2012, 21:88.
[7] 路晶晶,戚进,朱丹妮,等.白木香叶中黄酮类成分结构与抗氧化功能的相关性研究[J].中国天然药物,2008,6(6):456.
[8] Hara H , Ise Y, Morimoto N, et al. Laxative effect of agarwood leaves and its mechanism [J]. Biosci Biotechnol Biochem, 2008, 72 (2), 335.
[9] 张争,高志晖,魏建和,等.三年生白木香机械伤害转录组学研究[J].药学学报,2012,47 (8):1106.
[10] Kumeta Y, Ito M. Characterization of δ-guaiene synthases from cultured cells of Aquilaria, responsible for the formation of the sesquiterpenes in agarwood [J]. Plant Physiol, 2010, 154:1998.
[11] Benkert P, Biasini M, Schwede T. Toward the estimation of the absolute quality of individual protein structure models[J]. Bioinformatics, 2011, 27(3):343.
[12] Ferrer J L, Jez J M, Bowman M E. Structure of chalcone synthase and the molecular basis of plant polyketide biosynthesis[J]. Nat Struct Biol, 1999, 6: 775.
[13] Majewska-Wierzbicka M, Czeczot H. Flavonoids in the prevention and treatment of cardiovascular diseases [J]. Pol Merkur Lekarski, 2012, 32(187):50.
[14] 张争,杨云,魏建和,等.环境因子导致的植物防御反应与药用次生代谢物的合成和积累[J].植物生理学通讯,2009,45(9):919.
Cloning and bioinformatics analysis of chalcone synthase
(AsCHS1) gene in Aquilaria sinensis
WANG Meng-xi1,2, LI Wen-lan1, ZHANG Zheng2,3*, WEI Jiang-he2,3, YANG Yun3, XU Yan-hong2, LIANG Liang4
(1.Drug Research Institute of Life Science and Environment Science, Harbin University of Commerce, Harbin 150076, China;
2. Institute of Medicinal Plant Development,National Engineering Laboratory for Breeding of Endangered Medicinal Materials,
Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100193, China;
3. Hainan Branch of Institute of Medicinal Plant Development, Chinese Academy of Medicinal Sciences & Peking Union
Medical College, Hainan Provincial Key Laboratory of Resources Conservation and Development of Southern Medicine,
Wanning 571533, China; 4. College of Pharmacy, Shandong University of Traditional Chinese Medicine, Ji′nan 250355, China)
[Abstract] Objective: The study aimed to clone the open reading frame of chalcone synthase (CHS) from Aquilaria sinensis and analyze the bioinformatics and expression of the gene. Method: One unique sequence containing CHS domain was discovered in our previous reported wound transcriptome dataset of A. sinensis. The open reading frame of CHS was cloned by RT-PCR strategy with the template of mixed RNA extracted from A. sinensis stem which treated by different wound time.The bioinformatic analysis of this gene and its corresponding protein was performed. The AsCHS1 expression in calli was analyzed with histone gene as an internal control gene under wound condition by qRT-PCR technique. Result: One unique sequence of CHS, named as AsCHS1, was cloned from A. sinensis. The full length of AsCHS1 cDNA was containing a 1 192 bp ORF that encoded 397 amino acids. The result of qRT-PCR displayed that the highest expression level was at 12 h, which indicated that it was possibly involved in early-stage response to wound. Conclusion: Cloning and analyzing AsCHS1 gene from A. sinensis provided basic information for study the fuction and expression regulation of AsCHS1 in the flavonoids biosynthesis .
[Key words] chalcone synthase; Aquilaria sinensis; flavonoids biosynthesis
doi:10.4268/cjcmm20130202
[责任编辑 吕冬梅]

