康莱特联合长春瑞滨+顺铂方案治疗晚期非小细胞肺癌疗效的Meta分析
严晓玲,顾艳荭
肺癌是常见的恶性肿瘤,近年来,其发病率和死亡率居恶性肿瘤之首[1],其中70%非小细胞肺癌(non-small-cell lung cancer,NSCLC)患者在确诊时已丧失了手术时机,化疗是主要的治疗手段[2]。美国食品和药物管理局(FDA)于1994年12月将长春瑞滨(NVB)与顺铂(DDP)联合应用作为不可切除的晚期非小细胞肺癌患者的一线方案[3],但临床上会出现消化道、肝肾功能损害及骨髓抑制等不良反应,如何提高联合化疗的疗效,减轻化疗的不良反应是临床医生不断探索的问题。康莱特(KLT)注射液是从薏苡仁中提取天然有效抗癌药物,实验药理学研究证实KLT对体内外多种肿瘤细胞具有较强的杀伤和抑制效果[4]。近年来,有关康莱特注射液联合长春瑞滨+顺铂(NP)方案化疗治疗晚期非小细胞肺癌的报道有增多,但其并未被临床广泛应用,且各研究的临床试验方法、临床疗效及毒副反应等方面的结果不尽相同。康莱特注射液联合NP方案治疗晚期非小细胞肺癌的有效性、安全性是否优于单纯NP方案,其是否能有效减轻毒副作用,现仍无可靠的循证医学证据。本研究收集了有关康莱特注射液联合NP方案治疗晚期非小细胞肺癌的随机对照试验(randomized controlled trial,RCT),采用Cochrane系统评价的方法,旨在客观评价康莱特注射液联合NP方案治疗晚期非小细胞肺癌的有效性和安全性,为其应用于临床提供真实可靠的依据。
1 资料与方法
1.1纳入标准(1)研究类型:纳入研究注明为临床随机对照试验。(2)干预措施:NP vs.(NP+康莱特)。(3)研究对象:成人,经病理/细胞学检查证实为晚期非小细胞肺癌患者,影像学检查临床诊断为IIIB 期或 IV 期;排除合并有其他恶性肿瘤患者;预计生存期>3个月;Kamofsky评分(KPS评分)≥60分。(4)结局指标:有效:按照WHO抗肿瘤药物客观疗效标准评价标准分为:完全缓解(CR),部分缓解(PR),好转(MR),无进展(SD),恶化(PD),有效=CR+PR。KPS评分改善:治疗后KPS评分较治疗前增加 10分以上,减退:治疗后KPS评分较治疗前减少10分以上,稳定:增加或减少≤10分者。体质量上升、胃肠道反应等。(5)治疗前4 周内未接受过其他抗肿瘤治疗,排除伴有严重内科疾患及感染,治疗前血常规、肝肾功能及血液系统功能,心电图正常,患者签署了知情同意书并接受随访。
1.2排除标准非随机对照临床试验,综述性研究,重复性文献。
1.3文献检索通过电子检索Pubmed、Cochrane Library、EMBASE、中国学术期刊全文数据库,万方科技期刊全文数据库,维普中文科技期刊数据库数据库,检索词包括“Kanglaite”、“ Kanglaite injection”、“NP program”、“non-small-cell lung cancer”、“randomized controlled trials”、“康莱特”、“康莱特注射液”、“NP方案”、“非小细胞肺癌”、“临床随机对照试验”等。检索时间为其建库至2012年2月20日。RCT检索策略遵循Cochrane系统评价手册5.0的要求,其他检索采用主题词与自由词相结合的方式,并根据具体数据库调整,所有检索策略通过多次预检索后确定。另外,用Google等搜索引擎在互联网上查找相关的文献,追查已纳入文献的参考文献,以获取以上检索未发现的相关信息。
1.4方法学质量评价与资料提取采用Cochrane协作网推荐的方法,对每个研究进行方法学质量评价,主要内容包括:(1)是否描述了具体的随机分配方法;(2)是否描述了随机分配方案隐藏的情况,方法是否正确;(3)是否采用盲法评价疗效,对哪些人实施了盲法;(4)是否描述了失访、退出的发生情况,是否进行了意向性分析。
1.5统计学方法 采用 Cochrane协作网提供的 RevMan 5.0 统计软件[5]进行Meta分析,各纳入研究结果间的异质性采用χ2检验,若P>0.1和I2<50%,采用固定效应模型进行分析;若存在统计学异质性P<0.1,I2>50%时,分析异质性来源,确定是否能采用随机效应模型。如果研究间存在明显的临床异质性,只对其进行描述性分析。
2 结果
2.1检索结果共检出相关文献40篇,均为在中国内地发表中文的文献,通过阅读全文排除重复文献22篇,去除无关文献4篇,去除包含NP方案以外另有其他方案的文献4篇,最后纳入10项符合标准的随机对照试验[6-15],共687例患者,研究流程图见图1。

图1 研究流程图
2.2纳入研究的特征纳入的10项研究[6-15]均以康莱特注射液联合NP方案为试验组,以单纯NP方案化疗为对照组。有效性指标:所有研究均报告了治疗有效率(CR+PR);8项研究[6-7,9-13,15]均描述了KPS评分,且有具体的数据,其中1项研究[13]把KPS提高和稳定率合并在一起描述,数据处理时未将其纳入,其余7项研究[6-7,9-12,15]以百分比的方式描述。4项研究[7,9-10,13]描述了化疗前后体质量的变化。安全性指标:4项研究[8-9,12,14]描述了胃肠道反应情况,3项研究[8,13-14]描述了肝功能的变化,3项研究[8,13-14]描述了肾功能的变化,1项研究[13]描述发生了静脉炎。
2.3纳入研究的一般情况和质量评价结果10项研究[6-15]均提及随机分组,只有一项研究[7]描述随机分配方法;所有研究均未提及盲法的实施;两项研究[7,10]描述了退出与失访的病例,但未进行意向性分析;所有研究均报告了试验组和对照组具可比性。各纳入研究的特征及方法学质量评价结果见表1。

表1 纳入研究的基本特征及方法学质量评价
注:①治疗有效率(CR+PR);②KPS评分;③血液不良反应;④胃肠道反应情况;⑤肝功能的变化;⑥肾功能的变化;⑦体质量变化;⑧发生了静脉炎
2.4Meta分析结果
2.4.1治疗有效率10项研究[6-15]均报告了治疗有效率,共687例患者,其中康莱特联合NP方案组346例患者,NP方案组341例患者,各研究间存在异质性(I2=68%),采用随机效应模型。结果显示:两组在有效率方面差异有统计学意义〔RR=1.66,95%CI(1.21,2.27),合并效应量的检验Z=3.14,P=0.002〕。见图2。
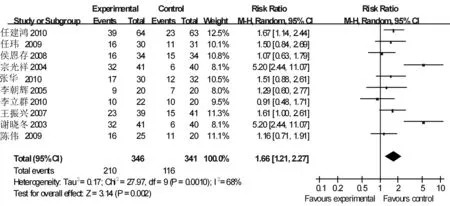
图2 治疗有效率的Meta分析
2.4.2 生活质量改善率对KPS评分提高10分以上的研究进行分析,各研究间存在异质性(I2=57%),采用随机效应模型。结果表明:与单用NP方案比较,康莱特注射液联合NP方案能更好地改善患者生活质量,二者比较差异有统计学意义〔RR=1.73,95%CI(1.34,2.23),合并效应量的检验Z=4.21,P<0.0001〕。见图3。
2.4.3体质量上升率4项研究[7,9-10,13]观察了化疗后体质量上升率,各研究间无异质性(I2=0%,P=0.51),采用固定效应模型,结果表明:与单用NP方案比较,康莱特注射液联合NP方案患者的体质量明显升高,二者比较差异有统计学意义〔RR=1.81,95%CI(1.35,2.43),合并效应量的检验Z=3.96,P<0.0001〕。见图4。
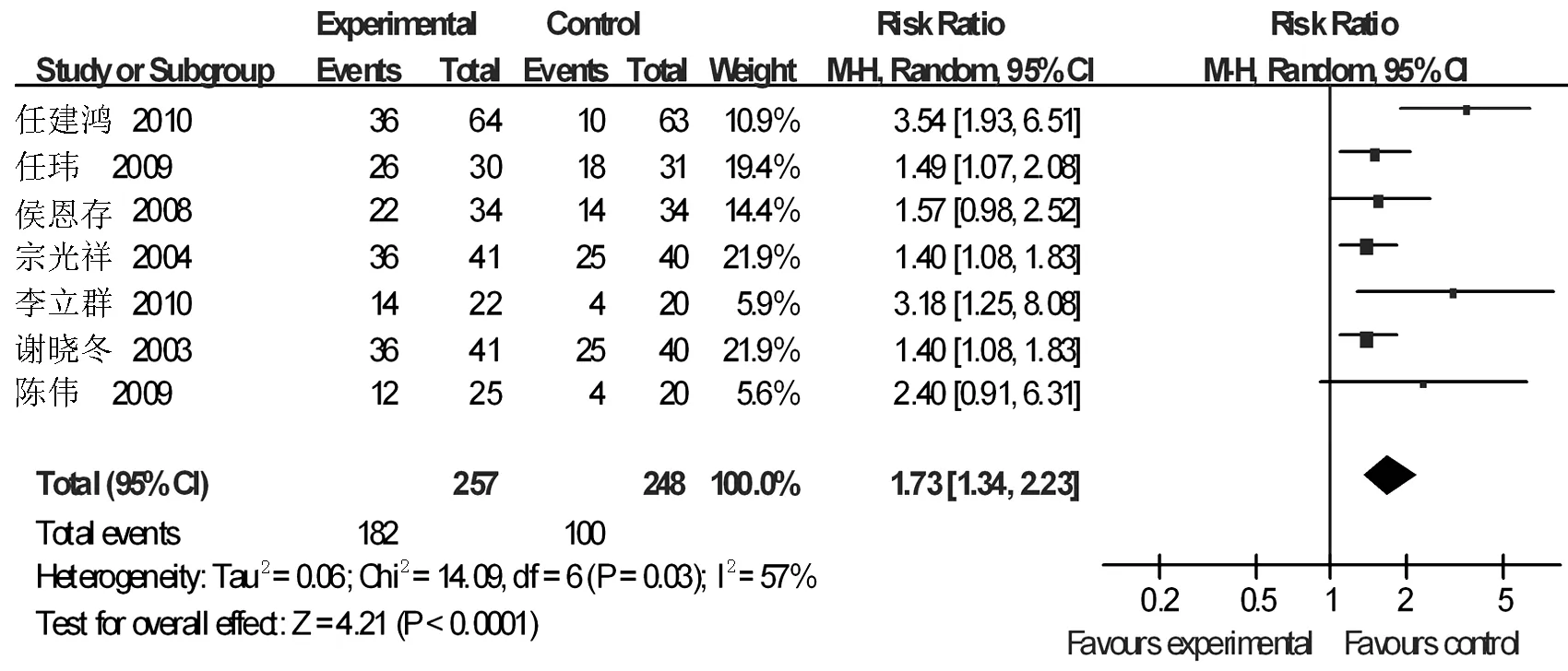
图3 生活质量改善率的Meta分析

图4 体质量上升率的Meta分析
2.4.4胃肠道不良反应发生率4项研究[8-9,12,14]报告了Ⅱ度以上恶心呕吐发生率,有详细的数据资料。各研究间无异质性(I2=0%,P=0.75),采用固定效应模型,结果表明,在恶心呕吐发生率方面,康莱特注射液联合NP方案治疗晚期非小细胞肺癌较单纯GP方案化疗低,差异有统计学意义〔RR=0.67,95%CI(0.47,0.97),合并效应量的检验Z=2.13,P=0.03〕。见图5。
2.4.5敏感性分析康莱特联合NP方案和单纯使用NP方案在治疗有效率和生活质量改善率方面各研究间存在异质性,现将治疗有效率和生活质量改善率分别再次采用固定效应模型进行分析(见图6、7),结果显示采用不同的效应模型得出的结论一致,说明本研究Meta分析结果的稳定性较好。
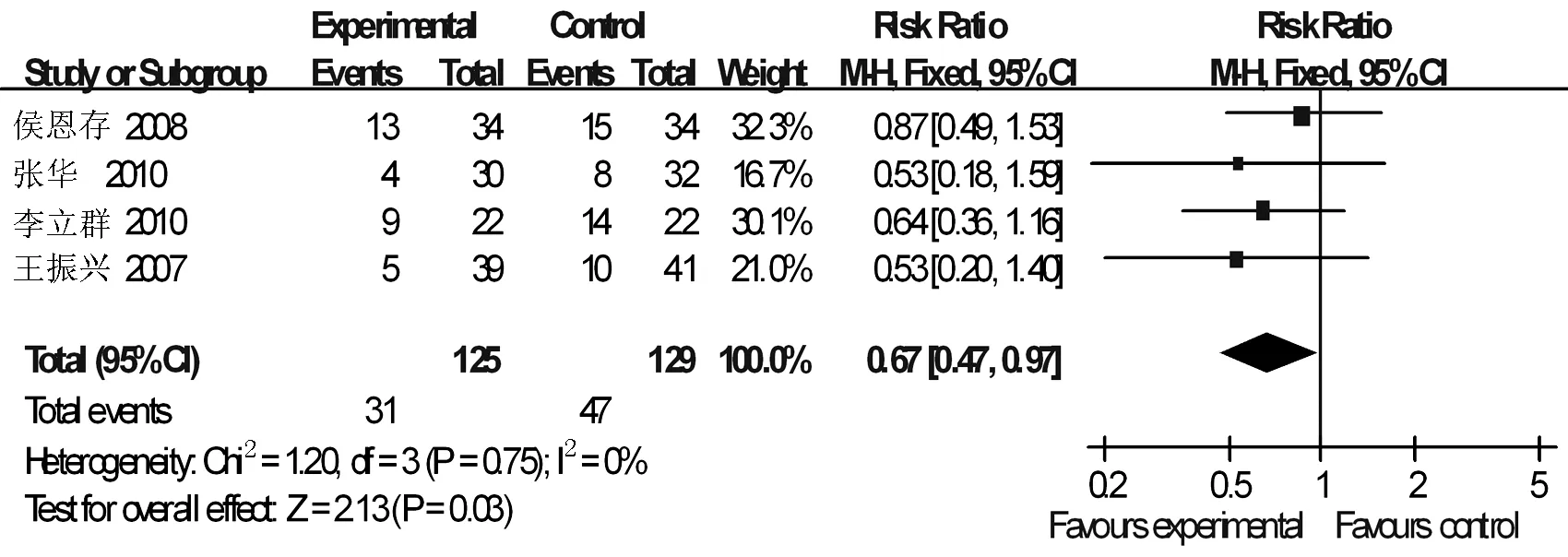
图5 胃肠道不良反应发生率的Meta分析
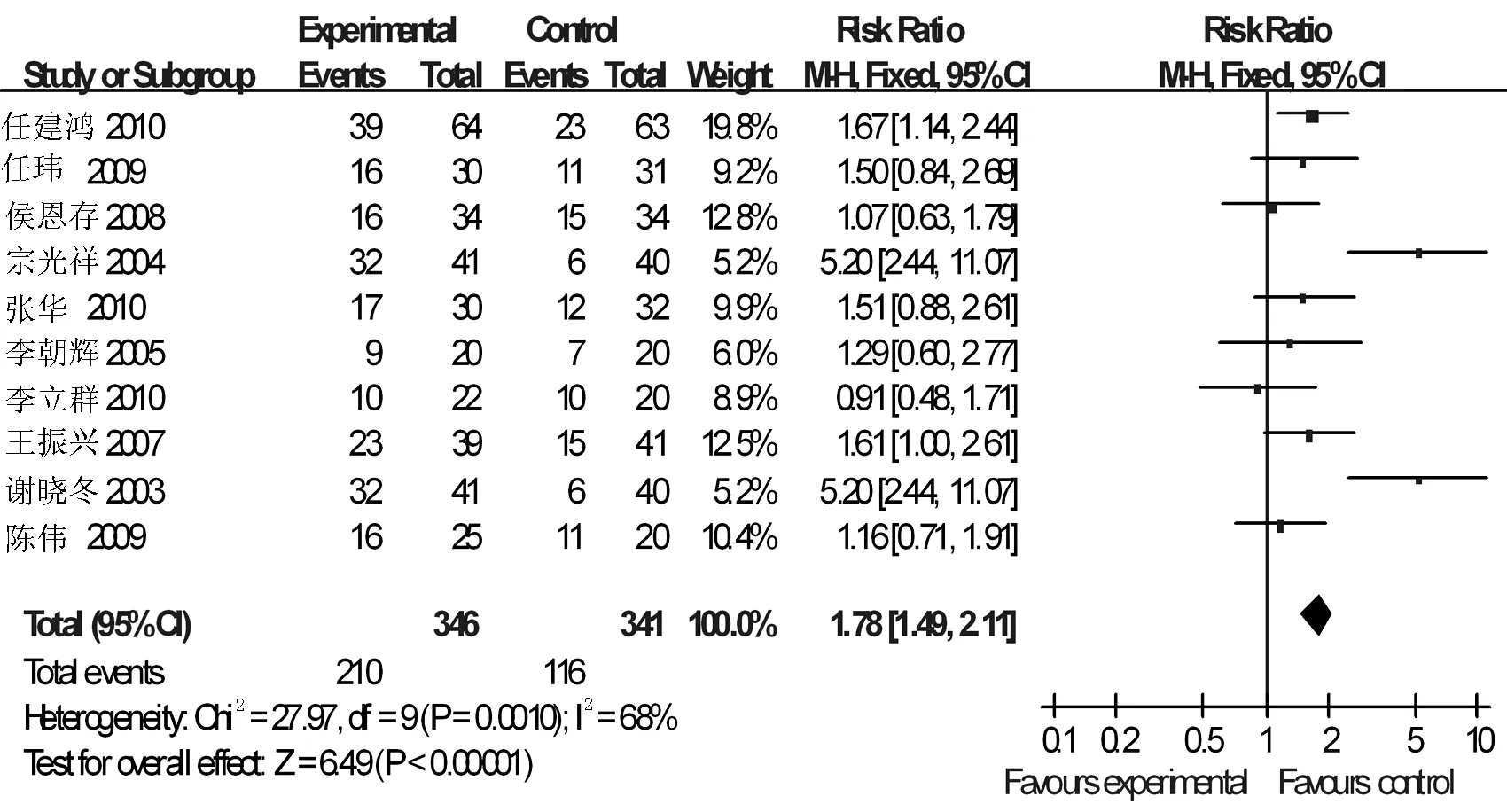
图6 治疗有效率的Meta分析
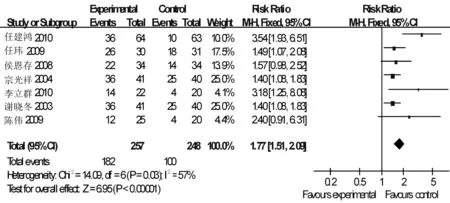
图7 生活质量改善率的Meta分析
2.4.6发表偏倚用 10项研究[6-15]的近期有效率指标绘制“漏斗图”,其呈不对称的散点图,说明存在发表性偏倚的可能。见图8。
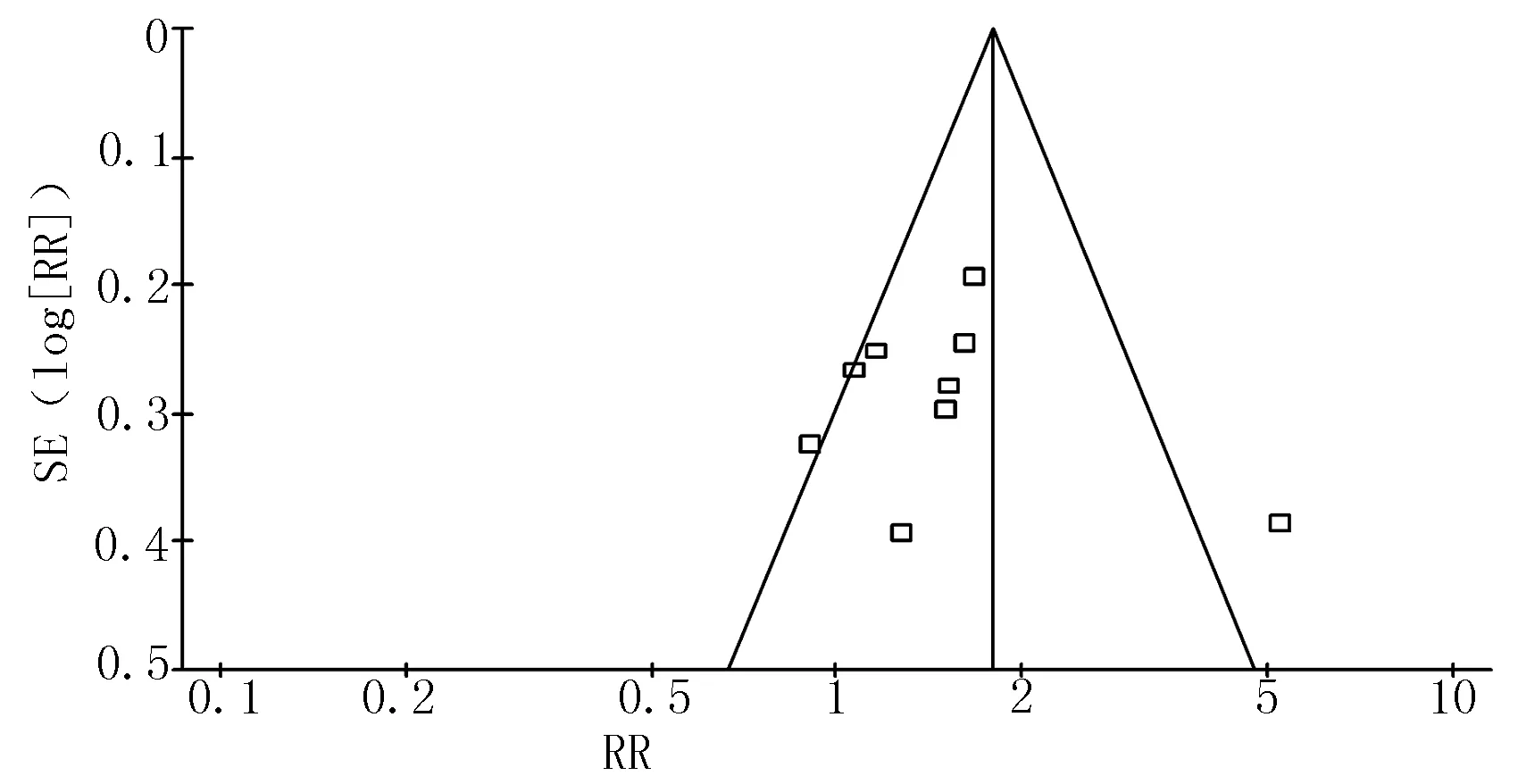
图8 漏斗图
3 讨论
康莱特作为抗肿瘤制剂,是从传统中药薏苡仁中提取分离的一种抗癌活性化合物[16],按中医药理论,其性味平甘,无毒,入肺脾经,有补益中气、消瘀散结的功效[17]。潘沛等[18]报道,康莱特注射液能通过降低肿瘤组织中EGFR 的蛋白表达量,抑制肿瘤血管生成,从而抑制小鼠Lewis 肺癌的生长。吴岩等[19]通过小鼠Lewis 肺癌模型研究发现,康莱特注射液在抗肿瘤的同时,能提高T细胞增殖活力,调节白介素2、核因子-KB 等细胞因子的表达,增强机体免疫功能。王云杰等[20]报道,康莱特注射液能使癌细胞停滞于G2/M期,抑制肿瘤细胞的增值,诱导肿瘤细胞的凋亡。谭煌英等[21]报道,康莱特注射液通过降低大鼠由完全福氏佐剂致炎皮肤水平促炎细胞因子、肿瘤坏死因子-α、白介素Iβ水平,升高大鼠痛阈,起到镇痛的效果。
本文通过Meta分析的方法对康莱特注射液与NP化疗方案联合应用治疗晚期非小细胞肺癌的有效性进行分析,表明其与NP方案化疗相结合可提高治疗有效率,提高生活质量,减少化疗不良反应。康莱特具有辅助治疗等有利于临床的作用,值得临床推广。
本系统评价纳入的研究存在如下局限性:(1)大部分研究未提及样本量估算的依据,且样本量较小,影响检验效能;(2)纳入研究中仅一项研究[7]描述随机方法,无一项实施隐蔽分组,不实施或不充分实施隐蔽分组会导致疗效评价不客观;(3)纳入的所有研究均未说明盲法的实施,未实施盲法会直接导致实施偏倚和测量偏倚的发生;(4)由于在评价疗效时部分采用主观性指标,人为因素影响结果的可能性较大,而未充分实施盲法会直接导致实施偏倚和测量偏倚的发生;(5)纳入研究对部分结果采用不同的统计量,致使有些试验不能合并,无法得出统一结论;(6)所纳入的研究在康莱特的使用量及使用时间上有不一致,这对最终的测量指标将会产生一定的影响。
综上所述,康莱特注射液联合NP化疗方案在治疗晚期非小细胞肺癌方面,优于单纯使用NP化疗方案,康莱特具有辅助治疗作用,值得临床推广。但本Meta分析所纳入的研究临床试验质量不高,临床研究方法不完全正确,且样本较少,所以其临床应用的确切疗效尚需设计严密、实施科学的大样本研究进一步证实。
1Jemal A,Thun MJ,R Ies LA,et al.Annual report to the nation on the status of cancer,1975—2007,featuring trends in lung cancer,tobacco use,and tobacco control[J].J Nat l Cancer Inst,2008,100(23):1672-1694.
2许英爱.一种新型的治疗非小细胞肺癌的抗肿瘤药长春瑞宾[J].国外医学药学分册,2002,24(2):82-84.
3潘启超.长春碱类的新进展:失碳长春碱[J].癌症,1996,15(3):228-231.
4李大鹏,康莱特注射液抗癌作用机理研究进展[J].中医新药与临床药理,2001,12(2):122-124.
5Revie MA.Computer program[M].Copenhagen:The Nordic Cochrane Center,2008:204-205.
6任玮.康莱特注射液联合化疗治疗晚期非小细胞肺癌30例[J].实用中医内科杂志,2009,23(3):39.
7谢晓冬,郑振东,高雅苓.康莱特对局部晚期非小细胞肺癌患者生活质量改善的临床对照研究[J].中国实用内科杂志,2003,23(11):677-678.
8张华,戚锐锋.康莱特注射液联合NP方案治疗晚期非小细胞肺癌临床观察[J].现代肿瘤学,2010,18(5):927-928.
9李立群.康莱特注射液联合NP 方案治疗非小细胞肺癌的临床观察[J].中医杂志,2010,51(2):164-165.
10宗光祥.康莱特对中晚期非小细胞肺癌患者生活质量的改善作用[J].基层医学论坛,2004,8(11):329-330.
11李朝辉,吕金芳,周立中.康莱特注射液联合NP 方案化疗治疗局部晚期非小细胞肺癌的临床观察[J].肿瘤防治杂志,2005,12(17):1339-1340.
12侯恩存.康莱特注射液联合化疗治疗非小细胞肺癌临床观察[J].中医新药与临床药理,2008,19(6):504-505.
13任建鸿,王红,刘丽梅.康莱特注射液联合NP 方案化疗治疗老年晚期非小细胞肺癌的临床观察[J].现代生物医学进展,2010,10(17):3275-3278.
14王振兴,张振国.康莱特注射液联合NP方案治疗晚期非小细胞肺癌临床疗效观察[J].河北医药,2007,29(1):47-48.
15陈伟,曲涛.康莱特联合NP 方案治疗晚期非小细胞肺癌45例临床观察[J].临床医药实践,2009,18(6):427-428.
16李大鹏.康莱特抗肿瘤的研究论文集[M].杭州:浙江大学出版社,2001:176.
17张明,谢可,陈琳.薏苡仁甘油三酯注射液改善晚期肿瘤患者食欲和生存质量的临床观察[J].肿瘤防治杂志,2003,10(12):1304.
18潘沛,吴岩,王蓉,等.康莱特注射液在Lewis肺癌中对肿瘤生长及EGFR蛋白表达的影响[J].中国临床药理学与治疗学,2010,15(1):32-35.
19吴岩,潘沛,王彧杰,等.康莱特注射液对Lewis 肺癌小鼠免疫功能的影响[J].上海交通大学学报(医学版),2009,19(12):1455-1458.
20王云杰,黄立军,张志培,等.康莱特注射液治疗原发性肺癌的临床研究[J].现代肿瘤医学,2006,14(8):964-965.
21谭煌英,李园,于莉莉,等.康莱特注射对大鼠的镇痛作用及其对促炎细胞因子的影响[J].中国中西医结合外科杂志,2007,13(4):152-155.

