pH 和NaCl对马铃薯、玉米淀粉黏度特性的影响
黄峻榕 薛 婷 魏宁果 李宏梁 刘树兴 杨大庆
(陕西科技大学生命科学与工程学院,陕西 西安 710021)
淀粉是由葡萄糖单元组成的多糖,经绿色植物利用二氧化碳与水进行光合作用合成,在自然界中可形成良性循环,通常以颗粒的形式贮藏在大多数高等植物的器官中及某些原生动物、藻类和细菌中。淀粉颗粒一般不溶于冷水,在含水体系中加热至一定温度可发生糊化。淀粉糊化后形成淀粉糊,属于非牛顿流体,该流体的黏度实际为表观黏度,除了与温度有关外,还与剪切速率、时间有关,并有剪切变稀或剪切变稠的变化[1]。不同来源的淀粉具有不同的黏度性质,同一淀粉在不同条件下的黏度性质也有较大差别[1,2]。大多数含淀粉食品(如方便面、酸奶、沙拉酱等)中,含有食盐、乳酸、乙酸等成分,这些小分子电解质会改变体系的pH 值和离子强度。
在已有关于pH 和NaCl对淀粉黏度性质影响的研究报道中,有学者[3]认为pH 是影响马铃薯淀粉黏度特性的重要因素,在pH=7时,黏度最大。Muhrbeck等的研究[4]表明:pH 对马铃薯淀粉的凝胶性质有很大影响,在pH 为8.5时,凝胶强度最大。Eliasson 等的研究结果[3]表明:对于NaCl而言,在NaCl的浓度为10-5mol/L 时,对马铃薯淀粉的黏度产生了很小但是很明显的抑制效果;当NaCl的浓度由10-5mol/L增加至0.1 mol/L 时,马铃薯淀粉的黏度增加;玉米淀粉的黏度在NaCl的浓度增加至10-3mol/L 时没有变化。随着NaCl的浓度由0.2mol/L增加至1.1mol/L,马铃薯淀粉的各点黏度值降低[5]。当NaCl浓度由0.5%增加至2.5%时,玉米淀粉的黏度降低[6]。上述研究在分析pH和NaCl对淀粉黏度的影响时都没有考虑离子强度这个因素。而相关研究[4,7]表明:离子强度对马铃薯淀粉的凝胶性质有很大影响,随着离子强度增大,其凝胶强度显著降低。马铃薯淀粉的黏度特性对离子强度非常敏感,在最低离子强度条件下,马铃薯淀粉糊的黏度可达最高[3]。离子强度对于马铃薯淀粉黏度特性的影响只与离子强度有关而与离子类型无关,在同一离子强度下,所有离子的影响相同。其他淀粉则受离子类型的影响,即盐的类型和浓度都会影响淀粉的黏度特性[3]。本课题拟在测定离子强度的基础上,采用快速黏度分析仪,研究pH、NaCl对马铃薯淀粉、玉米淀粉黏度性质的影响,研究结果将为进一步分析复杂食品体系对淀粉黏度性质的影响奠定基础。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
三边马铃薯淀粉:陕西定边源泽公司三边裕丰精淀粉厂;
新田源马铃薯淀粉:榆林市新田源集团富元淀粉有限公司;
玉米淀粉;北京可口林工贸有限公司;
纯净水:西航天鼎纯净水有限公司;
蒸馏水:本实验室自制;
乙酸、氢氧化钠、氯化钠:分析纯,天津市天力化学试剂有限公司。
1.1.2 主要仪器设备
分析天平:BS323S 型,赛多利斯科学仪器(北京)有限公司;
快速黏度分析仪:TechMaster型,RVA 波通瑞华科学仪器(瑞典)公司;
酸度计:PB-10型,赛多利斯科学仪器(北京)有限公司;
电导率仪:DDS-307 型,上海仪电科学仪器股份有限公司;
断水自控蒸馏水器:HS-Z68-5D 型,北京科伟永兴仪器有限公司。
1.2 方法
1.2.1 溶液配制
(1)pH 缓冲液的配制:以蒸馏水分别配制0.01 mol/L乙酸溶液和氢氧化钠溶液。0.01 mol/L 乙酸溶液的pH 值为3.4。pH 值为4,5,6,7,8,9,10,11的缓冲液用0.01mol/L乙酸溶液和氢氧化钠溶液配制,并测定电导率。
(2)NaCl 溶液的配制:用蒸馏水分别配制浓度为0.5%,1.0%,1.5%,2.0%,2.5%,3.0%的NaCl溶液,并测定pH 值和离子强度。电导率仪所用的电极常数为1cm-1,电导率的测量范围为2.0×10-3~10.0 mS/cm,1.0%及更高浓度的NaCl溶液的电导率超出了量程,所以根据式(1)进行离子强度的计算:
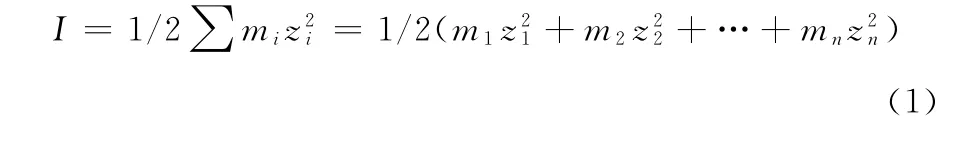
式中:
I—— 溶液的离子强度,mol/L;
mi—— 离子的摩尔浓度,mol/L;
zi—— 离子的价数,取1,2,…,7;
n—— 代表各种离子。
1.2.2 淀粉水分含量的测定 参照GB/T 12087-2008的方法。
1.2.3 淀粉黏度特性曲线的测定 采用快速黏度仪(RVA)测定不同条件下淀粉的糊化特性。准确称取用相应溶液配成的5% (DB,m/m)淀 粉 悬 浮 液28 g,最 初10 s 以960r/min搅拌,之后保持160r/min至测定结束。起始温度为50 ℃保持1 min,然后经3.7 min提高至95 ℃,并保持2.5min,在3.8min内降至50 ℃并保持2min,整个测定过程历时13min。由分析软件获得淀粉在糊化过程中的黏度变化曲线以及多个特征点,包括糊化温度、峰值黏度、谷值黏度、最终黏度、衰减值和回生值。
2 结果与分析
2.1 水、pH 缓冲液、NaCl溶液的pH 值和离子强度
由表1可知,蒸馏水、纯净水和自来水的pH 均在7 左右。液体的离子强度大小可用电导率表示,电导率越大,则离子强度越大。蒸馏水、纯净水的离子强度接近,显著低于自来水的离子强度。自来水是经过净化、消毒等工序生产出来的符合国家饮用水标准的生活、生产用水,里面含有Mg2+,Ca2+,Cl-,ClO-等离子[8]。蒸馏水是纯净水的一种,基本不含矿物质离子,因而,本试验所有溶液的配制均采用离子强度最小的蒸馏水。

表1 水、NaCl溶液的pH 值和离子强度Table1 pH value and ionic strength of different water and NaCl solution
随着pH 值的递增,缓冲液的离子强度如表2 所示:pH 3.4~6.0 离子强度逐渐增大;pH 6.0~10.0 离子强度趋于平 稳;pH 11.0 离 子 强 度 最 大。pH 3.4 的 溶 液 为0.01mol/L乙酸溶液,乙酸为弱酸,因而离子强度较弱;pH 4.0~6.0的溶液在配制时为碱加入酸,NaOH 为强碱,浓度为0.01mol/L 时,离 子 强 度 为2.03 mS/cm,远 远 大 于0.01mol/L乙酸的离子强度,因而随NaOH 加入量的增加,溶液的离子强度随着pH 的增加逐渐增大;pH 7.0~11.0时,为酸加入碱,pH 7.0~10.0时,乙酸的加入,对溶液的离子强度影响较小,pH 11.0时,乙酸的加入量最小,因此离子强度最高。
随着NaCl溶液浓度的升高,离子强度呈递增趋势,但pH 值变化不大。这主要是因为NaCl为强酸强碱盐,在水溶液中可以完全电离,因而NaCl溶液为中性,pH 值不随浓度发生变化。
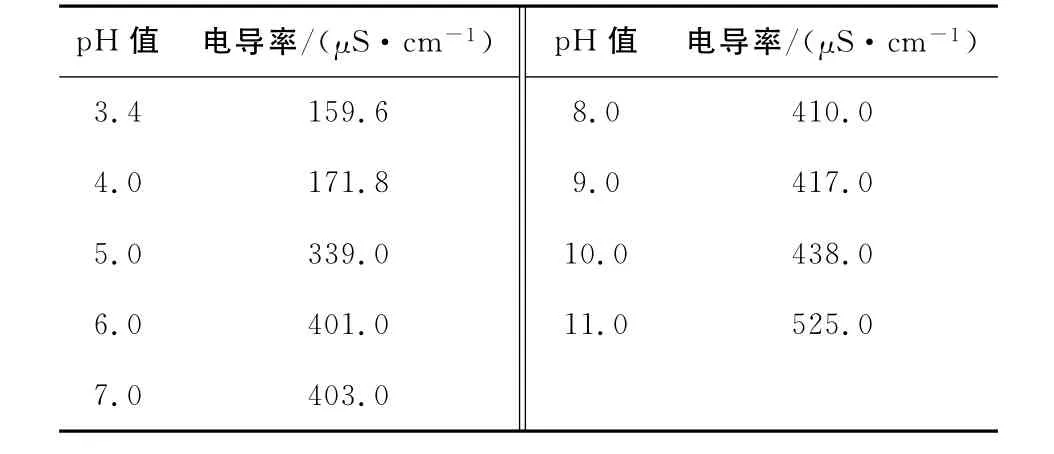
表2 pH 缓冲液的离子强度Table2 The ionic strength of the pH buffer solution
2.2 水对马铃薯、玉米淀粉黏度特性的影响
三边马铃薯淀粉、新田源马铃薯淀粉和玉米淀粉的水分含量分别为16.5%,12.5%,8.6%。玉米淀粉的水分含量显著低于马铃薯淀粉的,主要是因为马铃薯淀粉分子中的羟基自行结合形成氢键的程度较小,所剩余的羟基数目相对较多,通过氢键与水分子相结合的机会较多,因而其结合水的能力较玉米淀粉的大[9]。
马铃薯淀粉在蒸馏水和纯净水中的黏度曲线接近(见图1、2),在自来水中,三边、新田源马铃薯淀粉的峰值黏度分别比在蒸馏水中的降低了26%和52%,谷值黏度和最终黏度也明显降低,说明离子强度的增加可降低马铃薯淀粉的黏度。由于磷酸基团的存在使得马铃薯淀粉在溶液中具有电荷性,并具有阳离子交换功能,对离子比谷物淀粉更加敏感,因而,加工过程中的水质、离子会影响马铃薯淀粉的性质[3]。在同样的测试条件下,三边、新田源马铃薯淀粉的峰值黏度、谷值黏度和最终黏度,以及回生值、衰减值都不相同,说明淀粉的黏度性质受马铃薯品种、生长环境和淀粉生产工艺等因素的影响。
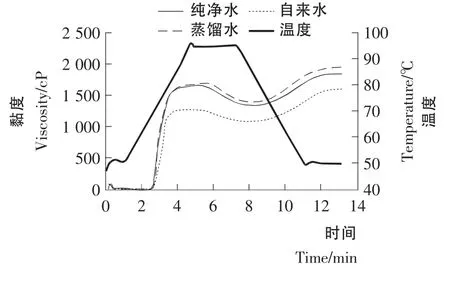
图1 不同的水对三边马铃薯淀粉黏度特性的影响Figure1 Effect of different water on pasting behaviors of Sanbian potato starch
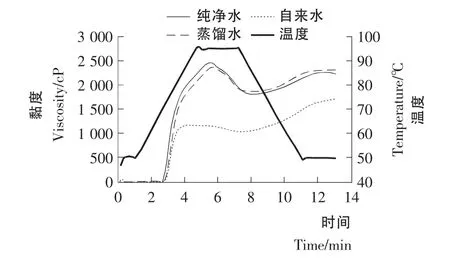
图2 不同的水对新田源马铃薯淀粉黏度特性的影响Figure2 Effect of different water on pasting behaviors of Xintianyuan potato starch

图3 不同的水对玉米淀粉黏度特性的影响Figure3 Effect of different water on pasting behaviors of corn starch
玉米淀粉在蒸馏水、纯净水和自来水中的峰值黏度逐步降低(见图3),在自来水中的最终黏度值最大,但总体黏度变化幅度不大,说明离子强度对玉米淀粉黏度特性影响较小。玉米淀粉的糊化温度(93.7 ℃)高于三边马铃薯淀粉(69.5 ℃)和新田源马铃薯淀粉(71.9 ℃)的糊化温度,即马铃薯淀粉比玉米淀粉容易糊化。马铃薯淀粉的微结晶结构具有弱的均一的结合力,玉米淀粉的微结晶结构是弱力和强力两种力结合,具有两段膨胀的性质,并且属强力结合,需比马铃薯淀粉高10 ℃以上的温度才能实现糊化[10]。此外,淀粉糊化的难易与淀粉的分子结构和直链淀粉含量有直接关系,糊化的本质是水分子进入淀粉粒中使淀粉分子之间的氢键断裂,破坏淀粉分子之间的缔合状态,一般颗粒大或结构松散的淀粉比颗粒小、结构紧密的淀粉易糊化,马铃薯淀粉颗粒较大,结构较为松散,直链淀粉含量较低[11],故比玉米淀粉易于糊化[12]。
7.1.3 Flood, mud-rock flow and countermeasures against them
目前最常用的淀粉糊化温度测定方法有布拉本德黏度仪法和快速黏度仪法。Pérez等的测试[13]表明,用快速黏度仪法测定得到的糊化温度都比布拉本德黏度仪法的测定值高。这是由于两种方法采用的升/降温速率以及搅拌速率都不同,而淀粉糊化受温度和搅拌速率的影响都非常显著[14]。本试验中淀粉糊化温度由快速黏度仪法测定获得,因而比采用布拉本德黏度仪法的测定值高。
2.3 pH 对马铃薯、玉米淀粉黏度特性的影响
在由0.01mol/L乙酸溶液和氢氧化钠溶液配制的缓冲液中,随着pH 值升高,三边马铃薯淀粉黏度变化不大;新田源马铃薯淀粉黏度在pH 4.0~5.0有一定的波动,但pH 3.4和pH 6.0~11.0之间的黏度值相近,因此,总的趋势为pH对马铃薯淀粉黏度的影响不大(见图4、5)。而马冰洁等[5]用强碱(氢氧化钠)和强酸(盐酸)配制pH 溶液,研究结果表明,在pH<7时,随着pH 值降低,马铃薯淀粉各点黏度值降低,pH≥7时,随pH 值增加,马铃薯淀粉黏度增高。与本研究结果有所不同,这是由于所用pH 溶液的差异。在pH 3.4~11.0范围内,两种马铃薯淀粉的糊化温度变化不大,最终黏度都大于峰值黏度;但三边马铃薯淀粉的衰减值大于新田源马铃薯淀粉的,而回生值则相反;说明两种马铃薯淀粉的糊化难易程度相近,但三边马铃薯淀粉的热稳定性较差,而凝胶性能较好。

图4 pH 对三边马铃薯淀粉黏度特性的影响Figure4 Effect of pH on pasting behaviors of Sanbian potato starch

图5 pH 对新田源马铃薯淀粉黏度特性的影响Figure5 Effect of pH on pasting behaviors of Xintianyuan potato starch
由图6可知,pH 由3.4升高至10.0时,玉米淀粉的峰值黏度、谷值黏度、最终黏度、衰减值的变化不大,pH 11.0时,玉米淀粉峰值黏度与pH 3.4~10.0相比略低,可能是由于pH 11.0时离子强度最大,对玉米淀粉黏度产生了影响。在pH 11.0时回生值与pH 3.4~10.0相比略高,说明此时玉米淀粉的凝胶强度最大。玉米淀粉在酸性条件下的衰减值略大于碱性条件下,这说明玉米淀粉在碱性条件下的黏度稳定性比在酸性条件下的稍好。
2.4 NaCl对马铃薯、玉米淀粉黏度特性的影响

图6 pH 对玉米淀粉黏度特性的影响Figure6 Effect of pH on pasting behaviors of corn starch
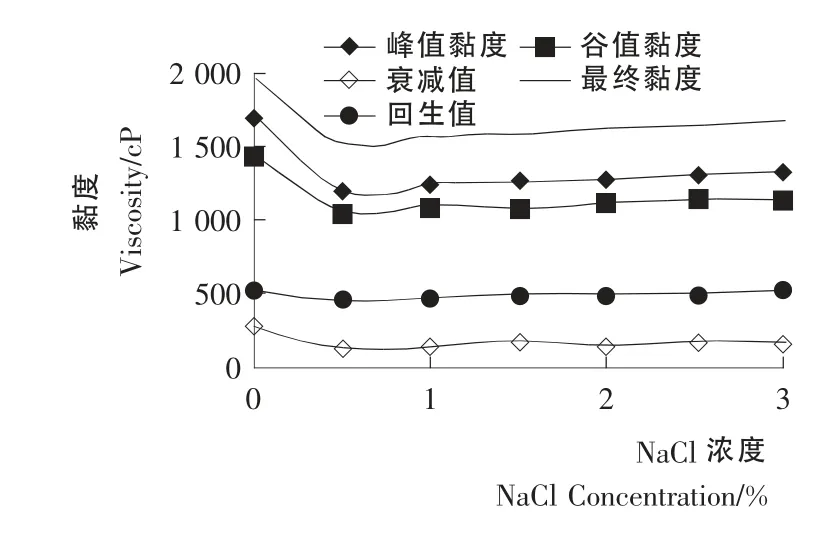
图7 NaCl对三边马铃薯淀粉黏度特性的影响Figure7 Effect of NaCl on pasting behaviors of Sanbian potato starch

图8 NaCl对新田源马铃薯淀粉黏度特性的影响Figure8 Effect of NaCl on pasting behaviors of Xintianyuan potato starch
三边、新田源马铃薯淀粉的峰值黏度随NaCl浓度由0.5%增大至3.0%而逐渐升高,但所有值都比在蒸馏水中的低,谷值黏度和最终黏度也是如此(见图7、8),即NaCl会使马铃薯淀粉的黏度降低,这是由于NaCl溶液的离子强度大于蒸馏水的且NaCl的相对分子质量较水分子的大,其存在降低了体系的水分活度,影响了淀粉分子与水分子之间的相互作用[1]。不同NaCl浓度时,三边马铃薯淀粉的衰减值相差不大;新田源马铃薯淀粉的衰减值比在蒸馏水中的低。吕振磊等的研究结果[1]表明,随着NaCl浓度的逐渐增大,马铃薯淀粉的峰值黏度、谷值黏度、最终黏度、衰减值和回生值都显著降低,与本试验结果的差异可能是由于本试验所用的NaCl为分析纯,而该试验所用的NaCl为食品级,食品级试剂的纯度低于分析纯的;另外,两个试验所使用的马铃薯淀粉乳浓度也存在差异,对试验结果产生影响,因为淀粉乳浓度不同时,其黏度特性会有差别[1]。
玉米淀粉的峰值黏度、谷值黏度、最终黏度、衰减值和回生值随着NaCl浓度的逐渐增大变化不大(见图9),即NaCl的加入对玉米淀粉的黏度特性无明显影响。而谢新华等的研究[6]表明:随着NaCl浓度的增加,玉米淀粉的峰值黏度、衰减值、回生值和最终黏度都显著降低。与本试验结果有所区别,因为该试验所用淀粉为从特定品种(豫单2001)玉米提取。淀粉品种不同,其结构与性质存在差异[15],两个试验所使用的玉米淀粉乳浓度也存在差异。

图9 NaCl对玉米淀粉黏度特性的影响Figure9 Effect of NaCl on pasting behaviors of corn starch
三边、新田源马铃薯淀粉在NaCl溶液中的峰值黏度分别比在蒸馏水中的降低了23%~30%和50%~53%。在NaCl浓度为3%时,玉米淀粉的峰值黏度(463cP)比在蒸馏水中的(391cP)增加18%。不同浓度的NaCl溶液对马铃薯淀粉峰值黏度的影响比其对玉米淀粉的影响更显著,这是因为马铃薯淀粉的磷含量高于玉米淀粉的[16],因而其黏度性质更易受Na+影响。
随着NaCl浓度的增加,马铃薯淀粉、玉米淀粉的糊化温度都升高,这是由于NaCl中的Na+与淀粉中的羟基作用生成羟基钠,导致淀粉糊化过程的活化能升高而引起糊化温度升高[17]。Chiotelli等[17]研究表明:马铃薯淀粉的糊化温度随着NaCl浓度的增加而升高,当NaCl浓度增加至7%时糊化温度降低,本试验中NaCl的最高浓度为3%,未达到使糊化温度降低的浓度,与该研究结果一致。此外,在对扁豆淀粉[18]、荞麦 淀粉[19]、糜 子 淀 粉[20]的 相 关 研 究 中 也 有 相 似 的结论。
2.5 离子强度对马铃薯、玉米淀粉黏度特性的影响
在由0.01mol/L乙酸溶液和氢氧化钠溶液配制的缓冲液中,随着pH 值的增加,马铃薯淀粉的黏度变化不大,但都明显低于在蒸馏水中的。这是由于pH 缓冲液的离子强度显著高于蒸馏水的,说明与pH 值相比,离子强度对马铃薯淀粉黏度性质的影响更重要,因此在研究pH 值对马铃薯淀粉黏度性质影响时,应同时分析离子强度的影响。pH 为6.0~11.0的缓冲液离子强度相近,马铃薯淀粉的黏度变化不大,说明离子强度一定时,pH 值对马铃薯淀粉的黏度无明显影响。
蒸馏水、pH 7.0的缓冲液,以及0.5%的NaCl溶液,这3种不同体系的pH 值都在7左右,离子强度依次显著增加,马铃薯淀粉在三种体系中的峰值黏度依次显著降低;玉米淀粉在三种体系中的峰值黏度变化不大,即pH 一定时,随离子强度的增加,马铃薯淀粉黏度特性的变化较大。再次说明离子强度对马铃薯淀粉黏度性质的影响比pH 值对其的影响更重要,而且马铃薯淀粉比玉米淀粉对离子强度更敏感。
随着NaCl浓度由0.5%升高至3%,溶液的离子强度显著增加,但马铃薯淀粉的黏度变化幅度明显小于离子强度的变化幅度,这说明离子强度在一定范围内对马铃薯淀粉的黏度特性有显著影响,超出该范围后,影响就明显减弱。
3 结论
(1)马铃薯淀粉在蒸馏水和纯净水中的黏度接近,远远高于其在自来水中的黏度。玉米淀粉在三种水中的黏度差异不大。说明在黏度性质方面,水质对马铃薯淀粉比对玉米淀粉更重要。
(2)pH 值对马铃薯淀粉的黏度特性无明显的影响,而NaCl会降低马铃薯淀粉的黏度。pH 值和NaCl对玉米淀粉的黏度特性均无明显影响。随着NaCl浓度的增加,马铃薯淀粉和玉米淀粉的糊化温度都升高。离子强度对马铃薯淀粉黏度性质的影响比pH 值对其的影响更重要;马铃薯淀粉比玉米淀粉对离子强度更敏感。
(3)pH 一定时,随离子强度的增加,马铃薯淀粉黏度的变化较大;离子强度一定时,随pH 值增加,马铃薯淀粉的黏度无显著变化。离子强度在一定范围内对马铃薯淀粉的黏度特性有显著影响,即增加离子强度可降低马铃薯淀粉的黏度;超出该范围后,影响就明显减弱。因此,在研究pH 值对马铃薯淀粉黏度性质的影响时,应同时分析离子强度的影响。
1 吕振磊,李国强,陈海华.马铃薯淀粉糊化及凝胶特性研究[J].食品与机械,2010,26(3):22~27.
2 黄峻榕,许亚伦.淀粉黏度性质研究最新进展[J].食品与机械,2011,27(6):7~11.
3 Eliasson A C.Carbohydrate in food[M].Boca Raton:Taylor and Francis Ltd,2006:82~83,435~438.
4 Muhrbeck P,Eliasson A C.Influence of pH and ionic strength on the viscoelastic properties of starch gels-a comparison of potato and cassava starches[J].Carbohydrate Polymers,1987(7):291~300.
5 马冰洁,唐洪波,马玲.马铃薯淀粉糊的黏度性质[J].东北林业大学学报,2006,34(4):73~75.
6 谢新华,艾志录,王娜,等.不同介质对玉米淀粉糊化黏度特性的影响[J].中国粮油学报,2010,25(3):37~41.
7 Simonin H,Guyon C,de Lamballerie M,et al.Gelatinization kinetic of waxy starches under pressure according to ionic strength[J].High Pressure Research,2010,30(4):499~506.
8 赵清,舒为群,李国平,等.纯净水、净化水、凉开水、自来水的水质分析及其卫生学意义[J].重庆环境科学,2001,5(23):47~52.
9 李光磊,曾洁,孙科祥.不同食品成分对红薯淀粉糊黏度特性的影响[J].食品工业科技,2009,30(1):104~106.
10 于天峰,夏平.马铃薯淀粉特性及其利用研究[J].中国农学通报,2005,21(1):55~58.
11 赵凯.淀粉非化学改性技术[M].北京:化学工业出版社,2009:21~29.
12 Kaur A,Singh N,Ezekiel R,et al.Physicochemical,thermal and pasting properties of starches separated from different potato cultivars grown at different locations[J].Food Chemistry,2007,101(2):643~651.
13 Pérez E E,Breene W M,Bahnassey Y A.Variations in the gelatinization profiles of cassava,sagu and arrowroot native starches as measured with different thermal and mechanical methods[J].Starch-Strke,1998,50(2):70~72.
14 Suh D S,Jane J L.Comparison of starch pasting properties at various cooking conditions using the micro visco-amylo-graph and the rapid visco analyser[J].Cereal Chemistry,2003,80(6):745~749.
15 张攀峰.不同品种马铃薯淀粉结构与性质的研究[D].广州:华南理工大学,2012.
16 Singh J,Mccarthy O J,Singh H.Physicochemical and morphological characteristics of new zealand taewa(maori potato)starches[J].Carbohydrate Polymers,2006,64(4):569~581.
17 Chiotelli E,Pilosio G,Le Meste M.Effect of sodium chloride on the gelatinization of starch:a multimeasurement study[J].Biopolymers,2002,63:41~58.
18 杜双奎,于修烛,杨雯雯,等.扁豆淀粉理化特性分析[J].农业机械学报,2007,38(9):82~86.
19 李新华,韩晓芳,于娜.荞麦淀粉的性质比较[J].食品科学,2009,30(11):104~108.
20 谢新华,高向阳.食品添加剂对糜子淀粉糊化特性的影响[J].西北农林科技大学学报,2012,40(1):61~65.

