网膜囊路径腹腔镜胃后壁间质瘤切除8例报告
肖俊峰 暨 玲 蔡华杰 朱恒梁 郑晓风 蒋飞照
(温州医学院附属第一医院腔镜中心,温州 325000)
胃间质瘤(gastric stromal tumor,GST)是起源于胃肠道起搏细胞的一种独立的肿瘤,最终诊断有赖于病理学检查和免疫组织化学标记CD117及CD34[1],对化疗及放疗均不敏感,手术切除是最有效的治疗手段。腹腔镜下切除具有创伤小、恢复快等特点,但是对于腹腔镜下胃后壁GST手术路径的选择存在很大争议。2006年9月~2011年9月我院行腹腔镜下网膜囊路径手术切除8例胃后壁GST,现报道如下。
1 临床资料与方法
1.1 一般资料
本组8例,男6例,女2例。年龄30~74岁,平均52岁。3例以腹胀就诊,胃镜提示胃大弯黏膜下肿物;3例因上腹部痛就诊,胃镜提示胃小弯肿物;2例体检腹部CT提示胃壁肿物,术前腹部增强CT未发现转移。4例位于胃体后壁胃大弯,2例位于胃体后壁胃小弯,1例位于胃窦后壁,1例位于胃后壁靠近贲门。肿瘤最小2 cm×1.5 cm,最大8 cm×8 cm。
病例选择标准:一般情况能够耐受手术,无腹腔镜手术禁忌,>5 cm的GST并不是腹腔镜手术的禁忌证,只要做到术中无瘤原则即可[2];无远处转移;病人知情同意。
1.2 方法
全身麻醉。头高足低仰卧位,分腿位。术者站于患者左侧,助手站于患者右侧,扶镜手位于两腿中间。气腹压力设定为12~14 mm Hg。常规于脐部置入10 mm trocar作为观察孔,左右锁骨中线平脐上2 cm分别置入5、12 mm trocar作为牵引孔,左侧腋前线肋缘下2 cm置入10 mm trocar为主操作孔,右腋前线肋缘下2 cm置入5 mm trocar用于牵引、暴露肝脏。切除方法根据肿瘤位置而定。①胃体后壁靠近胃大弯的肿瘤:充分游离胃底,打开胃结肠韧带,充分离断肝胃韧带,将胃向右上方翻转,提起肿瘤后用线形切割吻合器(Endo-GIA)在距肿瘤边缘2 cm处将肿瘤完整切除,靠近胃窦及贲门的GST手术切缘保证R0即可[3]。切除肿瘤用标本袋从右锁骨中线处troar取出;对于较大的肿瘤,可在标本袋中剪碎取出,如不行可适当延长切口,但要谨防术中标本袋的破裂。②胃体后壁靠近胃小弯的肿瘤:离断部分肝胃韧带,将胃向后向下翻转,然后使用线形切割吻合器(Endo-GIA)在距肿瘤边缘2 cm处将肿瘤完整切除。③胃窦或贲门处肿瘤:局部切除可引起术后胃入口及出口狭窄,分别行腹腔镜下远端或近端胃大部切除术[4]。
2 结果
6例均成功行腹腔镜下网膜囊路径局部楔形切除术,1例行近端胃大部分切除+胃-食管吻合,1例行远端胃大部分切除+毕Ⅰ式吻合。手术时间30~90 min,平均60 min;术中出血量20~80 ml,平均50 ml。术后2~6 d,平均4 d进食流质。住院时间3~7 d,平均5 d。术后病理:全部为GST,5例低度恶性,2例中度恶性,1例高度恶性;8例CD117全部为阳性;胃周淋巴清均未见转移,切缘均阴性。3例中~高度恶性给予伊马替尼1年的治疗。8例随访3~62个月,平均32.5月,无复发、吻合口狭窄,见表1。
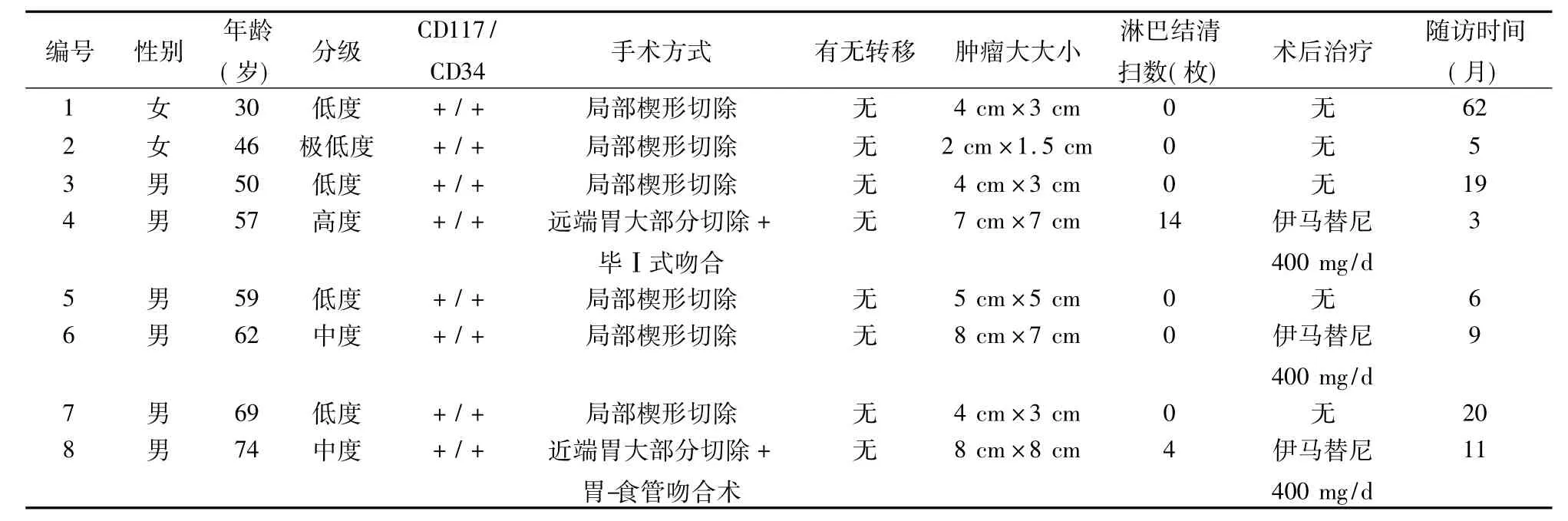
表1 8例GST手术前后情况
3 讨论
近年来,腹腔镜下行GST楔形切除广泛开展,胃后壁GST由于其特殊位置,往往腔镜下暴露较困难。李际辉等[5]提出切开胃前壁,挤出肿块,行肿块切除,这样方便腹腔镜下操作,简化步骤,但是这种方法会不会导致肿瘤播散,污染腹腔,目前存在很大争议。因此,有必要对于胃后壁GST的腹腔镜手术路径进行研究,并制定相关标准。
腹腔镜下网膜囊路径切除是根据肿瘤的位置离断相应胃的韧带(肝胃韧带、胃结肠韧带、胃脾韧带、胃膈韧带、胃胰韧带),充分显露胃后壁,把肿瘤暴露在视野中,行肿瘤局部切除,切缘至少距肿瘤3 cm,对于距贲门或胃窦较近且较大的肿瘤,也应显露胃后壁,暴露肿瘤在视野中。虽然这些位置的肿瘤需要行近端或远端胃大部分切除,不需要考虑是切开胃前壁挤出肿瘤切除,还是网膜囊路径切除,但是这些位置可能向后侵犯邻近组织,有必要充分显露胃后壁,了解是否侵犯邻近组织,减少切除的不彻底。腹腔镜网膜囊路径切除对于减少术中肿瘤播散有重要的作用,本组6例均游离胃后壁,充分暴露胃后壁,行胃后壁间质瘤切除术,1例行近端胃大部分切除+胃-食管吻合,1例行远端胃大部分切除+毕Ⅰ式吻合,术后随访3~62个月均无复发。
切开胃前壁,提拉出肿瘤,行胃后壁GST切除的争议主要在以下几点:①GST本身组织较脆,包膜较薄,挤压易导致肿瘤破裂及播散,而肿瘤播散也被认为是恶性程度分级的独立因素,最终会引起肿瘤复发,导致生存率下降[6]。②当肿瘤>5 cm时,会造成抓持或钳夹困难,导致增加钳夹的力量,进而会引起肿瘤破裂和腹腔内种植的风险[7]。③GST早期往往没有临床表现,发现时往往肿瘤已较大,有的已向胰腺及脾脏侵犯,如果单纯挤出切除,极有可能漏掉向周围组织侵犯的肿瘤组织[8]。④腹腔镜下切开和缝合胃壁,手术创伤和技术难度增加,不仅会延长手术时间,并且存在引起肿瘤播散和腹腔污染的潜在危险,还存在胃液污染腹腔的可能[9]。⑤由于腹腔镜手术缺乏手的“触觉反馈”,对术者要求较高,应当有熟练的并且对GST的特征有深入了解的外科医师来完成腹腔镜下GST切除术,否则有可能导致肿瘤播散污染腹腔,而对于切开胃前壁,提拉切除胃后壁GST的技术要求更高,增加污染腹腔的概率[10]。⑥根据我们的经验,对于呈哑铃状生长的胃后壁GST,只切除突入胃腔的肿瘤,可能还有部分残留在肌层,导致切除不完整,甚至广泛转移。从网膜囊路径行GST切除能防止术中因肿瘤挤压、提拉导致的肿瘤术中播散,继而污染腹腔,最终导致肿瘤复发,影响生存率,故对于胃后壁GST应离断相关胃的韧带,充分显露肿瘤,行肿瘤完整切除,对减少肿瘤复发以及提高生存率有重要意义。本组全部充分显露胃后壁,行肿瘤完整切除。如果距离胃窦或贲门很近,为避免术后胃入口或出口狭窄,须行近端或远端胃大部切除术。如果距离较近且肿瘤较大,根据肿瘤根治原则,为保证3 cm的切缘距离,必须行胃大部切除术,如果肿瘤侵及邻近脏器,可行多器官的整块切除。
对于胃后壁GST,为减少医源性肿瘤播散、污染腹腔,应当充分暴露胃后壁,进行胃大弯和胃小弯侧的充分游离后,依靠术前美蓝定位,一般术前4 h在胃镜室病灶处注射美蓝。美蓝量不要太多,距手术时间不要超过4 h,否则会造成美蓝弥散而不能精确定位,术中根据美蓝显示的位置行手术切除,对于美蓝定位差的可行术中胃镜定位。术中及术后遵循以下几点,对减少术中肿瘤播散、减少复发以及改善预后有重要意义:①手术操作轻柔,严格避免直接抓持肿瘤,如需抓持,可选择周边健康胃壁组织;②包括肿瘤包膜在内完整切除;③保证切缘阴性;④标本存放及取出过程无污染,用标本袋存放及取出标本,术毕冲洗腹腔及戳孔,避免切口污染及腹腔种植[11];⑤术后根据病理分级给予伊马替尼辅助治疗并定期复查全腹部CT。
手术完整切除肿瘤可达到根治的目的,但对于中~高度恶性的患者,术后仍有复发可能,故对于KIT基因阳性的患者应每天400 mg伊马替尼,疗程1年。本组3例均是KIT基因阳性,术后给予辅助治疗,按2008年Joensuu提出的分级标准:不能完整切除或有转移的KIT基因阳性患者,一线治疗应当是每天400 mg伊马替尼,外显子9突变的每天800 mg。手术虽然已经完整切除,但术后的复查仍是必须的,每3个月一次腹部CT作为治疗后的评估,对于中~高度恶性的病人前3年每4个月一次腹部CT,第4~5年每6个月一次,第6年开始每年一次。低度复发的病人每6个月一次已经足够,对于极低复发的病人,没有要求常规CT复查[12]。本组8例按以上要求复查全腹部CT,均未见复发。
1 Fletcher CD,Berman JJ,Corless C,et al. Diagnosis of gastrointestinal stromal tumors:a consensus approach.Human Pathology,2002,5(33):459-465.
2 王 港,付 卫,王德臣,等.腹腔镜与开腹胃问质瘤楔形切除的临床对比研究.中国微创外科杂志,2010,10(2):126-129.
3 中国CSCO胃肠间质瘤专家委员会.中国胃肠间质瘤诊断治疗专家共识(2011 版).中华胃肠外科杂志,2012,15(3):301-305.
4 El-Hanafy E,El-Hemaly M,Hamdy E,et al.Surgical management of gastric gastrointestinal stromal tumor:a single center experience.Saudi JGastroenterol,2011,17(3):189-193.
5 李际辉,方国恩,郑成竹,等.胃间质瘤的腹腔镜手术.中华胃肠外科志,2003,6(4):274.
6 Joensuu H.Risk stratification of patients diagnosed with gastrointestinal stromal tumor.Hum Pathol,2008,39(10):1411-1419.
7 徐雪良.胃间质瘤的腹腔镜切除术.中华普外科杂志,2010,25(1):66.
8 师英强,杜春燕,周 烨,等.胃肠间质瘤联合脏器切除22例疗效分析.中国实用外科杂志,2008,28(4):274.
9 Fernández JA,Sánchez-Cánovas ME,Parrilla P.Controversies in the surgical treatment of primary gastrointestinal stromal tumours(GIST).Cir Esp,2010,88(2):69-80.
10 Kakeji Y,Nakanoko T,Yoshida R,et al.Laparoscopic resection for gastrointestinal stromal tumors in the stomach.Surg Today,2011,11:11-15.
11 Palanivelu C,Rangarajan M,Parthasarathi R,et al.Laparoscopic resection for benign tumors of the stomach.JSLS,2007,11(1):81-86.
12 Ploner F,Zacherl J,Wrba F,et al.Gastrointestinal stromal tumors:recommendations on diagnosis,therapy and follow-up care in Austria.Wien Klin Wochenschr,2009,121:780-790.

