何首乌致肝损伤病例分析
谢先吉,马葵芬,刘莹
浙江大学医学院附属第一医院药剂科 浙江 杭州 310003
随着人们保健意识的增强,口服补益类中药越来越广泛。何首乌为蓼科植物首乌(Polygonum multiflorum Thunb)的干燥块根。其主要含二苯乙烯苷类、磷脂类、蒽醌类成分。由于具有补肝肾、益精血、乌发、强精骨的功效,并兼有药食同源的应用基础,所以在民间以粉末或成药及煎剂配伍其他中药形式被广泛使用。但近几年来何首乌致药物性肝损伤(DILI)的不良反应逐渐增多,所以有必要引起重视予以研究。我们采集了本院2008年3月~2012年3月的药物性肝损伤的165病例,从中发现了10例明确由何首乌所致的药物性肝损伤,对其病因、肝功能指标、影像资料、治疗方案、预后和转归进行分析。
1 资料和方法
1.1 一般资料 采集2008年3月~2012年3月药物性肝损伤病例165例,由中药引起的64例,占38.8%,明确由何首乌及制剂引起的药物性肝损伤10例,排除甲乙丙丁戊型病毒性肝炎、酒精性肝病、免疫性肝损伤等及其他传染病和资料不完整者。其中男7例,女3例,年龄46.1±10.2;平均住院日21.7±10.7;根据Maria诊断标准[1]计分:>17分 2 例; 14~17 分 6例 ;10~13分2例。根据世界卫生组织所属国际医学科学组织委员会(CIOMS)推荐的DILI的分型标准:丙氨酸氨基转移酶(ALT)上升至正常上限2倍以上,或ALT/ALP(碱性磷酸酶)5,为肝细胞型;ALT/ALP2为肝内淤胆型;ALT和ALP均升高2倍,ALT/ALP在2~5,为混合型[1]。
本组10例A L T均上升至正常上限2倍以上,其中1例ALT/ALP2。总胆红素(TB)、直接胆红素(DB)、总胆汁酸(TBA)、r-谷酰基转移酶(r-GT)均升高。
1.2 方法 应用回顾性的研究方法,记录患者的年龄、性别、基础疾病、用药时间及用药史、临床表现、肝功能、影像检查结果、治疗方案、预后与转归。
2 结果
10例均为服用何首乌,其中服用何首乌粉2例;药酒2例;养血生发胶囊2例,服用时间为10d及30d,用量未记载;服用原药2例,其中网购何首乌及鹿鞭膏1例,其余2例为何首乌煎剂,服用时间为30~105d。有1例为停药后肝损好转再用药再次激发肝损。
2.1 临床表现 临床症状为乏力6例、纳差4例、尿黄7例、厌油2例、发热3例,腹部胀痛1例、剑突下疼痛并伴随呃逆1例、皮肤瘙痒2例、大便发灰陶土色1例、盗汗1例、皮肤黄染3例、巩膜黄染8例。10例均无皮疹、瘀斑、腹水、肝掌等体征。
2.2 肝功能及其他生化指标 10例均嗜酸性粒细胞未增多,白细胞未减少,抗核抗体(ANA)阴性,说明这10例肝脏损害不是超敏反应[1]。红细胞平均容积均增加(MCV),凝血时间、C反应蛋白、α-岩藻糖苷酶均有不同程度的增高。有尿胆红素报告的病例都有3或4个“﹢”。
2.3 影像学资料 B超显示大部分病例出现胆囊壁毛糙,肝脾肿大1例、胆囊水肿2例,但未出现门静脉增宽现象[2]。由于我院收治的患者多为当地医院治疗效果不好转院而来的,所以未出现早期肝损症状。螺旋CT报告显示肺部感染伴颅内出血1例。
2.4 治疗方案 一般采取护肝降酶,利胆退黄、抗炎等对症治疗。使用腺苷蛋氨酸、甘草酸铵N-乙酰半胱氨酸(阿斯欣泰)、多烯磷脂酰胆碱、水飞蓟素、还原型谷胱甘肽等药物,用甲泼尼龙抗炎。有些还使用小分子肝素钙改善肝脏微循环,有一例出现亚急性肝衰竭采用人工肝(ALSS)技术进行置换,ALSS对危重的肝衰竭有较好的疗效。
2.5 预后及转归 除1例出现肝性脑病自动出院,其余9例均有不同程度好转。见表1。
2.6 肝损伤类型及转归与服用时间、剂量及方式的相关性 见表2 。

表 1 何首乌致肝损伤病例治疗前后肝功能指标的比较Tab 1 Comparison of liver function before and after treatment on cases of drug-induced liver injury
3 讨论
3.1 何首乌中主要成分 为游离及结合态蒽醌类,如大黄素、大黄酸,这些成分是引起肝肾毒性的主要物质基础,在高浓度、长时间的作用下对肝细胞产生毒性,游离蒽醌类的毒性顺序为:芦荟大黄素>大黄素甲醚>大黄素>大黄酚;结合态的蒽醌的毒性顺序为结合芦荟大黄素>结合大黄素甲醚>结合大黄酚>结合大黄素>结合大黄酸[3]。有研究证明何首乌脂溶性成分是引起肝细胞损伤的主要物质,大黄素是其中一个成分,它对肝细胞存在双相作用,即低剂量促进生长,高剂量抑制其生长的特性[4],临床上DILI的患者当超剂量短时间与低剂量长时间服用都使体内大黄素浓度达到阈值即会引起肝损。一般生首乌的毒性大于制首乌,用何首乌浸酒的肝损伤发病时间早于粉末早于煎剂,从表2可以初步推断何首乌所致的药物性肝损伤具有一定剂量及时间依赖性的可能[5]。
3.2 何首乌致DILI可能的机制 蒽醌类可能具有类肾上腺皮质激素样作用,对肝脏有一定毒性;蒽醌类、蒽酚衍生物在结肠形成高活性的蒽酮,吸收后引起肝损伤;何首乌具有免疫调节作用,可能导致免疫介导的肝损伤或特异质反应;何首乌在代谢过程中产生的代谢产物引起肝细胞的过氧化、干扰肝细胞摄取和胆汁的分泌及肝内转运,导致胆汁淤积和胆管的损伤,表现胆道功能的缺失;与肝代谢酶缺陷或功能障碍有关系,所以本课题组将进一步研究这些病例的P450的基因多态性,以了解何首乌致肝损伤的个体差异。
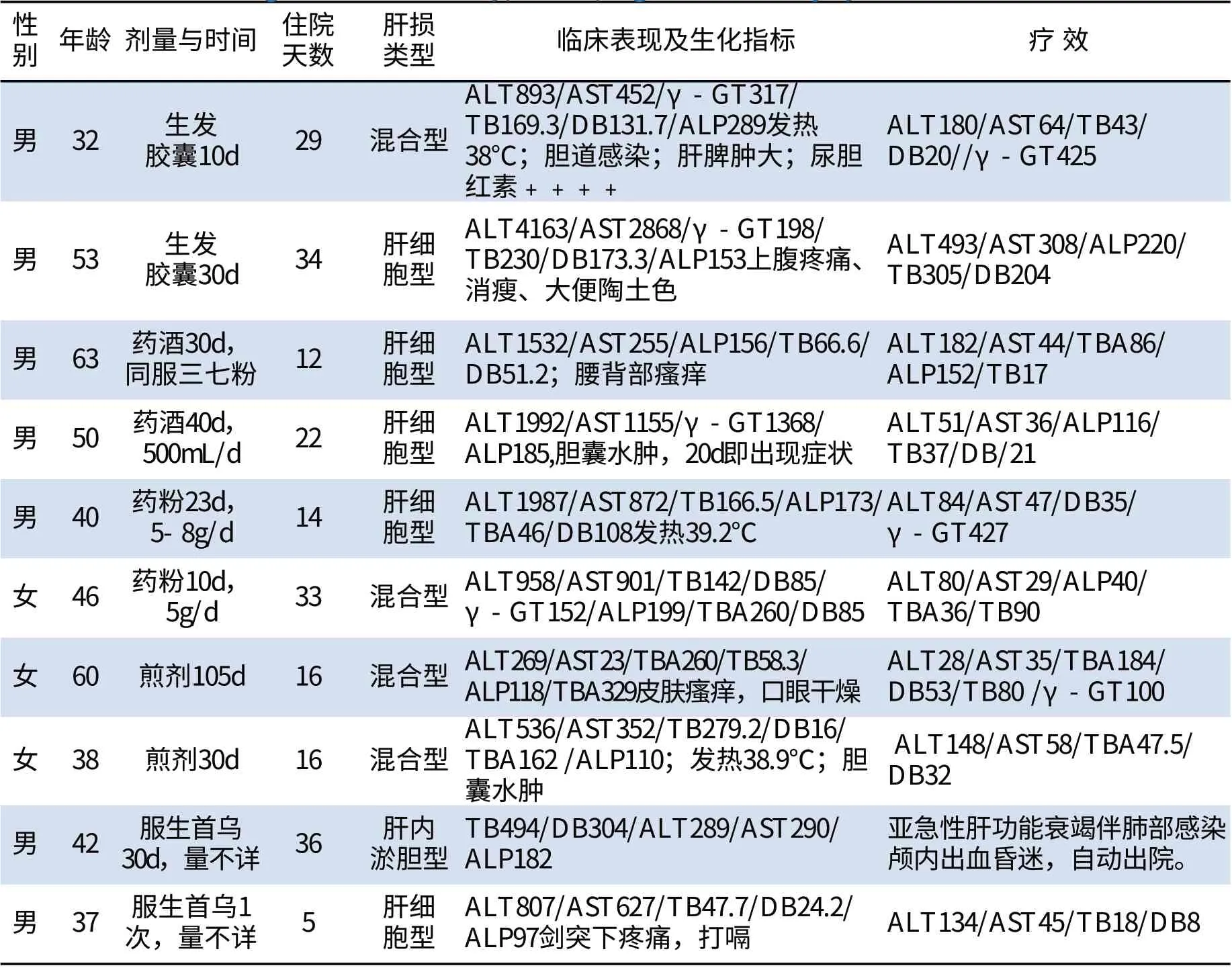
表 2 摄取何首乌的剂量与方式对肝损伤类型及转归的影响Tab 2 Influence of dosage and methods on types and prognosis of liver injury
3.3 肝损伤出现时间 大部分病例在用药后3~90d内出现症状,最早3d。以肝细胞损伤型居多,混合型其次,肝内淤胆型最少。发热、瘙痒等DILI的肝外表现有5例[6]。
3.4 何首乌制剂 含何首乌的市售成方制剂有生发胶囊、七宝美髯丸、肾宝合剂、康尔心胶囊、安神胶囊、泽泻首乌胶囊、当归芦荟胶囊等,在说明书中应予以提醒。临床医师和药师也要提高对此类制剂可能致肝损伤的警惕。
[1] Danan G,Benichou C.Causality assessment of adverse reactions to drugs-L .A novel method on the conclusion of international of the consensus meetings: application to drug-induced liver injuries[J].Clin Epidemiol,1993,46:1323-1330.
[2] 唐岸柳,沈守荣,贺达仁.药物性肝损伤的诊断思维[J].医学与哲学(临床决策论坛版),2009,vol30,No11 63-65
[3] 俞捷,谢洁,赵荣华,等.何首乌肝脏不良反应研究进展[J].中草药2010.7 Vol41 No7:1206-1210
[4] 张瑞晨,刘斌,孙震晓,徐冬艳.何首乌提取物对人正常肝细胞L02周期阻滞及凋亡的影响[J]. 中西医结合学报2010.6.Vol8.No6:554-561
[5] 孙向红 ,孙玉维,李红,等.何首乌主要成分大黄素、大黄酸和二苯乙烯苷类对肝细胞、肝癌细胞的影响[J].现代中西医结合杂志 2010 APR.19(11)1315-1319
[6] Norris W,Paredes AH, Lewis JH. Drug-induced liver injury in 2007[J].Curr Opin Gastroenterol,2008 May;24(3):287-97

