高效液相色谱法测定连朴饮不同煎液中栀子苷的含量Δ
冯华,聂明华,邹孔强,王祥培,罗秀琼(.遵义市食品药品检验所,贵州遵义56300;.贵阳中医学院,贵阳55000)
高效液相色谱法测定连朴饮不同煎液中栀子苷的含量Δ
冯华1*,聂明华1,邹孔强1,王祥培2,罗秀琼1(1.遵义市食品药品检验所,贵州遵义563002;2.贵阳中医学院,贵阳550002)
目的:考察用合煎液(传统汤剂)、分煎液(配方颗粒汤剂)方法制备的连朴饮汤剂中栀子苷含量的变化。方法:建立高效液相色谱(HPLC)法,采用Diamonisl C18柱(200 mm×4.6 mm,5 μm);流动相为乙睛∶水(20∶80);流速为1 mL·min-1;检测波长为238 nm。结果:连朴饮分煎液中栀子苷平均含量比合煎液中栀子苷平均含量高。结论:与传统汤剂比较,连朴饮配方颗粒汤剂中栀子苷的含量高。
连朴饮;栀子苷;合煎;分煎;高效液相色谱法
连朴饮出自《霍乱论》,处方由制厚朴、川连、石菖蒲、焦栀子等组成,具有清热化湿、理气和中等功效。本文以有效成分栀子苷作为指标,比较该方2种煎液中栀子苷含量差异,探索中药复方汤剂不同制法对其有效成分溶出量的影响,对单味中药配方颗粒应用于临床打下一定基础。
1 仪器与试药
Waters 1525型高效液相色谱仪,KQ-300DE超声仪,色谱柱:Diamonsil C18(5 μm,200 mm×4.6 mm)。厚朴、川连、石菖蒲、制半夏、香豉、焦栀子、芦根7味药材饮片由遵义医药有限公司提供,经遵义市药品检验所鉴定均符合《中华人民共和国药典:一部》(2010年版)收载品种。栀子苷对照品(中国药品生物制品检定所提供,批号:110749-200572),甲醇为色谱纯,水为娃哈哈纯净水。
2 方法与结果
2.1 色谱条件
流动相:乙睛∶水(20∶80);流速为1 mL·min-1;检测波长为238 nm;柱温为25℃[1];进样量为10 μL。色谱图见图1 。
2.2 溶液的制备
2.2.1 对照品溶液的制备:精密称取栀子苷对照品适量,加甲醇溶解制成每1 mL含0.085 mg的溶液,即得。
2.2.2 合煎液的制备:称取药材制厚朴6 g、川连3 g、石菖蒲3 g、制半夏3 g、香豉9 g、焦栀子9 g、芦根60 g,加8倍量的水煎煮,保持微沸30 min,倒出煎液;药渣再加8倍量的水煎煮30 min,合并2次煎液,减压干燥成干粉。称取相当于原药材处方量的干粉,置100 mL量瓶中,用开水溶解定溶至刻度,精密吸取2 mL,置50 mL容量瓶中,加甲醇至刻度,称重,超声处理(功率为250 W,频率为20 kHz)25 min,取出,放冷,加甲醇补足重量,摇匀,取续滤液,即得。
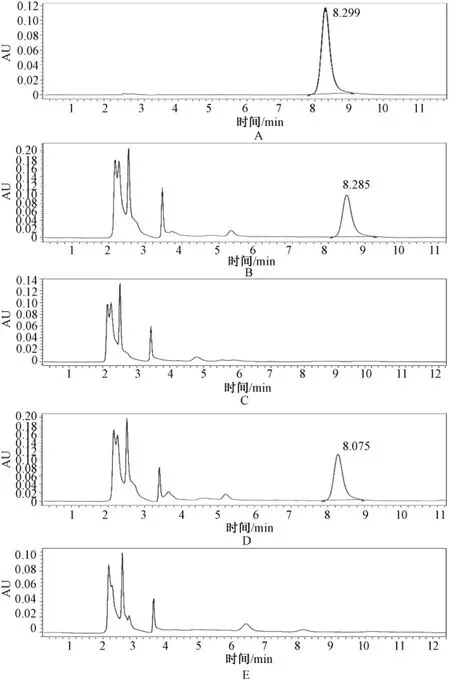
图1 HPLC色谱图Fig 1HPLC chromatgrams
2.2.3 分煎液的制备:称取上述处方量的药材分别加8倍量的水煎煮2次,每次保持微沸30 min,制备各药材的煎液,减压干燥成干粉。干粉混合均匀,同法制得分煎液溶液。
2.2.4 阴性溶液的制备:称取不含栀子的药材,同法制备成阴性溶液。
2.3 线性关系考察
标准曲线的绘制:精密称取栀子苷对照品,配制成0.065 88、0.076 86、0.087 84、0.098 82、0.109 80 mg·mL-1的栀子苷对照品溶液,精密吸取对照品溶液10 μL,按上述色谱条件依次测定,得回归方程:Y=1.9×106X+88 530,r=0.999 5,栀子苷在65.88~109.80 μg·mL-1间线性关系良好。
2.4 精密度试验
重复进样6次,平均峰面积分别为1 813885、2 153 595;RSD分别为0.6%、0.8%,表明精密度良好。
2.5 稳定性试验
在0、4、8、16、24 h分别测定其峰面积,合煎液的RSD=1.0%、分煎液的RSD=1.2%,表明2种煎液在24 h内稳定。
2.6 重复性试验
分别取同一样品各5份,测定含量,结果合煎液和分煎液栀子苷平均含量分别为114.21、133.08 mg,RSD分别为0.9%、1.0%,表明重复性好。
2.7 回收率试验
按分煎液、合煎液制备项下制备各5份,稀释50倍进行加样回收,精密加入栀子苷对照品(1.250 mg·mL-1)1 mL,进行加样回收试验,过0.45 μm滤膜,并按色谱条件项下进样,同法测定,结果见表1 、2(mg/m代表1 个样品稀释50倍后含栀子苷量的毫克数)。
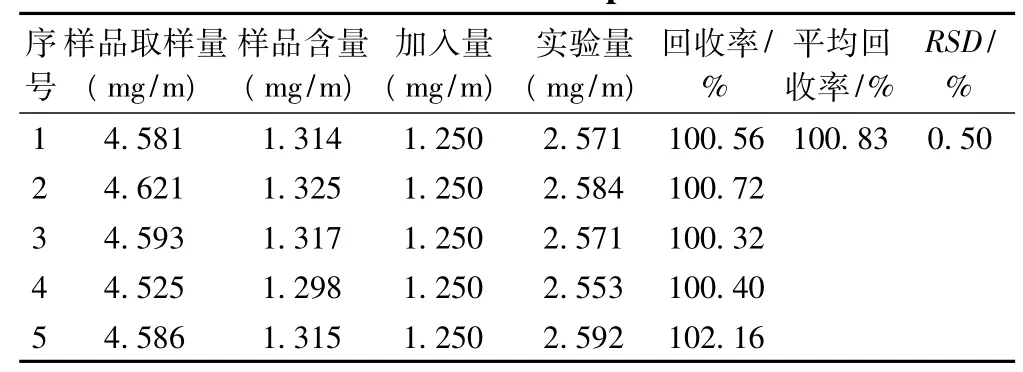
表1 分煎汤剂栀子苷加样回收测定结果Tab 1Results of recovery test of geniposide in separated decoction sample

表2 合煎汤剂栀子苷加样回收率测定结果Tab 2Results of recovery test of geniposide in mixed decoction sample
2.8 样品含量测定
各制备5份,测定栀子苷含量,求平均含量。合煎液平均含量为114.98 mg,分煎液平均含量为130.41 mg。结果显示,连朴饮分煎液比合煎液中栀子苷的含量高。
3 讨论
本研究采用HPLC法测定中药复方制剂中的栀子苷含量,文献报道可用多种不同组成的流动相系统[2,4],本实验选择《中华是否是一个比较普遍现象,还有待广泛的研究才能确定。本实验测定连朴饮中有效成分栀子苷在分煎、合煎过程中含量有无变化,为连朴饮配方颗粒应用于临床提供一些理论依据。
[1]国家药典委员会.中华人民共和国药典:一部[S].2010年版.北京:中国医药科技出版社,2010:231-232.
[2]吴红娟,王清波,谭朝阳,等.不同来源栀子中栀子苷含量测定[J].湖南中医药大学学报,2010,30(5):35-37.
[3]段启,庄义修,陈华师.HPLC法测定不同产地栀子中栀子苷含量[J].亚太传统医药,2009,5(6):20-21.
[4]刘瑛,张浩.栀子药材中栀子苷的含量测定[J].华西药学杂志,2003,18(5):374-375.
Determination of Geniposide in Mixed vs.Separated Decoctions of Lian Pu Drink by HPLCΔ
FENG Hua1*,NIE Ming-hua1,ZOU Kong-qiang1,WANG Xiang-pei2,LUO Xiu-qiong1(Zunyi Institute for Food&Drug Control,Guizhou Zunyi 563002,China;2.Guiyang College of Traditional Chinese Medicine,Guiyang 550002,China)
OBJECTIVE:To investigate the content change of geniposide in of Lian Pu Drink prepared by mixed decoction(traditional decoction)method or separated decoction(decoction of dispensing granules)method.METHODS:The content of geniposide was determined by HPLC using Diamonisl C18column(5 μm,4.6 mm×200 mm)with a mobile phase of CH3CN∶water(20∶80)at a flow rate of 1 mL·min-1and a detection wavelength of 238 nm.RESULTS:The mean content of geniposide in separated decoction of Lian Pu Drink was higher than in its mixed decoction.CONCLUSION:The content of geniposide in decoction of dispensing granules of Lian Pu Drink was higher than in its traditional decoction.
Lian Pu Drink;Geniposide;Mixed decoction;Separated decoction;HPLC;
R932
B
1672-2124(2012)09-0809-03
遵义市中药现代化科技产业研究开发专项项目课题(市科合中药专字[2009]4号)
*主管药师。研究方向:新药研究、药品检验。E-mail:fenghua781014@yahoo.com.cn
2011-12-09
2012-02-16)
*副主任药师。研究方向:临床药学、医院制剂研发。E-mail:jgyylgb@sina.com
——贵州省遵义市绥阳县老年大学校歌
——遵义市春节联欢晚会

