SO3体系中碘催化甲烷的选择性氧化反应
李明华,洪 林,陈立宇
(1.西北大学化工学院, 陕西 西安 710069; 2.第四军医大学化学教研室, 陕西 西安 710032)
SO3体系中碘催化甲烷的选择性氧化反应
李明华1,2,洪 林1,陈立宇1
(1.西北大学化工学院, 陕西 西安 710069; 2.第四军医大学化学教研室, 陕西 西安 710032)
在SO3体系中,采用碘系列化合物作为催化剂进行甲烷部分氧化反应的研究。对催化剂进行筛选,考察反应工艺条件的影响,并对反应机理进行探讨。最终确定I2为最佳催化剂,反应的最优工艺条件为:催化剂0.099 mol·L−1,温度T=433 K,初始压力P=4.0 MPa,搅拌速度500 r/min。该工艺条件下甲烷转化率可达63.57%,目的产物收率为52.6 %,产物选择性82.74%。
甲烷;部分氧化;碘催化;SO3体系
甲烷液相部分氧化反应是近几十年发展起来的研究领域,目的在于将甲烷转化成为易于运输的甲醇。前苏联科学家在20世纪60年代开创了甲烷液相部分氧化制甲醇的研究工作,研究主要集中在强酸溶液中催化剂的开发,主要的催化剂为Pt、Pd过渡金属及稀土金属。近些年来,Xiao Gang、Periana、Michalkiewicz 、陈立宇等研究者提出在发烟硫酸体系中甲烷液相部分氧化制甲醇的工艺,并对催化机理进行讨论[1-8]。
之前的研究都证明,贵金属及碘系列催化剂在强酸体系中均对甲烷部分氧化有较好的催化效果。而在发烟硫酸体系中,SO3是发烟硫酸中主要的氧化剂,其浓度直接影响甲烷的转化率[9]。本实验利用 SO3来充当甲烷部分氧化的溶剂和氧化剂,碘溶解于SO3中作为催化剂,直接合成硫酸单甲酯。水解后可以得到甲醇,并可以避免应用发烟硫酸过程中而产生过多稀酸,为甲烷液相部分氧化工作开辟一个新的思路。
1 实验部分
1.1 实验仪器
250 mL不锈钢高压反应釜(大连通产高压设备有限公司),电磁搅拌,电加热炉加热。反应采用热电偶采集反应温度,霍尔组件采集搅拌转速,PID控制器显示并调控反应温度和搅拌转速,反应釜上的压力传感器将压力送至压力表并在计算机上记录。
1.2 实验流程
在高压反应釜中加入一定量的催化剂和 SO3,封釜。用一定比例的CH4-Ar(Ar作为标定气体)混合气置换釜内空气,加压至需要压力,升温至所需温度后开始搅拌,反应3 h后停止,冷却至室温,取气相样品用气相色谱分析。气相产物分析后打开针形排气阀,反应釜压力降至常压,打开反应釜,取液相产物用核磁共振进行分析,将剩余液体转移至三口烧瓶进行水解并取样分析。
2 结果与讨论
2.1 碘系列催化剂的筛选
在发烟硫酸中,碘对甲烷部分氧化的催化性能较好[10],因此,实验首先挑选了几种常用的碘系列催化剂进行筛选,结果如表1所示。
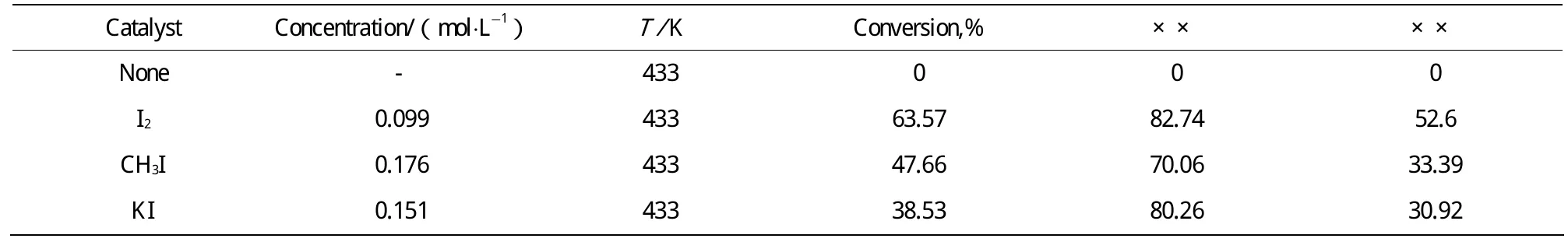
表1 碘化合物系列催化剂对甲烷部分氧化反应的影响Table 1 the impact of the iodine compound catalysts for partial oxidation of methane reaction
由表1看出,同在发烟硫酸中相似,碘系列催化剂均可对甲烷选择性氧化反应起作用。碘化合物溶解在SO3中,可能形成I+或I2+作为亲电试剂进攻甲烷,发生亲电取代反应[10]。在考察的碘系列化合物中,碘单质的催化效果最好。
由图1和图2看出,甲烷的转化率随着催化剂加入量的增大而不断升高,当催化剂用量增加至0.75 g时,继续增加用量,转化率趋于平缓,同时,目的产物的选择性随着催化剂用量的增加而不断降低,这是因为在反应中产生了 CO2,阻碍了反应的进一步转化。综合考虑转化率和选择性,最终选择催化剂用量为1 g。
2.2 碘催化剂加入量的考察
催化剂浓度是影响甲烷催化反应的重要因素,实验采用I2作为催化剂,考察不同催化剂浓度对反应的影响。结果如图1和2所示。
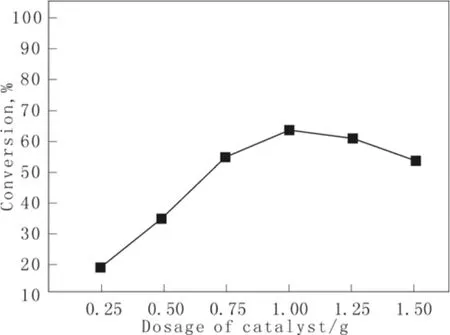
图1 催化剂加入量对甲烷转化的影响Fig.1 The impact of catalyst addition on
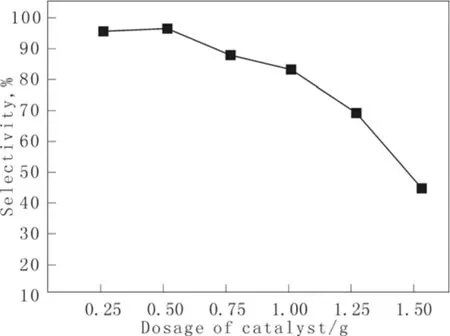
图2 催化剂加入量对产物选择性的影响Fig.2 The impact of catalyst addition on product methane conversion selectivity
2.3 初始压力对反应的影响
反应压力是甲烷转化的另一个重要影响因素,实验考察了初始压力对反应的影响。结果如表2所示。
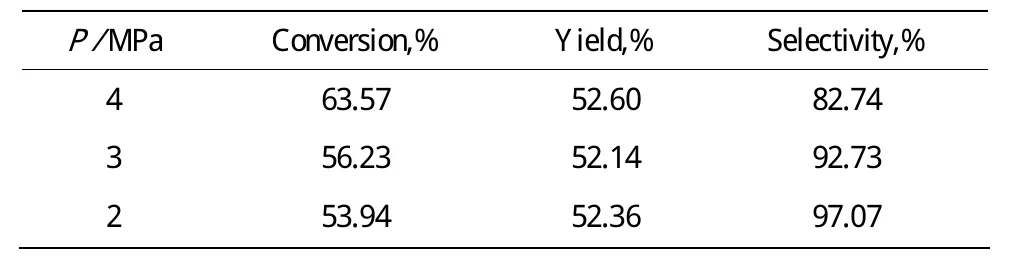
表2 不同初始压力对甲烷转化的影响Table 2 the impact of different initial pressure on methane conversion
由表2看出,甲烷反应转化率随着初始压力的增加而增大,产物选择性则相反,总体收率来说初始压力的影响不是很大。原因可能是由于甲烷初始压力高,使得它在气相中的分压大,促进甲烷通过气相主体扩散到气液界面,在界面和液相主体中,甲烷的相对含量增加,从而使得转化率有所提高。同时,甲烷被SO3深度氧化为CO2的副反应速率也增大。考虑到较高的压力更加容易使甲烷活化,选择初始压力P=4 MPa。
2.4 温度对反应的影响
温度也是影响反应的重要因素,实验考察了温度对反应的影响,如表3所示。

表3 反应温度对转化率、目的产物收率及选择性的影响Table 3 The impact of different reaction temperatures on conversion, yield and selectivity
由表3看出,甲烷转化率在140 ℃时很低,当温度升高到160~200 ℃时,转化率大幅度提高,同时产生的CO2量也迅速增大,产物选择性降低。为了保证转化率的同时避免甲烷被过度氧化成为CO2,温度应选择在160~180 ℃之间。
2.5 搅拌速率对甲烷部分氧化反应的影响
本实验还进行了搅拌速率对甲烷部分氧化反应的考察,如图3和4所示。
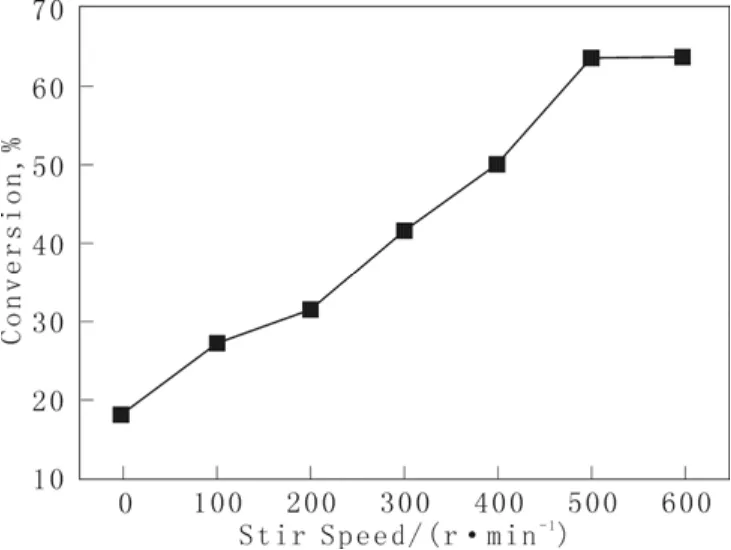
图3 搅拌速率对甲烷转化率的影响Fig.3 the impact of stirring rate on methane Conversion
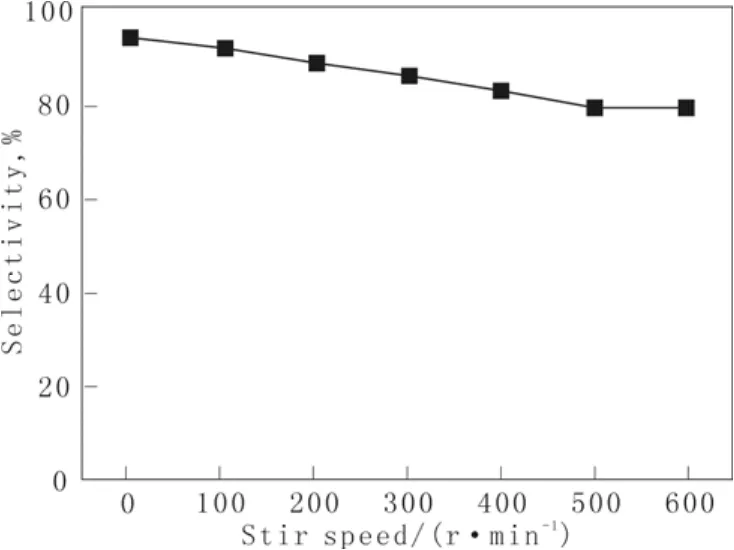
图4 搅拌速率对产物选择性的影响Fig.4 the impact of stirring rate on product selectivity
由图3和图4看出,搅拌速率在0到500范围内,搅拌速率增加,甲烷转化率也随之增加,同时,副反应产物CO2增加,因此选择性有所降低。当搅拌速度达到500后,甲烷转化率和目的产物的选择性随着搅拌速率的增加趋于平缓,这是由于搅拌速率增加引起釜内气液相界面积增大,当搅拌速率达到一定程度时,气液相界面积不再随其增加而增大。同时,搅拌速率增加可以促进液相产物扩散,维持浓度梯度。最终确定甲烷的部分氧化反应搅拌速率为500 r/min。
2.6 碘催化机理探讨
实验中还进行了SO3体系中碘催化剂催化机理的探索,将反应产物进行核磁共振分析,如图5所示。
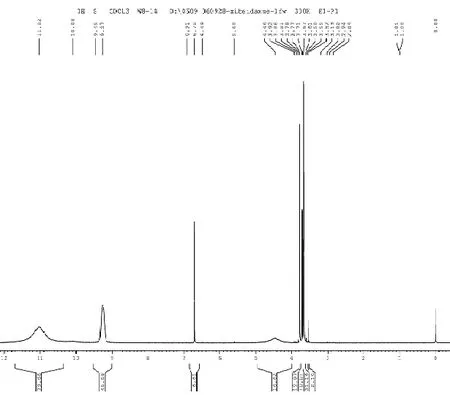
图5 三氧化硫与甲烷反应液相产物1H谱的核磁共振谱图Fig.5 Sulfur trioxide with liquid methane reaction product 1H NMR
由图5看出, 0处对应的峰为加入的硝基甲烷用来定零基准,3到4之间的峰为硫酸单甲酯和硫酸二甲酯,7到8之间的峰为碘甲烷。确定方法为内标法,通过在液相产物中加入硫酸二甲酯或碘甲烷,可以通过同一时间峰面积大小的变化对比进行判断。另外,将产物进行蒸馏后,采用色谱-质谱联用检测馏出液的成分,由气质联用谱图得出,蒸馏产物中含有甲醇,硫酸二甲酯,证明中间产物硫酸单甲酯的存在,而硫酸单甲酯在减压蒸馏的过程中会转化成硫酸二甲酯。同时,蒸馏出的产物中含有少量SO2,这是硫酸单甲酯分解产生的。
通过对反应产物检测与理论分析,我们提出SO3体系中甲烷部分氧化反应机理是亲电取代反应机理。碘催化的甲烷亲电反应机理可描述如图6所示。
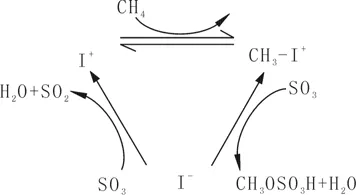
图6 甲烷部分氧化I2催化循环图Fig.6 I2catalytic partial oxidation of methane cycle map
4 结 论
在 SO3体系中,以碘系列化合物为催化剂研究甲烷部分氧化反应,对催化剂进行筛选并考察反应工艺条件的影响,最终得出以下结论:
(1)SO3体系中进行的甲烷部分氧化反应,碘系列化合物均可起到催化反应的作用,硫酸氢甲酯是转化反应的第一步产物,进一步水解得到甲醇。
(2)对催化剂进行筛选,最终确定催化剂为碘单质。
(3)在SO3体系中以碘单质为催化剂进行甲烷液相部分氧化反应,最优工艺条件确定为:催化剂用量0.099 mol·L−1,温度T=433 K,初始压力P=4.0 MPa,搅拌速度500 r/min。该工艺条件下甲烷转化率可达63.57%,目的产物收率为52.6 %,产物选择性82.74%。
(4)I2溶解在 SO3中,形成 I+或 I2+,反应遵循亲电取代反应机理。
[1] Xiao G, Yimin Zhu, Henning Birch, et al.Iodine as catalyst for the direct oxidation of methane to methyl sulfates in oleum[J].Appl Catal A, 2004, 261: 91- 98.
[2] Periana R A, Doube J T, Gamble S, Taube H, Satoh T, Fujii H.Platinum catalysts for the high-yield oxidation of methane to methanol derivation [J].Science,1998, 280: 560-564.
[3] Michalkiewicz B, Kalucki K, Sosnicki J G.Catalytic system containing metallic palladium in the process of methane partial oxidation[J].J Catal, 2003, 215: 14-19.
[4] Oxgaard J, Periana R A, Goddard W A.Mechanistic Analysis of Hydroarylation Catalysts[J].J Am Chem Soc, 2004, 126: 11658-11665.
[5] Periana R A, Bhalla G, Tenn W J, Young K J H, Liu X Y,Mironov O, Jones C J, Ziatdinov V R.Perspectives on some challenges and approaches for developing the next generation of selective, low temperature, oxidation catalysts for alkane hydroxylation based on the CH activation reaction[J].J Mol Catal A, 2004, 220: 7–25.
[6] Shilov A E, Shulpin G B.Activation of C-H bonds by metal complexes[J].Chem Rev, 1997, 97(8): 2879-2932.
[7] Periana R A, Doube J T, Evitt R E, Lottler D G, Wentrcek P R, Voss G, Masuda T.A mercury-catalyzed high-yield system for the oxidation of methane to methanol [J].Science, 1993, 259: 340-343.
[8]陈立宇, 杨伯伦, 张秀成, 董武, 张小平.含钒杂多酸催化发烟硫酸中甲烷液相部分氧化反应[J].催化学报,2006,27(6):462-464.
[9]李锋伟,甲烷液相催化氧化制甲醇的工艺研究[D].西安:西北大学, 2007.
[10]陈立宇,杨伯伦,张秀成,董武.甲烷液相部分氧化合成甲醇过程研究[J].高校化学工程学报,2005,19(1):54-58.
Iodine-Catalyzed Partial Oxidation of Methane in SO3system
LI Ming-hua1,2, HONG Lin1, Chen Li-yu1
(1.College of Chemical Engineering,Northwest University, Shaanxi Xi’an 710069,China;2.Department of Chemistry ,Fourth Military Medical University, Shaanxi Xi’an 710032, China)
Using iodine compounds as catalyst, partial oxidation reaction of methane in SO3system was studied.Catalysts were screened, and effect of process conditions were investigated, the reaction mechanism was discussed.The results show that the best catalyst is I2;the optimal process conditions are as follows: temperature is 433 K, amount of the catalyst is 0.099 mol·L−1,the initial pressure is 4 MPa, the stirring speed is 500 r/min.Under above conditions, the methane conversion rate is 63.57%, the yield of target product is 52.6%, and the product selectivity is 82.74%.
Methane;Partial oxidation;Iodine catalysis;SO3system
TQ 203.2
A
1671-0460(2012)04-0348-04
2012-02-28
李明华(1983-),女,陕西西安人,助教,硕士,2009年毕业于西北大学化学工艺专业,研究方向:从事材料、催化剂研究工作。E-mail:76150836@qq.com。

