二维片状二钛酸钡颗粒的熔盐法合成
徐 军,冷浩博,伍建华
(武汉工程大学材料科学与工程学院,湖北 武汉 430074)
0 引 言
铁电材料是一类应用广泛的材料,它能大量地应用到微电子、光电子、微机电领域,因此受到人们的广泛关注[1].但是传统的铁电材料锆钛酸铅Pb(ZrxTi1-x)O3(PZT)含有大量对人体和环境有害的Pb,因此势必面临淘汰的命运.目前,研究一类新的环境友好型铁电材料成为铁电领域的热点.近年发现的新型无铅铁电材料BaTi2O5有并不输于PZT等传统材料的介电性能[2-3],其居里温度TC高达475 ℃,在其b轴方向上其介电常数能达到30 000,是现在被作为陶瓷电容器介质大量使用的BaTiO3的介电常数的2~3倍.但是,BaTi2O5在其a轴和c轴方向上的介电常数仅为100左右,因此BaTi2O5的介电性能具有很大的各向异性.基于应用的目的,BaTi2O5陶瓷的织构化就成为必要条件.
制备织构化陶瓷一个行之有效的方法就是先制备具有各向异性形貌的颗粒[4].软化学方法合成在制备复杂氧化物颗粒和控制其形貌上具有很大的优势[5-6].目前,有关BaTi2O5的软化学方法合成的报道非常少,且制备的BaTi2O5颗粒形貌均为等轴状[7-9]、一维长线状[10]或短棒状.本文在我们前期利用BaCO3和TiO2制备BaTi2O5一维纳米棒(另文发表)的基础上,利用制备出的片状TiO2为反应原料,通过熔盐法制备出了二维片状 BaTi2O5颗粒.
1 实 验
1.1 片状TiO2模板的制备
以K2CO3(AR), Li2CO3(AR), 和TiO2(AR)为原料,以KCl(AR)为熔盐,按照具有纤铁矿层状结构的K0.8Ti1.73Li0.27O4(KTLO)的化学计量比称量K2CO3, Li2CO3, 和TiO2粉末,与同等质量的KCl混合在玛瑙研钵中研磨均匀.然后将混合粉末放进氧化铝坩埚放入高温炉中在1 000 ℃的条件下保温20 h,炉冷至室温.反应产物用蒸馏水溶解,利用高速离心机(TG16-WS) 10 000 r/min离心,分离,如此重复清洗8次后, 在烘箱中80 ℃干燥.
制备的KTLO放入配好的1mol/L的HNO3(68%)溶液中,利用H+交换K+,Li+离子.酸交换一天,重复两次,保证K+,Li+离子完全被H+离子取代,所得到的产品用蒸馏水清洗,然后室温干燥,得到酸交换后的产物H1.07Ti1.73O4·nH2O(HTO).
将3.211 g的HTO在30 mL的蒸馏水中利用磁力搅拌器搅拌2 h,放入带聚四氟乙烯内衬的不锈钢反应釜,在200 ℃的条件下水热反应一天.反应产物用高速离心机10 000 r/min分离,循环清洗8次.最后将得到的粉体产品(片状TiO2)放入烘箱80 ℃干燥过夜.
1.2 片状BaTi2O5颗粒的制备
按照摩尔比1∶2称量BaCO3和制得的片状TiO2,与适当大小和质量的玛瑙球混合,以无水乙醇为介质,在玛瑙球磨罐中在行星式球磨机(QM3S-P04)上球磨混合12 h,转速504 r/min.混合粉末经干燥后,与相等质量的共晶成分NaCl-KCl熔盐(熔点650 ℃)混合,在玛瑙研钵中研磨30 min,放入高温炉中在840 ℃的条件下,保温5 h,炉冷至室温.反应产物在蒸馏水中用高速离心机10 000 r/min离心清洗8次后,放入烘箱80 ℃干燥过夜.
1.3 相成分和颗粒形貌的表征
对各反应产物,利用带单色器的铜靶粉末X射线衍射(XRD)分析仪(日本理学D/MX-ⅢAX)分析相纯度,利用扫描电子显微镜(JSM-5510LV)观察其形貌特征.
2 结果与讨论
图1(a)是第一步熔盐法1 000 ℃,20 h下制备的KTLO的XRD图谱,与标准卡片JCPDS(NO.089-5420)吻合,峰强度的相对变化是由于制备的KTLO的片状形貌(图2(a))所导致的择优取向引起的.经过酸交换后得到的HTO并没有相对应的标准卡片,但XRD图谱(图1(b))与Feng等人[5]所报道的一致.KTLO和HTO均具有纤铁矿层状结构,层间距分别为0.781 nm和0.922 nm,形成离子交换通道.在酸处理的过程中发生了离子交换,H+取代了K+和Li+,此为原位拓扑反应,因此KTLO的形貌得以保存.图2给出了KTLO和HTO的扫描电镜照片.从图中可以看到KTLO为分散良好的片状颗粒,长20~50 μm,宽10~30 μm,厚度大约为5 μm.其光滑的表面及棱角分明的形貌表明为单晶颗粒,适合用来作为模板进行下一步反应.制得的HTO很好地保持了KTLO的形貌和大小,证明酸交换过程通过原位拓扑反应进行.
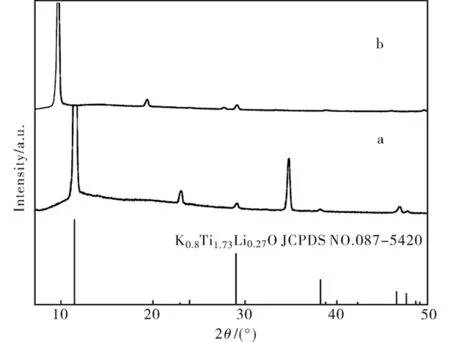
图1 (a)熔盐法制备的K0.8Ti1.73Li0.27O4 (KTLO)样品和(b)酸交换处理KTLO制备的HTO样品的XRD图谱Fig.1 X-ray diffraction patterns of (a) K0.8Ti1.73Li0.27O4 (KTLO) sample prepared by the molten salt method and (b) H1.07Ti1.73O4nH2O (HTO) sample obtained by acid-treatment of the KTLO sample.

图2 制备的KTLO(a),HTO(b)和TiO2(c)颗粒的SEM照片.Fig.2 SEM photographs of the prepared KTLO(a),HTO(b) and TiO2(c) samples.
图3为HTO经过水热反应之后得到的TiO2的XRD图谱,与锐钛矿的标准卡片(JCPDS NO.021-1272)完全一致,表明制得的是锐钛矿结构的TiO2纯相.
其形貌在图2(c)中给出.可以看到片状的TiO2颗粒也很好的保留了HTO的形貌,这正是由于层状结构的HTO具有优秀的离子交换性能,使HTO的水热反应也得以原位拓扑的方式进行而不改变其形貌.

图3 水热法制备的片状TiO2颗粒的XRD图谱Fig.3 XRD pattern for the plate-like TiO2prepared by hydrothermal treatment
图4是利用BaCO3和片状TiO2在NaCl-KCl复合熔盐中在840 ℃保温5 h制备的BaTi2O5的XRD图谱,可以看到与标准卡片(JCPDS NO.34-0133)吻合.扫描电镜照片(图5)显示合成的BaTi2O5为片状颗粒,长20~50 μm,宽10~20 μm,厚约5 μm.边缘有些不规则,应为在球磨混合过程中的机械碰撞所致.同时可以看到从片状颗粒表面生长出许多无规则取向的纳米棒.

图4 以片状TiO2为反应原料通过熔盐法制备的BaTi2O5的XRD图谱Fig.4 The XRD pattern for BaTi2O5 synthesized by the molten salt method using the plate-like TiO2 as precursors
根据笔者前期的研究,在与本文相同的熔盐法制备条件下,以普通TiO2粉末为原料所制备出的为BaTi2O5纳米棒.本文利用片状TiO2为原料,制备出了BaTi2O5的片状颗粒,其尺寸基本保持了TiO2片状颗粒的大小,表明在该熔盐法反应过程中,TiO2也起到了模板的作用.其反应机理与前述HTO和TiO2合成过程中的原位拓扑反应不同,来源于熔盐法反应的另一机制:溶解-沉积机制.BaCO3和TiO2在NaCl-KCl熔盐中反应时,溶解的反应物分子扩散到未溶解的相异的反应物颗粒表面发生反应并沉积在上面.由于TiO2在NaCl-KCl熔盐中的溶解速度要大大慢于BaCO3[6],因而溶解更快的BaCO3分子扩散到未溶解的TiO2颗粒表面发生反应生成BaTi2O5并发生沉积,结果TiO2成为反应的模板,反应产物(BaTi2O5)保留了TiO2颗粒的形貌.本文中所用的TiO2片状颗粒较大,反应在表面各处缺少关联,结果产生从表面生长的取向无规则的纳米棒.

图5 从片状TiO2制备的BaTi2O5颗粒的扫描电镜照片Fig.5 SEM photograph of BaTi2O5 prepared from plate-like TiO2
3 结 语
软化学方法具有反应温度相对较低,可以控制反应产物形貌的优点.首先用熔盐法合成具有纤铁矿层状结构的KTLO作为初始模板,通过原位拓扑反应机制,先后利用酸交换和水热反应制备出保留KTLO形貌的HTO和TiO2.所得到的锐钛矿TiO2为片状颗粒,长20~50 μm,宽10~30 μm,厚度大约为5 μm.以片状TiO2和BaCO3为反应原料,在NaCl-KCl混合熔盐中在840 ℃保温5 h条件下得到了片状BaTi2O5颗粒,基本保持了片状TiO2颗粒的大小.反应机制为溶解-沉积机制,由于TiO2在熔盐中的溶解速度大大低于BaCO3,因此反应基本在TiO2颗粒的表面发生,从而反应产物BaTi2O5保留了TiO2的片状形貌.
参考文献:
[1] Scott J F. Applications of modern ferroelectrics[J], Science. 2007, 315:954-959.
[2] Akishige Y,Fukano K,Shigematsu H.New ferroelectric BaTi2O5[J].Japanese Journal of App1ied Physics,2003,42(8A):L946-L948.
[3] Akashi T, Iwata H, Goto T. Dielectric property of single crystalline BaTi2O5prepared by a floating zone method[J]. Materials Transactions,2003,44(8):l644-1646.
[4] Saito Y, Takao H, Tani H, et al. Lead-free piezoceramics[J]. Nature,2004,432:84-87.
[5] Qi Feng.Solvothermal soft chemical synthesis and characterization of plate-like particles constructed from oriented BaTiO3nanocrystals[J]. Journal of the Ceramic Society of Japan,2010,118(2): 141-146.
[6] Huang K C, Huang T C, Hsieh W F. Morphology-controlled synthesis of barium titanate nanostructures[J]. Inorganic Chemistry, 2009, 48: 9180-9184.
[7] Tangiuank S,Tunkasiri T.Sol-gel synthesis and characterization of BaTi2O5powders[J].App1ied Physics A, 2005, 81:1105-1107.
[8] Beltrán H, Gómez B, Masó N, et al. Electrical properties of ferroelectric BaTi2O5and dielectric Ba6Ti17O40ceramics[J]. Journal of Applied Physics, 2005, 97:084104.
[9] Xu J, Akishige Y. KF-doped BaTi2O5ferroelectric ceramics by solid state reaction of KF and sol-gel-derived BaTi2O5powders[J]. Applied Physics A, 2008, 90:153-157.
[10] Deng Z, Dai Y, Chen W, et al. Synthesis and characterization of single-crystalline BaTi2O5nanowires[J]. Journal of Physical Chemistry C, 2010, 114: 1748-1751.

