1039例隐源性肝炎患者AMA-M2抗体的筛查
张 玮 王 磊 王 奕 王俐琼 杜慧慧 李青梅
原发性胆汁性肝硬化(Primary biliary cirrhosis,PBC)是一种慢性进展性自身免疫性肝病,多见于女性[1]。国外文献报道该病患病率呈逐年增加趋势[2]。PBC 起病隐匿,症状不典型,发现时患者往往处于疾病的晚期[3],给治疗带来难度。因此,我们在1039 例隐源性肝炎患者进行了M2抗体检测,以早期诊治。
资料与方法
一、临床资料 2009年~2010年在我院就诊的肝功能异常的1039 例隐源性肝炎患者,男485例,女 554 例,平均年龄 55.0±12.1岁。PBC 的诊断根据2000年美国肝病学会(AASLD)指导建议进行[4],即:(1)碱性磷酸酶(ALP)等反映胆汁淤积的生化指标升高;(2)B 超或胆管造影检查示胆管正常;(3)血清抗线粒体抗体(AMA)或AMA-M2亚型阳性;(4)如果血清 AMA/AMA-M2阴性,则肝脏病理学检查符合PBC 的改变。经血清学和超声检查等排除非PBC 病变。
二、血清M2抗体测定 采用ELISA 法(上海富莼科芯生物技术股份有限公司),M2抗体<25 为阴性。
结果
一、M2抗体检测结果 在1039 例患者中,81例(7.9%)M2 抗体阳性(表1)。在 1039 例隐源性肝炎患者中,女性M2抗体阳性患者57 例(10.29%,57/554),男性 24 例(4.95%,24/485,P<0.01)。根据AASLD 关于PBC 指导建议,本组男性患者诊断22例,女性56 例,被排除的3 例患者均为滴定度在25~50,提示M2抗体滴度的高低和BPC 的诊断有一定的相关性,但还有待进一步证实。在PBC 患者中,男性22 例,年龄22~86岁,平均年龄52.0±17.3岁;女性56 例,年龄22~79岁, 平均年龄53.4±13.8岁。
二、两组患者免疫功能指标的比较 见表2。
表2 两组患者免疫功能指标(±s)的比较
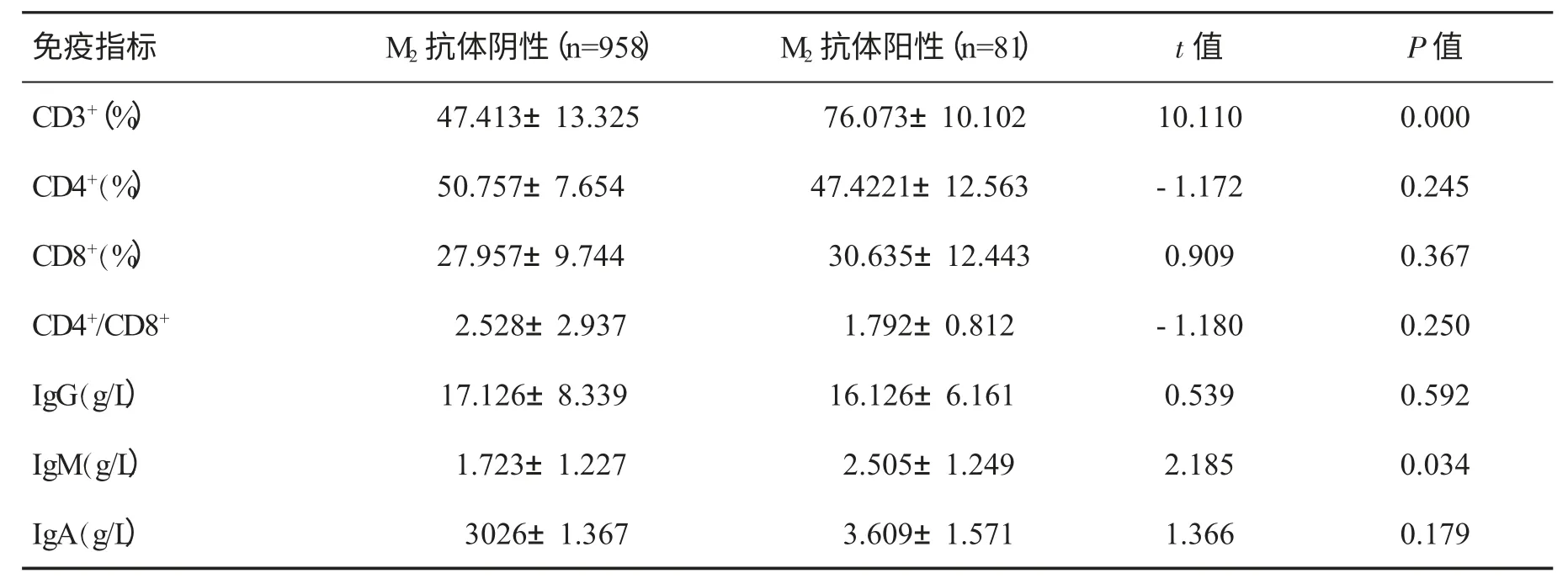
表2 两组患者免疫功能指标(±s)的比较
免疫指标 M2 抗体阴性(n=958)M2 抗体阳性(n=81)t 值 P 值CD3+(%)47.413±13.32576.073±10.10210.1100.000 CD4+(%)50.757±7.654 47.4221±12.563-1.172 0.245 CD8+(%)27.957±9.744 30.635±12.443 0.909 0.367 CD4+/CD8+ 2.528±2.937 1.792±0.812-1.180 0.250 IgG(g/L)17.126±8.339 16.126±6.161 0.539 0.592 IgM(g/L)1.723±1.227 2.505±1.249 2.185 0.034 IgA(g/L)3026±1.367 3.609±1.571 1.366 0.179
三、PBC 患者相关抗体检测情况 所有患者均检测了抗核抗体、抗Nucleosomes(核小体)抗体、抗组蛋白(Histones)抗体、抗 Sm 抗体、抗 U1-snRNP抗体、抗 SS-A/Ro 60kD 抗体、抗 SS-A/Ro 52kD 抗体、抗SS-B/La 抗体、抗着丝点(ACA)抗体、抗Scl-70 抗体、抗 Jo-1 抗体,见表3。
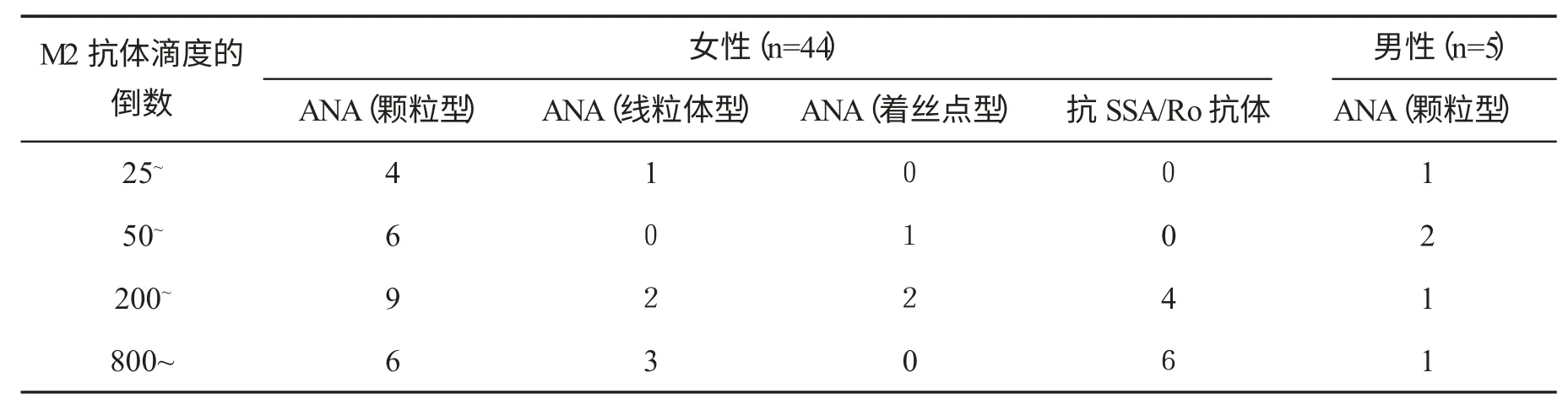
表3 PBC患者相关抗体合并情况
四、临床表现 本组以乏力(74.4%,58/78)、黄疸(38.5%,30/78)、皮肤瘙痒(37.2%,29/78)为主;14例(17.3%)患者自觉无明显症状;47.4%(37/78)病人肝脏肿大,但无触痛;24.4%(19/78)病人脾脏肿大;约14.1%(11/78)病人同时出现皮肤黄色瘤和黄斑瘤;23.1%(18/78)病人发生色素过度沉着。
五、PBC 患者肝穿刺病理学检查情况 12 例PBC 患者行肝穿刺活检,结果Ⅰ期2 例,Ⅱ期7例,Ⅲ期2 例,Ⅳ期1 例。
讨论
PBC 是以肝内细小胆管非化脓性进行性破坏,伴门脉炎症性改变为主要特征,并有长期持续性肝内胆汁淤积,最终导致纤维化和肝硬化的慢性进展性自身免疫性疾病[5]。本病多见于中年妇女[4]。其发病机制尚未明确,目前大多集中于遗传易感性、环境因素及自身免疫功能紊乱等方面[6,7]。患者起初肝功能正常,无症状,但检测抗AMA 或AMA-M2呈阳性, 80%患者在5年内出现肝功能异常[8]。随病情发展陆续出现瘙痒、疲劳、黄疸、乏力、腹痛,因维生素吸收障碍出现皮肤粗糙和夜盲症,最后出现蜘蛛痣、肝掌,肝脾肿大等肝硬化表现,晚期出现门静脉高压。同时患者常伴有干燥综合征、类风湿性关节炎、溃疡性结肠炎、甲状腺疾病、肾小管酸中毒及硬皮病等其他自身免疫性疾病。在PBC 早期,由于肝内胆管阻塞即可有血清ALP、γ-GT 水平明显升高,而ALT 和AST 水平仅轻至中度升高, 并常伴有血脂异常(以TC 升高为主)。早期血清胆红素水平可正常,而晚期随疾病进展而上升,高胆固醇血症较常见,凝血酶原时间延长[9]。
PBC 患者外周血和肝脏内均能检测到针对PDC-E2 的自身反应性CD4+和CD8+T 细胞,肝脏中这些细胞的浸润是本病的主要特征[10],肝内可见大量辅助性(CD4+)TCRαβ 细胞[11]。Ambrosini YM研究认为[12],CD45RO(high)CD57(+)CD8(high)T细胞是一个末端分化的细胞毒T 细胞(效应记忆T 细胞)的子代,在胆道上皮细胞进行性破坏中发挥重要的作用。我们研究显示,M2抗体阳性患者伴有CD3+细胞的改变。在体液免疫中,M2抗体阳性患者IgM 升高,提示体液免疫参与了本病的发病过程[13]。
M2抗体的靶抗原为线粒体内膜上的2-氧酸脱氢酶复合体(2-OADC)家族成员,尤其是丙酮酸脱氢酶复合物E2 亚单位(pyruvate dehydrogenase complex,PDC-E2)[14]。尽管所有有核细胞都含有线粒体自身抗原,但AMA 仅对肝胆管线粒体自身抗原进行免疫攻击,影响肝脏胆汁代谢[15]。此外,对没有肝脏疾病表现的AMA 阳性患者的随访观察显示可在PBC 开始出现之前的几年检测到自身抗体的存在[16],其具体免疫机制目前尚不清楚。
PBC 患者除了M2 抗体阳性外,还检测出抗核抗体(其中颗粒型出现频率最高,其次为线粒体型和着丝点型)、抗 SS-A/Ro 抗体和少量的抗U1-snRNP 抗体阳性。大约有1/3 的PBC 患者可以检测到ANA,甚至在AMA 阴性患者中更常见,阳性率仅次于AMA[14]。这与我们本次的研究基本相符。但关于抗核抗体阳性的意义还有待进一步探讨[18,19]。
[1]Lleo A,Battezzati PM,Selmi C,et al.Is autoimmunity a matter of sex?.Autoimmun Rev,2008,7:626-630.
[2]Roblin X,Bonaz B.Primary biliary cirrhosos.N Engl J Med,2005;353:2719-2720.
[3]Prince MI,Chetwynd A,Craig WL,et al.Asymptomatic primary biliary cirrhosis:clinical features,prognosis,and symptom progression in a large population based cohort.Gut,2004,53:865-870.
[4]Selmi C,Bowlus C,Gershwin ME,et al.Primary biliary cirrhosis.Lancet,2011,377:1600-1609.
[5]Invernizzi P.Update on primary biliary cirrhosis.Digest Liver Dis,2010,42:401-408.
[7]Muratori P,Granito A,Pappas G,et al.The serological profile of the autoimmune hepatitis/primary biliary cirrhosis overlap syndrome.Am J Gastroenterol,2009,104(6):1420-1425.
[8]蒋天舒,周晔,邓安梅,等.原发性胆汁性肝硬化研究进展.中国实验诊断学,2006,10(12):1539-1541.
[9]Gershwin ME,Mackay IR.The causes of primary biliary cirrhosis:convenient and inconvenient truths.Hepatology,2008,47:737-745.
[10]Shimoda S,Miyakawa H,Nakamura M,et al.CD4 T-cell autoreactivity to the mitochondrial autoantigen PDC-E2 in AMA-negative primary biliary cirrhosis.J Autoimmun,2008,31:110-115.
[11]Shimoda S,Harada K,Niiro H,et al.Biliary epithelial cells and primary biliary cirrhosis:the role of liver-infiltrating mononuclear cells.Hepatology,2008,47:958-965.
[12]Murator I,Granito A,Ferri S,et al.Multiple nuclear dots and rim-like/membranous IgG isotypes in primary biliary cirrhosis .Autoimmunity,2009,42:224-227.
[13]Agmon-levin N,Shapira Y,Selmi C,et al.A comprehensive evaluation of serum autoantibodies in primary biliary cirrhosis.J Autoimmun,2010,34:55-58.
[14]Invernizzi P,Lleo A,Podda M.Interpreting serological tests in diagnosing autoimmune liver disease.Semin Liver Dis,2007,27:161-172.
[15]Vleggaar FP,Van Buuren HR.No prognostic signif icance of antim-itochondrial antibody profile testing in primary biliary cirrhos-is.Hepatogastroenterology,2004,51(58):937-940.
[16]Metcalf JV,Mitchison HC,Palmer JM,et al.Natural history of early primay biliary cirrhosis.Lancet,1996,348:1399-1402.
[17]Muratori P,Muratori L,Ferrari R,et al.Characterization and clinical impact of antinuclear antibodies in primary biliary cirrhosis.Am J Gastroenterol,2003,98:431-437.
[18]Zhang W,Yang GX.Fine phenotypic and functional characterization of effector CD8(+)T cells in patients with primary biliary cirrhosis.Hepatology,2011,[Epub ahead of print]
[19]Hsu W,Zhang W,Tsuneyama K,et al.Differential mechanisms in the pathogenesis of autoimmune cholangitis versus inflammatory bowel disease in interleukin-2Ralpha(-/-)mice.Hepatology,2009,49:133-140.

