HPLC测定复方菊陈颗粒中绿原酸的含量
黄 媚 刘喜华
1黄媚(1979.8—),女,助理工程师,主要从事制剂开发和检验工作,广西梧州制药集团(股份)有限公司 广西梧州 543002 2 广西卫生职业技术学院 广西南宁 543002
复方菊陈颗粒是由菊花等多味中药组成的复方制剂,具有散风清热、燥湿健脾等功效,可用于风热感冒、厌食口腻等症状,临床上还将其用于解酒、醒酒等方面。本实验以菊花中的绿原酸为控制指标,采用高效液相色谱法(HPLC)对成品进行质量控制。
1 仪器和试药
1.1 仪器
Agilent1100高效液相色谱仪(美国安捷伦科技有限公司);Ultimate XB-C18(月旭材料科技(上海)有限公司,4.6×250mm,5μm);BS224S电子天平(北京赛多利斯);LG-16WA台式高速离心仪(北京京立离心机有限公司);SB5200DT超声波清洗仪(宁波新芝生物科技股份有限公司)。
1.2 试药
绿原酸对照品,供含量测定用,购于中国药品生物制品检定所,批号为:110753-200413;甲醇、乙腈(美国fisher公司,色谱醇);娃哈哈纯净水(杭州娃哈哈集团有限公司);其它试剂为分析纯;复方菊陈颗粒三批(本公司自行研制,批号:110901、110902、110903)。
2 方法与结果
2.1 色谱条件
结合预试验结果,按以下条件和方法进行。色 谱 柱:Ultimate C18柱(4.6×250mm,5μm);流动相:乙腈-0.1%磷酸梯度洗脱(详见表1);流速:1.0mL·min-1;检测波长:328nm;柱温:300;进样量:10μL;理论塔板数计算应不少于7500[1-3]。分别取对照品溶液、供试品溶液、阴性样品溶液按照上述色谱条件进行测定。结果表明:供试品溶液中绿原酸能与相邻组分峰分离,分离度R>1.5,阴性对照品溶液无干扰,色谱图见图1-3。

表1 绿原酸含测梯度洗脱程序(后运行时间:10min)
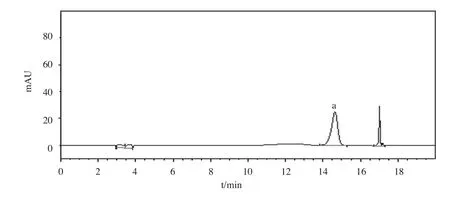
图1 绿原酸对照品色谱图(a为绿原酸)
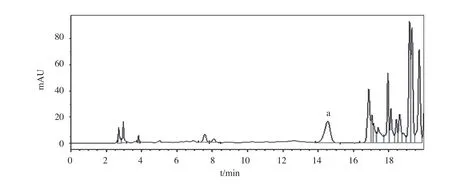
图2 供试品色谱图(a为绿原酸)

图3 阴性样品色谱图
2.2 溶液的制备
2.2.1 对照品溶液的制备
精密称取低温真空干燥至恒重的绿原酸对照品适量,加甲醇至溶解制成每1ml中含33.04μg绿原酸对照品溶液。
2.2.2 供试品溶液的制备
取样品研细1g,精密称定,置具塞锥形瓶中,加入甲醇20ml,称定重量,超声提取60min,放冷至室温,再称定重量,用甲醇补足减失重量,摇匀,滤过,取续滤液,过0.45μm微孔滤膜即得。
2.2.3 阴性样品溶液的制备
按处方比例配制成不含菊花的阴性样品,并按2.2.2项下方法制成阴性样品溶液。
2.3 线性关系考察
精密称取绿原酸对照品4.13mg置于25m1容量瓶中,加甲醇溶解,并定容至刻度,制成浓度为165.2μg/ml的绿原酸对照品溶液,然后分别稀释成 82.6、33.04、16.52、6.608μg/ml。按上述色谱条件,分别吸取这5个对照品溶液10μl进样,测定峰面积。以峰面积为纵坐标,对照品溶液浓度为横坐标绘制标准曲线,并计算得回归方程为Y=23.818X-63.398,r=0.9998。结果表明,绿原酸在进样量为0.066μg~1.652μg线性良好。
2.4 精密度试验
精密吸取浓度为33.04μg/ml的绿原酸对照品溶液10μ1,按上述色谱条件重复进样6次,测定绿原酸峰面积,RSD值仅为0.39%,表明仪器的精密度良好。
2.5 稳定性试验
取同一供试品溶液,分别在制备后0,2,4,6,8,10,12h精密吸取10μl进样,记录每次进样绿原酸峰面积,RSD值为2.06%,表明供试品溶液在12h内稳定。
2.6 重复性试验
取同一批样品(110901)6份,按供试品溶液的制备方法制备,进样10μl,测定峰面积。计算绿原酸含量。绿原酸平均含量为0.3820mg·g-1,RSD值为2.29%,表明该方法的重复性良好。
2.7 加样回收率试验
取已测得绿原酸含量的样品(110901)6份,每份1g,精密称定,置具塞锥形瓶中,分别精密加入一定量的绿原酸对照品,按2.2.2项下的方法制备供试品,在上述色谱条件下依法测定,计算回收率,结果见表2。
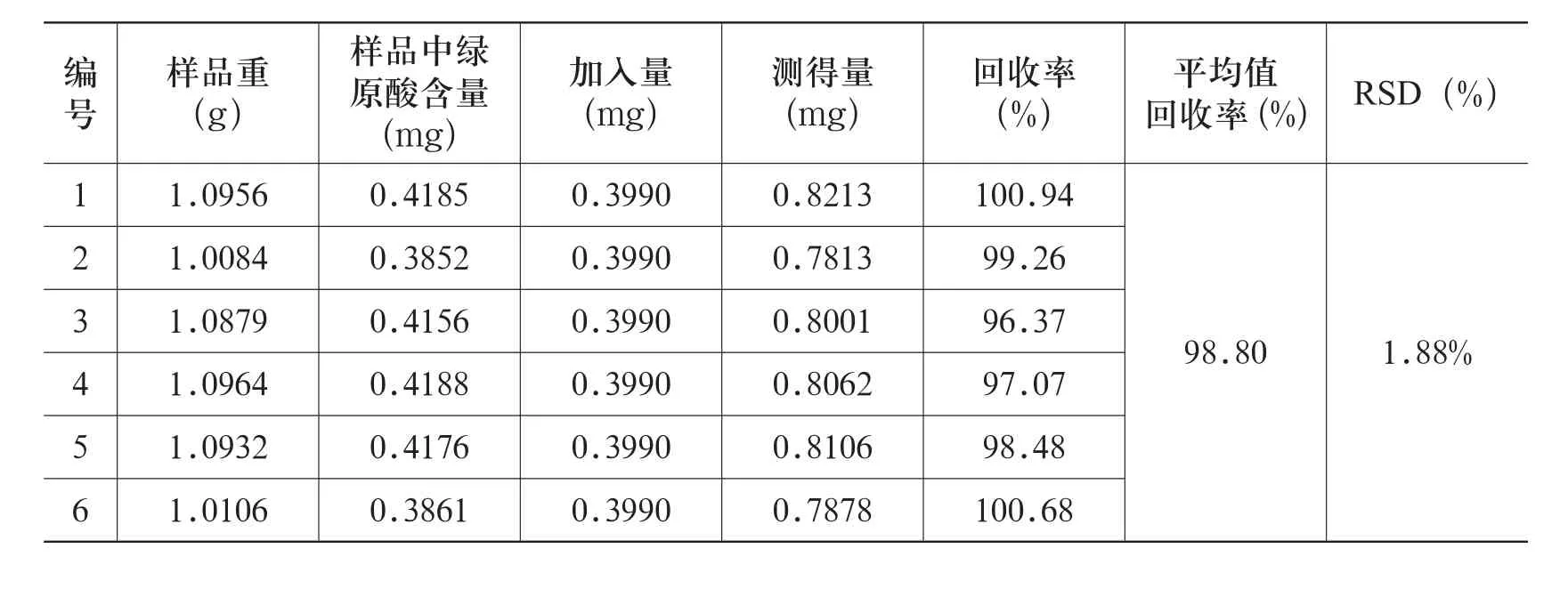
表2 绿原酸加样回收试验结果
2.8 样品测定
取三批样品研细,取1g,精密称定,按2.2.2项下的方法制备供试品溶液。分别精密吸取对照品溶液和样品溶液各10μ1,注入液相色图谱仪,测定绿原酸峰面积,外标法计算绿原酸的含量,结果见表3。表中RSD值为0.04%,表明三批样品绿原酸含量稳定。

表3 样品绿原酸含量测定
3 讨论
3.1 预实验曾对绿原酸采用了高效液相的等度洗脱,但在连续注入数个样品之后,后期色谱图基线出现了极大的波动,可能为低极性物质保留时间过长导致,于是将绿原酸的测定改为梯度洗脱,使低极性物质不影响绿原酸的测定,同时节省分析时间。
3.2 供试品中的绿原酸进行DAD扫描,结果发现在328nm处有最大吸收,故确定其作为检测波长。同时对供试品制备方法进行了提取溶剂、提取方法、提取时间的考察,结果表明:甲醇提取的绿原酸比水及乙醇提取的更充分;超声提取比回流提取及索氏提取的更完全;30min、60min、90min提取以60min提取的含量最高,故供试品制备方法按上述最佳条件进行。
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:化学工业出版社,2010:292.
[2]陈秋虹,徐慧,蒋艳芳.高效液相色谱法测定桑叶中的绿原酸和芦丁的含量[J].中华中医药杂志,2009,(5):663-665.
[3]吴怀恩,劳深,王雯慧,等.HPLC测定石韦配方颗粒中绿原酸、咖啡酸及芒果苷的含量[J].中国实验方剂学杂志,2010,16(16):54-61.

