HPLC法测定氢化可的松洗剂的含量
赵玉平 杨夏 高峰丽
氢化可的松洗剂是由氢化可的松、甘油、乙醇及蒸馏水配制而成。在临床上多做为医院自制制剂,临床应用广泛[1],用于抗菌止痒,多用于过敏性皮炎、脂溢性皮炎、瘙痒症。医院拟标准多采用紫外分光光度法测定氢化可的松洗剂中氢化可的松的含量,该方法准确度低。查阅相关文献,对氢化可的松洗剂含量测定的研究很少,本实验为了控制氢化可的松洗剂的质量,采用高效液相方法对其进行研究[2]。
1 仪器与试药
Vertex STIP5000高效液相色谱仪,535型紫外检测器(美国生物公司);氢化可的松洗剂(医院自制);氢化可的松对照品(实验室提取制得,纯度99.9%);乙腈为色谱纯,水为蒸馏水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:Kromstar C18柱(4.6 mm×250 mm,5 μm);流动相:乙腈-水(28∶72);检测波长:245nm;流速:1.0 ml.min;柱温:室温。进样量:10 μl。
2.2 溶液的制备 ①对照品溶液制备:精密称取氢化可的松对照品10.0 mg置50 ml量瓶中,加甲醇稀释至刻度,摇匀,制成氢化可的松对照品溶液。氢化可的松含量为0.20 mg/ml。②供试品溶液制备:精密量取本品1.0 ml至50 ml量瓶中,加甲醇稀释至刻度,摇匀,即得氢化可的松供试品溶液。③阴性样品溶液的制备:按处方量取除氢化可的松外的氢化可的松洗剂各原辅料,依法制成不含氢化可的松阴性供试品,按“②”项下方法制备阴性样品溶液。
2.3 系统适用性试验 分别精密吸取上述对照品溶液、供试品溶液和阴性样品溶液各10 μl,注入高效液相色谱仪,记录色谱图。结果表明,氢化可的松的理论塔板数不低于3000,分离度大于1.5,拖尾因子等符合要求。阴性样品对氢化可的松含量测定无干扰。色谱图见图1。
2.4 线性关系考察 分别精密量取氢化可的松对照品溶液(0.2 mg/ml)2.0,4.0,6.0,8.0,10.0 ml置10 ml量瓶中,加甲醇稀释至刻度,摇匀,制成系列标准品溶液,按“2.1”项下色谱条件各进样10 μL,记录色谱图,测定各浓度氢化可的松的峰面积,以各对照品溶液的峰面积Y对浓度X作线性回归,得回归方程为Y=1.97965×105X+101534,r=0.9996。结果表明,氢化可的松在0.04~0.2 mg/ml的范围内与峰面积呈良好的线性关系。
2.5 精密度试验 取“①”项下制备的对照品溶液,连续进样6次,测定峰面积,RSD=0.82%,表明仪器精密度良好。
2.6 重复性试验 取批号为20120224的供试品溶液6份,照样品测定法项下方法测定,RSD=1.45%(n=6),方法重复性良好。
2.7 稳定性试验 取批号为20120224的样品溶液,分别于0,1,2,4,8,24 h 进样测定,RSD 为 1.61%,表明供试品溶液在24 h内稳定。
2.8 加样回收率试验 取同一批号(20120309)已知含量的氢化可得松样品适量,按“②”项下方法制备供试品溶液,分别加入对照品溶液5、10、15 ml,按“2.1”项下色谱条件进样测定,计算平均回收率100.13%(n=9)。
2.9 样品的含量测定 精密量取按“②”项下方法制备的对照品溶液和按“②”项下方法制备的供试品溶液,并按“2.1”项下色谱条件进样测定,进样量为10 μl。以外标法计算样品中氢化可的松的含量。见表1。

图1 高效液相色谱图
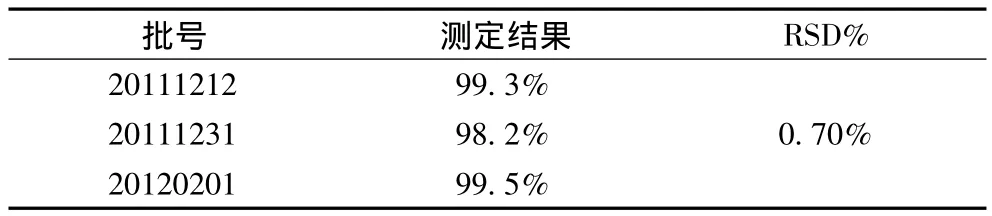
表1 氢化可的松洗剂测定结果(标示量%,n=3)
3 讨论
3.1 检测波长的选择 精密称定氢化可的松对照品10 mg,至50 ml量瓶中,加甲醇稀释至刻度,摇匀。照分光光度法进行扫描,结果在245 nm的波长处有较大吸收,故选取245 nm为检测波长。
3.2 流动相的选择 通过查阅文献资料,对氢化可的松洗剂的研究很少,《中国药典》2010版曾用乙腈-水对氢化可的松注射剂进行测定,选乙腈-水不同比例的流动相进行试验,结果选用乙腈-水(28∶72),峰形好,保留时间适中。本法操作简单、准确、重现性好,与紫外分光光度法比较,方法专属性更强,适用于该产品的质量控制。
[1] 邵建斌.氢化可的松洗剂及霜剂的含量测定.秦州职业技术学院学报,2010,10(3):36-37.
[2] 国家药典委员会.中国药典.二部.中国医药科技出版社,2010:550.
[3] 陈笑天,刘慧莹,刘小英,等.HPLC法测定尿素氢化可的松乳膏中氢化可的松的含量.江西中医学院学报,2011,23(5):69-70.

