注射型胶原蛋白填充剂在整形美容外科中的应用现状
柯林楠 王晨 冯晓明
1 中国食品药品检定研究院(北京 100050)
2 北京市药品监督管理局医疗器械技术审评中心(北京 100053)
随着生活质量的提高,人们不仅追求生活得健康,更追求生活得美丽。人们寻找安全、有效、经济的方式减轻老化迹象,减少脸部皱纹,改变容貌。近年来相对安全有效的医疗美容方式是在面部软组织直接注射填充剂,修复皮肤组织缺损。
用于软组织填充的注射型填充剂已经被FDA归为医疗器械批准上市。目前FDA 已经批准的用于整形美容外科的四类可吸收材料包括:(1)胶原蛋白;(2)透明质酸钠 ;(3)羟基磷灰石;(4)聚乳酸。这四类材料还可以与不可吸收的高分子材料(如聚甲基丙烯酸甲酯,简称“PMMA”)复合作为填充剂。其中胶原蛋白是一类天然蛋白质,作为皮肤组织的主要组分,是纠正面部软组织缺陷的较为理想的材料。
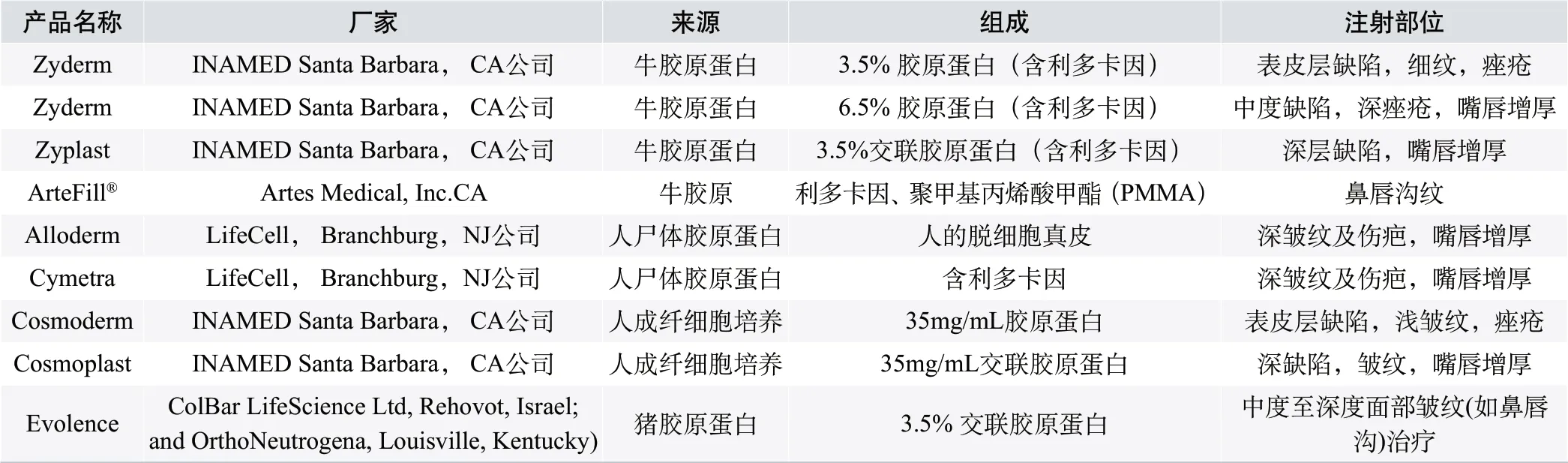
表1.FDA 已经批准上市的填充剂产品[5,6]
1.注射型胶原蛋白植入剂简介
1.1 胶原蛋白作为面部软组织填充材料具有的优点
(1)良好的生物相容性。植入组织的胶原蛋白对生物体无毒性、无刺激性。
(2)可以与细胞相互作用。胶原蛋白是细胞外基质的主要成分,作为细胞生长的依附与支架,胶原蛋白填注入矫形部位后,能诱导上皮细胞等的增殖分化和移植,促使细胞进一步合成新生胶原,产生与宿主相同的新生组织,与周围正常皮肤共同作用,从而起到矫形作用,恢复正常外观。
(3)良好的机械性能。胶原蛋白分子的三条α 肽链相互缠绕形成的右手螺旋[1],以及分子内、分子间集团的交联,均使得胶原具有良好的强度、弹性[2]。
(4)保湿性。胶原蛋白分子中含有大量羧基与羟基等亲水集团,使得胶原蛋白分子极易与水形成氢键,因此胶原蛋白具有良好的保水保湿性能。
(5)低免疫原性。胶原蛋白具有甘氨酰(Gly)-X-Y(脯氨酸经常占据X 位,羟脯氨酸占据Y 位)的重复结构,是一类免疫原性很低的蛋白质大分子,其主要抗原决定簇存在于胶原分子两端的非螺旋区。在胶原蛋白的提取过程中,可用胃蛋白酶将引起免疫原性的端肽选择性切掉,进而使其本已很弱的免疫原性进一步降低[3]。
(6)生物可降解性。胶原蛋白在胶原酶的水解作用下,胶原肽键会发生断裂,其螺旋结构随即破坏,断裂的胶原多肽能被大多数蛋白酶水解[4]。
1.2 FDA 已经批准上市的注射型胶原蛋白填充剂产品
由于胶原蛋白具有良好的生物相容性、可降解性、低的免疫原性以及大规模生产的可行性等优点,使得胶原蛋白在整形美容外科中占有重要位置。到目前为止,FDA 已经批准了几家公司的注射型胶原蛋白填充剂(简称“填充剂”),用以皱纹、寻常痤疮疤痕、小型外伤疤痕等缺陷的填充矫正。这些产品主要以牛皮、猪皮或人体组织作为原料来源,通过加工处理过程获取高纯度的胶原蛋白,在无菌条件下,将纯化的胶原蛋白均匀分散于磷酸盐缓冲液中配成不同浓度的胶原蛋白悬浮液后,充填于无菌注射器中制成。表1 为FDA 已经批准上市的填充剂产品。
2.注射型胶原蛋白填充剂的质量控制
根据国家食品药品监督管理局(SFDA)有关规定,注射型胶原蛋白填充剂作为植入人体的医疗器械,被归为三类产品,属于高风险产品,它的安全性受到普遍关注:
(1)目前疯牛病(BSE)、口蹄疫(FMD)等疫病的发生,会对陆生哺乳动物胶原蛋白及其制品的安全性造成威胁,为了保证原料来源质量可控性和重复性,应该固定胶原蛋白的动物来源、取材部位,并有符合动物源医疗器械管理要求的检验检疫证书,以备追溯查证。
(2)胶原蛋白原料来自于动物界和人类,有携带感染性疾病等潜在危险,要进行原料检疫、病毒测试,采取有效措施进行病毒去除或灭活,降低病毒传播的危险,以保证其使用安全性。
(3)尽管胶原蛋白与许多其他蛋白质相比,其免疫原性很弱,但免疫学分析和研究结果表明,胶原蛋白分子中非螺旋的区域(又被称为“端肽”),是引起免疫原性的主要位点,目前主要是在胶原蛋白提取过程中,通过有选择性的水解或失活来去除端肽。另外,由于胶原蛋白来自于复杂的生物组织,细胞膜的表位抗原,同种异体或异种材料中的DNA以及某些蛋白质,如S-100等[7]都可能会引起人体的免疫排斥反应,所以应在胶原蛋白分离纯化过程对这些免疫原性因子予以去除。生产企业应该对胶原蛋白填充剂中免疫原性因子的残留量进行检测,制定科学合理的限量标准,并建立该类产品的免疫评价方法。
(4)在制备填充剂的过程中,由于原料的来源、加工工艺、生产环境等因素均可引入各类杂质,比如重金属,它们是对人体存在危害的物质,应该严格控制。
(5)为了满足临床需要,在填充剂加工过程中还会引入某些添加剂(比如控制产品降解时间及增加强度的交联剂,目前多采用戊二醛;可以起到局部麻醉作用的利多卡因药品等),这些外源物质虽然在产品中含量甚微,但若大量使用或使用不当或有过敏因素存在时,都有可能引发不良反应。因此,必须针对植入剂生产过程的具体情况,对可能存在安全隐患的添加剂,建立它们的残留检测和质量控制的方法。
目前,已有数家生产企业申请填充剂产品在国内注册上市,但是国内外尚无普遍认可的关于填充剂产品的通用性要求或质量标准,各个企业依据自己的生产和检验条件制定注册产品标准,标准中检验方法不统一,有的甚至不能满足检验该产品的需要。为规范控制此类产品质量,保障人们健康、用械安全,加强监管,有关部门应该尽快出台该产品的行业标准。
3.展望
自1981年,第一个胶原填充剂产品Zyderm被FDA 批准上市,到今天已经使用了近30年,临床结果表明胶原蛋白填充剂是安全有效的。根据美国整形手术协会(ASPS)调查表明,从1992年到2002年的,在美国实施整形手术的人数已经增加了393%,这种增长势头也反映了全球的趋势[8]。目前在中国,注射型胶原蛋白填充剂的市场潜力巨大。在人口老龄化,人类越来越关注自身的健康以及追求高质量的生活品质的今天,填充剂有着广阔的市场开发前景。我国是农业大国,胶原蛋白原料来源丰富,如何有效地利用资源,提高产品附加值,对于实现可持续发展的绿色经济有着十分重要的现实意义和深远的历史意义。基于此,近年来研究者将研究主要集中在:(1)弄清胶原蛋白的结构和性能之间的关系,以便高效率提取及分离纯化胶原蛋白,提高胶原蛋白的纯度,降低产品的成本。(2)通过对胶原蛋白化学修饰、交联以及与其他材料复合的方式,改善胶原蛋白填充剂性能,如控制降解速率、提高机械强度等以延长美容效果,适用不同美容部位。(3)考虑到疯牛病、口蹄疫等动物源性有关的疾病对人类的威胁,以及来自于异种种属的蛋白可能引起人类的过敏、免疫反应,寻找合适的胶原蛋白来源加以利用,如重组人胶原蛋白,实现产品安全、质量稳定等优点。随着研究的不断深入和生产工艺的改进,将会有越来越多满足人们不同需要,价廉质优的胶原蛋白填充剂出现,造福人类。
[1]刘秉慈.胶原蛋白作为医用生物材料的应用,《基础医学与临床》1992年 第12 卷第6 期:30-32.
[2]李卫林,曹健,汤克勇,左锦静,王岩.胶原蛋白结构和稳定性关系研究.中国皮革,2005,34(23):14-16
[3]林崇韬,文胡实,孙宏晨等.乙酸溶解一酶消化法制备医用胶原膜[J].吉林大学学报(医学版),2004,30(1):75.78.
[4]王碧,林炜,马春辉,张铭让.皮革废弃物资源回用-胶原蛋白的利用基础、现状及前景。皮革化工,2001,18(3):10-14
[5]Donald W,Buck II a,Murad Alam,John YS Kim,Injectable fillers for facial rejuvenation:a review.Journal of Plastic,Reconstructive &Aesthetic Surgery(2009)62:11-18
[6]Neil S.Sadick,Cheryl Karcher,Laura Palmisano.Cosmetic dermatology of the aging face.Clinics in Dermatology 2009(27):S3–S12
[7]Stephen F.Badylak,Thomas W.Gilbert.Immune response to biologic scaffold materials.Seminars in Immunology 2008(20):109-116.
[8]Rohrich RJ,Rios JL,Fagien S.Role of new fillers in facial rejuvenation:a cautious outlook.Plast Reconstr Surg 2003;112:1899-1902.

