福多司坦片健康人体药动学研究
周 佳,李 珍*,杨武云,唐世新,闻 俊,范国荣,胡晋红*
(1.第二军医大学长海医院药学部,上海200433;2.第二军医大学药学院药物分析学教研室,上海200433)
福多司坦是一种新型祛痰药,为L-半胱氨酸衍生物,具有抑制炎症、修复黏膜、促进气管分泌的作用[1]。临床广泛用于呼吸道疾病的祛痰治疗[2]。基于福多司坦广泛的临床应用,对其药动学特点的了解很有必要。本研究应用建立的LC-MS/MS法测定血浆中福多司坦药物浓度,考察单次口服给药后,福多司坦在健康志愿者体内的药动学特征,为临床应用确定给药剂量和给药方案提供依据。
1 材料和方法
1.1 仪器和试药 VARIAN 1200L液相色谱-质谱联用仪,包括ProStar 210高压泵,ProStar 410自动进样器,1200L Quadrupole MS/MS仪,MS 6.3工作站(美国瓦里安公司)。XW-80A涡旋混合器(上海医科大学仪器厂),TGL-16G台式高速离心机和80-2B台式离心机(上海安亭科学仪器厂)。Millipore Simplicity 185超纯水系统(美国Millipore公司)。福多司坦对照品(批号030801,含量99.15%)由上海医药(集团)有限公司信谊制药总厂提供。试验药物福多司坦片[由无锡药明康德新药开发有限公司和上海医药(集团)有限公司信谊制药总厂联合研制,规格:200mg/片,批号:030901C],经检验合格,符合临床研究用药质量要求。甲醇(色谱纯,美国Merck公司),水为去离子水。
1.2 受试者选择 10例男性健康志愿者,年龄20~24岁,体重55~75kg,身高166~181cm。无心、肝、肾、消化道和血液系统等疾病史,且精神状态良好。经体检,血常规、尿常规、血生化、凝血酶原时间、粪常规(包括潜血)、心电图、胸片检查等合格。试验方案经第二军医大学长海医院伦理委员会审批同意,所有健康志愿者明了本试验的目的与要求,并自愿签署知情同意书。
1.3 试验方案 受试者于给药前1d入选并入住试验病房,给药前1d晚餐后开始禁食,给药当天早上7:00空腹口服400mg福多司坦片,用200ml温开水送服。服药2h后可以饮水,服药4h后进食统一低脂餐。于给药前及给药后的0.083、0.167、0.25、0.5、0.75、1、2、3、4、6、8、10、12h于肘静脉取血4ml,肝素抗凝,置一次性塑料离心管中,9×102× g离心10min,分取血浆1ml于-20℃冰箱保存至测定。血样采集及临床观察均在Ⅰ期病房中进行,由临床经验丰富的医师进行监护。试验期间受试者禁用含柑橘、柠檬类、葡萄柚汁类、咖啡因、乙醇或黄嘌呤等的饮料,避免剧烈运动及长时间卧床。
1.4 血药浓度测定
1.4.1 色谱分离条件 色谱柱:Diamonsil C18柱(200mm× 4.6mm,5μm,美国迪马公司);柱温30℃;流动相:甲醇-水(50∶50),采用等梯度洗脱方式;流速0.6ml/min;分流比3∶1;进样量20μl;分析时间6min。
1.4.2 质谱检测条件 采用ESI离子源、负离子检测,选择SRM工作方式进行一/二级质谱分析。质谱检测工作参数如下:福多司坦Q1(m/z)178、Q3(m/z)91;扫描时间1.0s,SIM宽0.7,Q1峰宽1.5;分析针4 500V、12μA;阀门压力600V、55psi;干燥气体380℃、21psi;毛细管35V,Q0 0.7V,L4 1.0V,Q1 1.0V;Q2碰撞能量12.0V,碰撞气体0.24Pa;负离子检测1 300V。在上述LC-MS/MS条件下测得福多司坦一/二级质谱及空白血浆、空白血浆添加对照品、实测血浆样品的典型谱图,见图1。

图1 血浆中福多司坦的LC-MS/MS谱图
1.4.3 血样预处理 静脉血样置于5.0ml塑料离心管中(肝素抗凝),9×102×g离心10min,分离血浆。取血浆100μl置于1.5ml塑料Eppendorf离心管中,加入300μl甲醇,涡旋振荡1min,于1.1×104×g高速离心10min。分取上清液250μl置于0.5ml塑料Eppendorf离心管中,于1.1×104×g二次离心4min。吸取上清液150μl,自动进样20μl进行LC-MS/MS分析。
1.4.4 标准曲线的制备 精密称取福多司坦对照品10.10mg,置于10.0ml量瓶中,加去离子水溶解并稀释至刻度,摇匀,即得1 010.0μg/ml的对照品贮备液。精密吸取对照品贮备液适量,用去离子水分别稀释定容至3个10.0ml量瓶中,配成浓度为101.00、10.10和1.01μg/ml的对照品溶液。从福多司坦对照品溶液中精密吸取相当于1.01、2.02、5.05、10.10、20.20、50.50、101.00μg福多司坦溶液置于7个10.0ml量瓶中,加入空白血浆稀释定容,配制成含福多司坦0.101、0.202、0.505、1.01、2.02、5.05、10.10μg/ml的标准血浆样品。按1.4.3项步骤操作,并进行LC-MS/MS分析。以福多司坦对照品的峰面积(A)对相应的浓度(c)进行线性回归,得福多司坦血浆标准曲线方程为:A=6.134 c-0.505 3, r=0.999 7(n=5),线性范围0.101~10.10μg/ml。本法测定血浆中福多司坦的最低定量浓度为0.101μg/ml(S/N>3)。1.4.5 回收率和精密度考察 (1)回收率实验 配制0.202、1.01、5.05μg/ml低、中、高3种不同浓度的福多司坦标准血浆样品,按1.4.3项下步骤操作,将血浆样品中福多司坦色谱峰面积代入血浆标准曲线,通过测得量与加入量的比值求得相对回收率。(2)精密度实验 取上述3种浓度的福多司坦血浆样品测定峰面积,每日制备随行标准曲线,从当日标准曲线上求算血浆样品的浓度,连续测定5d,再计算方法的日内和日间RSD,结果见表1。

表1 福多司坦的回收率与精密度实验结果(n=6)
2 结 果
2.1 血药浓度-时间曲线 10名健康志愿者单剂量口服400mg福多司坦片后,福多司坦血药浓度-时间曲线见图2。
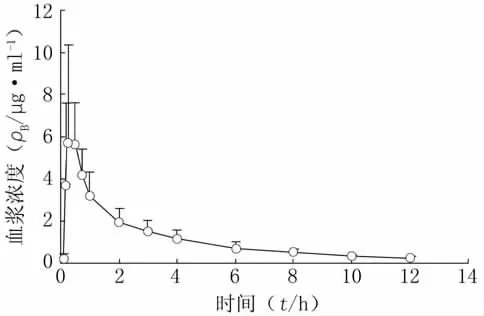
图2 单剂量口服400mg福多司坦片后平均血药浓度-时间曲线n=10
2.2 药动学参数 采用非房室模型(统计矩)法计算药动学参数,cmax和tmax采用实测值,梯型面积法计算药-时曲线下面积。10名健康志愿者单剂量口服400mg福多司坦片后体内福多司坦药-时曲线的末端相消除半衰期(t1/2)、平均驻留时间(MRT)、峰浓度(cmax)、达峰时间(tmax)、AUC0~12、AUC0~∞分别为(3.88±0.65)h、(4.50±0.75)h、(6.96±3.78)μg/ml、(0.4±0.2)h、(14.23± 4.99)μg·h·ml-1、(15.51±5.23)μg·h·ml-1。
3 讨 论
本研究采用甲醇沉淀蛋白质法预处理血浆样品,应用建立的LC-MS/MS法测定福多司坦在健康受试者体内血药浓度。通过测定单剂量口服福多司坦400mg后不同时间的血药浓度,对福多司坦在人体内的药动学规律进行了研究。研究结果显示,福多司坦在健康人体内主要药动学参数与文献报道[3,4]基本一致。通过本研究发现,福多司坦片口服给药后,约0.5h血浆中药物浓度即达峰值,3~4h后血药浓度即可下降50%。其口服吸收迅速、良好,临床用药起效快,半衰期较短,体内排泄较快。
[1] 陈 光.福多司坦的药理及临床试验[J].泰州职业技术学院学报,2009,9(6):35-38.
Chen Guang.Pharmacology and clinical trial of fudosteine[J].J Taizhou Polytech Coll,2009,9(6):35-38.In Chinese with English abstract.
[2] 张华峰,王健康,戴 博,等.高效液相色谱-串联质谱法测定人血浆中福多司坦的浓度[J].解放军药学学报,2010,26(2):156-157,164.
Zhang HuaFeng,Wang JianKang,Dai Bo,et al.Determination of fudosteine in human plasma by high performance liquid chromatography-tandem mass spectrometry[J].Pharm J Chin PLA,2010,26(2):156-157,164.In Chinese with English abstract.
[3] 张 红,胡 敏,熊玉卿,等.液质联用测定血中福多司坦浓度及其人体药动学[J].中国医院药学杂志,2008,28(16):1370-1373.
Zhang Hong,Hu Min,Xiong YuQing,et al.Determination of fudosteine in plasma and its pharmacokinetics by LC-MS[J].Chin Hosp Pharm J,2008,28(16):1370-1373.In Chinese with English abstract.
[4] 卢 姗,刘 伟,李晓红,等.人血浆中福多司坦的LC-MS/MS法测定[J].中国医药工业杂志,2009,40(5):365-367.
Lu Shan,Liu Wei,Li XiaoHong,et al.Determination of fudosteine in human plasma by LC-MS/MS[J].Chin J Pharmaceuticals,2009,40(5):365-367.In Chinese with English abstract.

