降低β-胡萝卜素配油粘度的工艺研究
沈仲兴 王 力 宋文祥 谭均华
(上虞新和成生物化工有限公司,浙江 上虞 312369)
β-胡萝卜素是类胡萝卜素之一,作为一种抗氧化剂,它是自然界中最普遍存在也是最稳定的天然色素,是维护人体健康不可缺少的营养素,在抗癌、预防心血管疾病、白内障及抗氧化上有显著的功能,并进而防止老化和衰老引起的多种退化性疾病,应用十分广泛,全球每年销量在400t以上。β-胡萝卜素可用植物提取法和化学合成法获取,受技术和条件所限,生物发酵法和植物提取法的产量较小[1-6],主流市场上使用的β-胡萝卜素主要为化学合成产品[7-9]。
β-胡萝卜素的主要剂型是含量为30%β-胡萝卜素植物油配油[10],作为一种广泛使用的食用油溶性色素,用于人造奶油、胶囊、鱼浆炼制品、素食产品、速食面的调色等方面。通过化学合成法制备的β-胡萝卜素30%配油,粘度在500~50000 CP之间波动。粘度大于6000 CP时,配油的流动性减弱,严重影响制剂化处理,因此控制粘度是一个基本要求。
随着材料学的发展,通过研究应力、应变、温度和时间等方面对物质变形和流动的关系逐渐衍生出一门交叉学科--流变学。流变学的研究认为分散体系中细颗粒的比例太高或太低都会增大浆体的粘度。这可从固液悬浮体系的机理作出解释,当细颗粒比例较低时,细颗粒不能完全充满粗颗粒之间的空隙,不能达到颗粒的紧密堆积,从而导致有效流动相的体积分数降低,最终引起料浆的流动性降低、粘度增大;或者当细颗粒比率较高时,未填充的细颗粒会进入有效流动相区,使得有效流动相的浓度和粘度都增大。因此料浆中颗粒的粒度是影响粘度的主要因素[11-13]。
晶体的粒度是在物相转变的情况下形成的晶体群特性。体系内由于温度或浓度的局部变化,外部撞击,或一些杂质粒子的影响,会导致体系内各处首先出现瞬时的微细结晶粒子,在这些微小晶粒的诱导下进行二次成核,生成更大的晶体,晶核形成后会在溶液的过饱和度的推动下进行晶体生长,生成更大的晶体。晶体的大小受瞬时微细结晶粒子、溶液的过饱和度、搅拌桨搅拌速度和反应釜的降温速度、晶体网面间距、网面对外来质点引力等因素影响[14]。
本实验是寻找影响30%配油粘度的主要因素,通过对原料、结晶过程的研究,分析原料及合成过程与粘度的联系,从而得到合适的合成工艺降低30%配油的粘度。
1 实验材料与仪器
1.1 原料和试剂
乙醇:分析纯,杭州化学试剂有限公司;
丙酮:分析纯,杭州化学试剂有限公司;
β-胡萝卜素成品:含量99.5%,上虞新和成生物化工有限公司研究所提供;
玉米油:江苏益海(泰州)粮油有限公司提供;
葵花籽油:龙兴粮油批发有限公司提供;
色拉油:北京日上综合商品批发市场有限公司提供;
半月盐:含量85%以上,为上虞新和成生物化工有限公司研究所提供;
C10二醛[15-17]:含量95%以上,为上虞新和成生物化工有限公司研究所提供;
甲醇钠:含量30%以上,东营凯越化工有限公司提供。
1.2 主要仪器
10万级电子分析天平:梅特勒-托利多仪器(上海)有限公司;
R206D旋转蒸发器:上海申生科技有限公司;
S212恒速搅拌器:上海申生科技有限公司;
气相色谱仪GC-2010:日本岛津;
紫外分光光度计Cary 50:美国瓦里安;
压滤机:诸城联创机械有限公司;
研磨机:鹤壁市天冠仪器仪表有限公司;
粘度计:上海衡平仪器有限公司;
激光粒度分析仪:济南润之科技有限公司。
2 实验方法
2.1 制备β-胡萝卜素结晶
采用化学合成法,以C15膦盐及C10二醛为原料,在甲醇钠存在下、在低温条件下发生缩合反应,反应液经热异构结晶,再经冷却结晶并过滤得β-胡萝卜素粗品,再经纯水洗涤、溶剂精制后处理并烘干得β-胡萝卜素晶体。
2.2 配制β-胡萝卜素30%配油
称取31g的β-胡萝卜素晶体,69g玉米油,在25℃下搅拌混合1h后,在25℃下使用研磨机研磨得到悬浮状的油性液体,要求在48h内沉淀物不超过总量的0.5%,8周内沉淀物不超过总量的1%。
2.3 粘度测试
在常压和25℃保温条件下,使用粘度计测量30%配油的动力粘度,要求读数在量程的25%~75%之间,单位为厘泊(CP)。
3 结果与分析
3.1 粒径与粘度
取12个不同粘度的β-胡萝卜素30%配油,使用激光粒度分析仪分析配油中的晶体粒度,并积分计算其平均粒径,将平均粒径与粘度对应后列入表1并做图。

表1 粒径与粘度
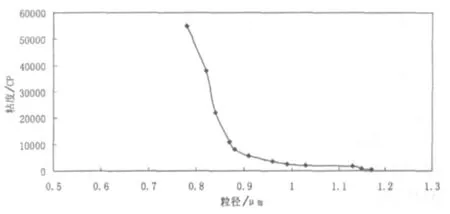
图1 粒径与粘度关系图
从图1可以看出30%配油的粘度与平均粒径成反比关系,即平均粒径越大则粘度越小。根据表1,在粘度小于5500 CP的30%配油,其中的晶体平均粒径大于0.91μm。
由于配油是由β-胡萝卜素晶体在植物油中配制研磨而成的,因此β-胡萝卜素晶体的粒径大于等于0.91μm才能研磨制备出5500 CP的配油,因此提高β-胡萝卜素晶体的平均粒径是降低配油粘度的方法之一。
3.2 影响粒径的因素分析
3.2.1 晶种对结晶的影响
人为的添加β-胡萝卜素晶体作为晶种,在异构结晶过程中诱导二次成核,生成更大的晶体,晶核形成后会在溶液的过饱和度的推动下进行晶体生长,生成更大的晶体。
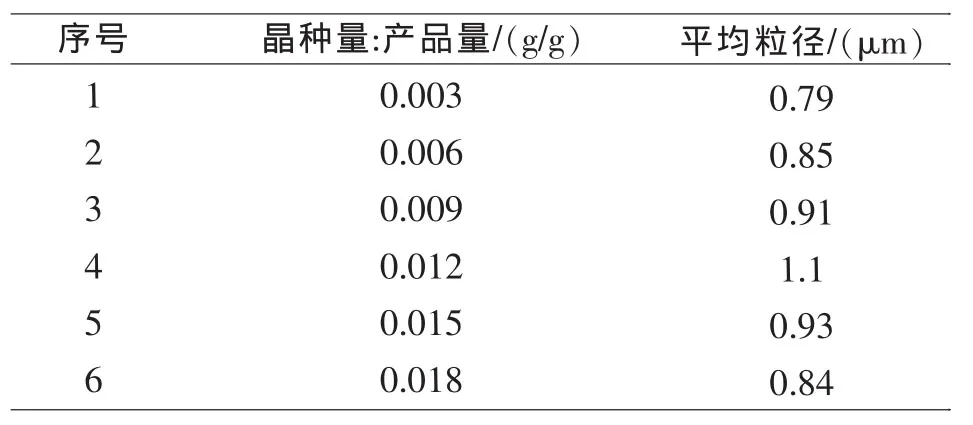
表2 晶种与平均粒径
由实验证明,加入适量晶种可以增大平均粒径,平均粒径的最大值出现在晶种加入量为0.009~0.015g/g之间。
3.2.2 搅拌强度对结晶的影响
搅拌的速度影响溶液的过饱和度、晶体碰撞强度和碰撞机率,造成晶体粒径的差异。为验证搅拌强度对晶体粒径的影响,本实验将同一批缩合反应液均分为6份,在不同强度的搅拌下进行热异构结晶和冷却结晶,并进行相同的后处理得到β-胡萝卜素晶体,进行粒度分析。实验结果如表3。
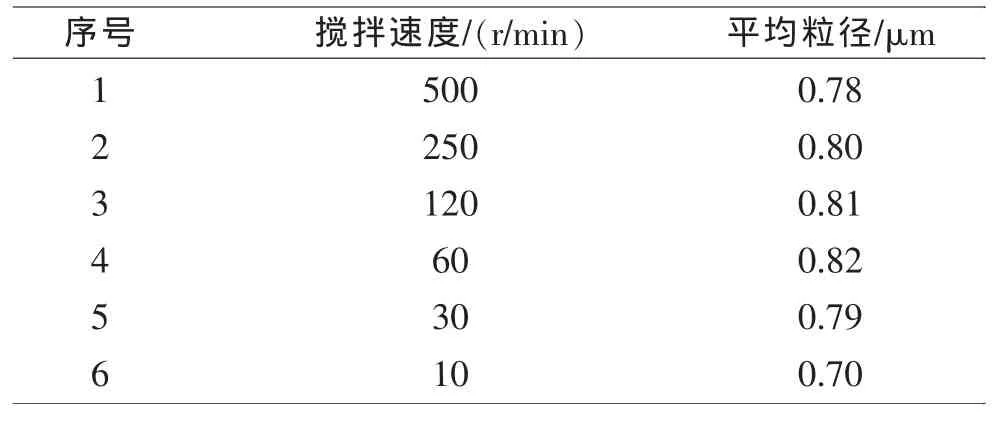
表3 不同搅拌速度与平均粒径
由实验证明,搅拌强度过大,溶液过饱和范围小,结晶中心少,二次成核少,粒径小;搅拌强度过小,晶体碰撞强度和碰撞机率小,二次成核少,粒径小。因此需要是适中的搅拌强度,才能取得较大的粒径。以上数据说明60r/min是合适的转速。
3.2.3 降温速度对结晶的影响
降温速度对二次成核和晶粒生长有影响,造成晶体粒径的差异。为验证搅拌强度对晶体粒径的影响,本实验投料将同一批缩合反应液均分为6份,在同样的条件下进行热异构结晶,在不同的降温速度下进行冷却结晶,并进行相同的后处理得到β-胡萝卜素晶体,进行粒度分析。实验结果如表4。

表4 不同冷却速度与平均粒径
由实验证明,较低的冷却速度,较长的冷却时间,溶液过饱和范围小,晶粒生长效果好。同时数据还表明,10℃~15℃∕h的降温速度已经可以保证晶体充分增大,过低的降温速度降低了反应的效率。
3.3 其他影响因素的分析
3.3.1 不同植物油的影响
市售β-胡箩卜素30%配油主要使用玉米油、葵花籽油、色拉油三种油配制,我们使用平均粒径为0.96μm的β-胡萝卜素分别在这三种油中配制配油。实验结果如表5。

表5 植物油种类与粘度
从实验结果看,玉米油、葵花籽油、色拉油对配油粘度的影响不大。
3.3.2 研磨时间的影响
我们使用平均粒径为1.13μm的β-胡萝卜素晶体,在不同的研磨时间下制备配油,完成研磨后测试粘度,配油静置48h检测沉淀物。实验结果如表6。

表6 研磨时间与粘度
从实验结果看,随着研磨的时间延长,晶体破碎较多,较细的颗粒数量增多,粘度逐渐增大。但是研磨时间较短的配油,有部分大颗粒由于粒径大而无法形成布朗运动,导致沉淀物增多,也不符合产品的使用标准。
4 优化实验方案
综合以上实验结论,得到最优实验条件为:
(1)在缩合反应液中加入0.01g/gβ-胡萝卜素晶体作为晶种进行异构结晶;
(2)热异构结晶和降温结晶中使用60r/min的搅拌转速进行搅拌;
(3)使用12℃/h的速度进行降温冷却结晶;
(4)配油研磨1.5h。
按照最优实验条件进行实验,实验结果如表7。

表7 验证实验数据表
实验数据说明优化是有效的,在最优条件下制备β-胡萝卜素30%配油,粘度可以下降至1800CP以下。
5 结论
配油粘度与配油中晶体的粒度有直接关系,通过调整结晶条件,提高全合成β-胡萝卜素晶体平均粒径,从而增大配油中的β-胡萝卜素晶体粒径,有效降低了配油粘度。
适量的晶种,适中的搅拌速度,稳定而适中的降温冷却速度,可以合成出平均粒径较大的β-胡萝卜素晶体,用该晶体配制配油中所含有的晶体颗粒也较大,因此配油的粘度小,制剂化性能好,可以更好的满足客户的需要。另外由于增大了晶体粒径,因此在使用不同种类的植物油配制配油时的粘度差异小,因此本工艺具有很好的原料适应性。
[1]刘云凤,邵斌.天然维生素和合成维生素的活性与标识[J].中国食品添加剂,2004(2):32-37.
[2]孙福征,刘广发,陈启伟,等.高产β-胡萝卜素杜氏藻类突变株的鉴定与分析[J].大连水产学院学报,2004,19(3):230-233.
[3]戴德慧,胡伟莲,吕圭源,等.生物合成法生产β-胡萝卜素发酵条件研究[J].食品科学,2008,29(2):247-251.
[4]刘月英,陈晓强,谢忠,等.产胡萝卜素酵母的筛选[J].工业微生物,2000,30(2):38-40.
[5]杜桂彩.不同培养条件对大肠杆菌工程菌产β-胡萝卜素的影响[J].食品科学,2008,29(7):272-276.
[6]张博,刘斌,郭强,等.微波辅助提取β-胡萝卜素工艺条件的研究[J].现代农业,2009(2):79-80.
[7]Ernst H.Recent advances in industrial carotenoid synthesis[J].Pure and Appl Chem,2002,74(8):1369-1382.
[8]Isler O.History and industry application of carotenoids and vitamin A[J].Pure and Appl Chem,1979,51(4):447-462.
[9]Hoffmann F.Novel pentenyne derivatives and a process for the manufacture thereof:GB,866691A[P].1959-02-06.
[10]程建华,郝文川.分光光度法测定植物油中β-胡萝卜素[D].商务部四川粮食贮藏研究所,2011:49.
[11]陆明盛,微观-流变学的方法与技术[J].药学进展,1963,(14):63-64.
[12]McKenna B M,David Kilcast.Texture in food[M].Cambridge:Woodhead Publishing,2000:130.
[13]江体乾.化工流变学[M].上海:华东理工大学出版社,2004:54.
[14]Mullin J W.Crystallisation[M].London:Butter-worths,1972.
[15]Ernst H.Recent advances in industrial carotenoid synthesis[J].Pure and Appl Chem,2002,74(8):1369-1382.
16]Isler O.History and industry application of carotenoids and vitamin A[J].Pure and Appl Chem,1979,51(4):447-462.
[17]Hoffmann F.Novel pentenyne derivatives and a process for the manufacture thereof:GB,866691A[P].1959-02-06.

