基于硫酸根自由基的高级氧化技术深度处理造纸废水的研究
郭 鑫 马邕文, 万金泉, 王 艳 黄明智
(1.华南理工大学轻工与食品学院,广东广州,510640;2.华南理工大学环境科学与工程学院,广东广州,510006)
随着水资源的紧缺以及GB3544—2008 制浆造纸工业水污染物排放标准的颁布和实施,使得许多造纸企业现有的废水处理及排放水平面临不达标的困境。经过二级生化处理的造纸废水仍存在COD偏高、色度较大等问题,因此需对其进行深度处理以保证达标排放甚至回用。
高级氧化法在处理有毒有害及难降解有机废水中极具应用潜力。许多研究利用激发产生氧化性极强的羟基自由基破坏有机物分子结构,例如Fenton氧化[1]、光-Fenton 氧化[2]、TiO2光催化氧化[3]等来降解造纸废水中的有机物。
近年来,基于硫酸根自由基 (SO4-·)的高级氧化法降解废水中难降解有机物的研究开始发展起来。过硫酸钠 (PS)因其氧化性强、室温下稳定性高、水溶性好、价格相对较低等优点得到了很大关注。但因其室温下稳定的特点,仅依靠PS氧化降解有机物很难达到理想的效果,需要激发其产生SO4-·来降解有机物。目前,激发PS产生SO4-·的方式主要有热活化、光照、超声波活化、微波活化、过渡金属活化等[4-5]。
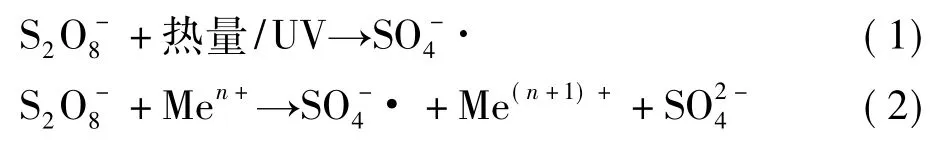
Huang[6-7]、Liang[8]、Waldemer[9]、Yang[10]等人通过热活化PS降解苯、甲苯、苯乙烷、甲基叔丁基醚、酸性橙AO7等物质发现降解率随温度的升高而增大,且一级动力学常数也随之增大;Lee等人[11]通过微波加热分解和零价铁 (ZVI)联合活化PS降解全氟辛酸铵时,发现有机物断裂成短链且具有脱氟的效果;Rasoulifard[12]、Bougie[13]等人也在加热活化方面进行了一些研究。
过渡金属离子活化PS的报道也有许多。Zhang等人[14]通过S2O28-派生氧化法催化降解水中甲基橙时发现 S2O28-/Ag+体系同Fenton氧化一样可以促使有机物矿化;Gayathri等人[15]通过钴离子活化产生SO4-·降解染料时亦可以得到良好的矿化效果。
Fe2+作为自然界中广泛存在的金属离子,在高级氧化技术中应用普遍。Liang[16]、Zhao[17]等人通过Fe2+活化PS降解三氯乙烯、4-氯酚、多氯联苯等难降解有机物时发现经Fe2+活化后的PS具有更好的效能。但有报道称[18],Fe2+与PS反应极快且SO4-·的半衰期又极短,导致反应很快停止;另外也有报道称[19-21],溶液中过高浓度的Fe2+会和有机物竞争消耗SO4-·,两者共同限制了活化的PS对污染物的降解效率。为了使Fe2+的浓度得到控制,一些研究用ZVI作为 Fe2+的产生源来替代 Fe2+活化 PS。Oh[22]、Kusic[23]、Zhang[24]等通过 ZVI活化 PS 产生 SO4-·降解偶氮染料RR45、二硝基甲苯、酸性橙AO7时发现ZVI可以缓慢释放可溶性Fe2+并附着在其表面,活化PS产生SO4-·,反应方程式 (3) 和式 (4)[22]。
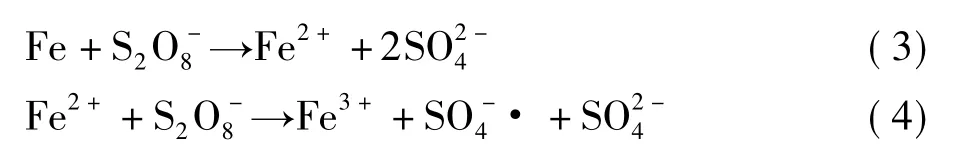
本实验以实际产生的造纸废水二级生化出水为研究对象,利用ZVI活化PS,考察了ZVI活化降解过程中各因素对降解效果的影响及降解过程的动力学模式,并通过气相色谱-质谱联用仪 (GC-MS)对处理前后废水中污染物质成分进行了定性定量分析,以寻找一种良好的深度处理方法并将其优化及应用。
1 实验
1.1 材料
废水取自广州市某造纸厂废水生化处理曝气池出水。主要水质指标见表1。

表1 废水主要水质指标
试剂:PS、还原铁粉、七水合硫酸亚铁,天津市科密欧化学试剂有限公司;浓硫酸,广州市东红化工厂;氢氧化钠,南京化学试剂有限公司;二氯甲烷,天津百世化工有限公司;无水硫酸钠,天津百世化工有限公。
仪器:Agilent7890A/5975C(U.S.A)型气相色谱-质谱联用仪;Unic UV-2100紫外/可见分光光度计;韶关明天COD微波消解仪;Mettler Toledo Seven Go pH计;电子分析天平。
1.2 实验方法
取100 mL废水样于250 mL锥形瓶中,用稀硫酸(10%)调节pH值,加入一定量的还原铁粉,然后快速加入氧化剂 (PS),急速混合并开始计时。到设定的时间取出一定量的废水样加入NaOH溶液调节pH值至9.0~9.5以终止反应。然后在3500 r/min下离心30 min,取上清液留待检测。实验均在室温下进行,通常情况下反应3 h,每组实验至少做两个平行。
1.3 分析方法
废水样CODCr用韶关明天COD微波消解仪加热至160℃消解25 min,待冷却后用回流滴定法计算废水样CODCr值,计算CODCr降解率。
采用Unic UV-2100紫外可见分光光度计测定废水样在350~600范围内的吸光度[25-26],并通过origin8.5拟合求其峰面积,通过峰面积与色度的换算公式求出色度值,计算其色度去除率。通过色度标准曲线得出扫描面积与色度换算公式:
B=8.6691Abs+4.1538
式中,B为所检测废水的色度,Abs为检测废水在350~600 nm的扫描面积。
废水处理前后污染物质成分变化情况通过Anglent GC-MS进行分析。色谱条件:色谱柱为DB-5毛细管柱 (30 m×0.25 mm×0.25 μm);载气 (He)1 mL/min;分流比10∶1;进样口温度230℃;进样量1 μL;升温程序为40℃ (保持3 min)→200℃ (5℃/min,保持 3 min) →280℃ (10℃/min,保持 4 min),溶剂延迟4 min。
质谱条件:电子轰击源 (EI),轰击电压70 eV,电子倍增电压1.2 kV,质量扫描范围33~500 amu,检索谱库为Nist08谱库,溶剂延迟4 min。
废水样预处理:量取废水样60 mL,不调节pH值,用60 mL二氯甲烷萃取,用力振荡5~10 min,静置,将二氯甲烷分离,调节pH值为中性,在中性条件下萃取1次,再调节pH值为碱性,在碱性条件下萃取1次,最后调节pH值为酸性,在酸性条件下再萃取1次,合并有机相,加入适量无水硫酸钠吸收萃取液中的水分,在旋转蒸发仪上将萃取液浓缩到1 mL左右。用0.45 μm的滤膜过滤,并装入色谱瓶中留待检测。
2 结果与讨论
2.1 pH值的影响
调节初始pH值分别为3、7、10进行实验,分别考察pH值对废水CODCr降解率及色度去除率的影响。实验结果如图1所示。
由图1可以看出,CODCr的降解率和色度的去除率皆随pH值的升高而降低。在pH值为3时降解效果最好,CODCr降解率和对降解率色度去除率分别达到了41.4%和83.5%,当pH值逐渐升高时,降解效果变差,pH值>7时下降趋势骤然增大,pH值从7升高到10时,CODCr降解率从39.3%降到27.3%,而色度去除率减少尤为明显,从83.0%减少至18.5%。这说明了SO4-·降解有机物的pH值范围为酸性至中性,酸性条件更有利于 SO4-·的生成。据报道[5],S2O28-非催化反应的活化能是140.0 kJ/mol,而酸催化反应的活化能仅为108.8 kJ/mol。这也证实了本实验的结果。碱性条件下有一定的降解率但效率不高,是由于酸性条件易生成SO4-·而碱性条件易生成羟基自由基[27],反应方程如式 (5)所示。有报道称[7],碱性条件下降解效率低可能是由于SO4-·和羟基自由基会与溶液中的OH-反应导致活性物种的快速淬灭,因而碱性条件下抑制了有机物的降解。
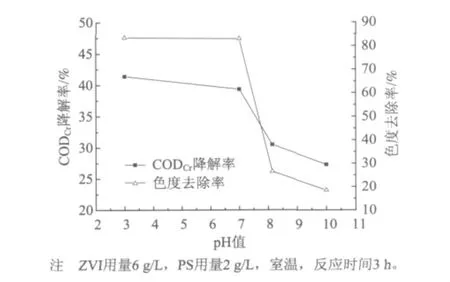
图1 pH值对CODCr降解率和色度去除率的影响

2.2 ZVI用量的影响
PS用量为2 g/L,在pH值为3和不调节pH值的条件下分别设定 ZVI用量为2、4、6、8、10和12 g/L,室温条件下反应 3 h,考察 ZVI用量对CODCr降解率及色度去除率的影响。
室温下,ZVI用量对CODCr降解率及色度去除率的影响如图2所示。在未调节生化出水pH值和调节初始pH值为3时,CODCr的降解率和色度的去除率皆随ZVI用量的增加而升高。当ZVI用量从2 g/L增加到8 g/L时,CODCr的降解率分别从未调节初始pH值时的5.3%和初始pH值为3时的14.5%上升到16.1%和63.0%,而色度的去除率从未调节初始pH值时的43.0%和初始pH值为3时的24.5%上升到85.0%和66.0%。当ZVI用量继续增加时,CODCr降解率和色度去除率皆出现下降趋势。这表明适量的ZVI会促进有机物的降解,ZVI过量时会对降解起到抑制作用。有研究证明[11],过量的Fe2+会与有机物竞争消耗SO4-·,从而抑制有机物的降解,反应方程如式 (6)所示。因此,当体系中ZVI用量≥10 g/L时,Fe2+的释放速度过快从而抑制了有机物的降解。
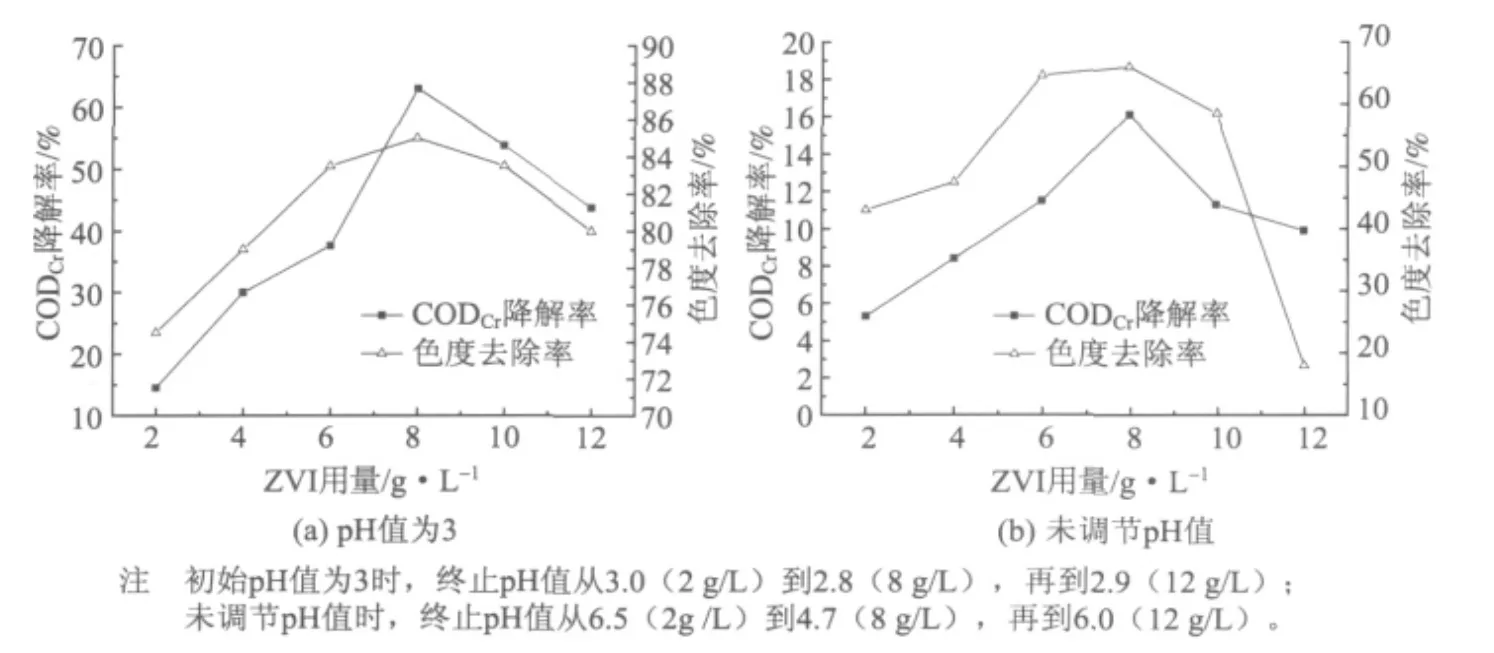
图2 ZVI用量对CODCr降解率和色度去除率的影响
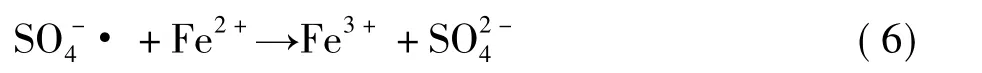
因此,适量的ZVI能够有效地活化PS产生SO4-·降解有机物。综合考虑ZVI用量和CODCr降解率及色度去除率的关系选取 ZVI用量为8 g/L进行后续实验。
2.3 PS用量的影响
ZVI用量恒定为8 g/L,在pH值为3和不调节pH值的条件下分别设定PS用量分别为0.2、0.5、1、2、3、4和5 g/L,室温条件下反应3 h,考察PS用量对CODCr降解率和色度去除率的影响。
1 mg/L CODCr理论需O2质量浓度为1 mg/L,每12 mol S2O2-8分解产生约1 mol O2,则1 mg/L CODCr所需S2O2-8约为12 mg/L。本实验处理废水CODCr为160 mg/L,因此理论上,当PS用量约为2 g/L时,投加的PS刚好氧化所有CODCr,但由于体系中存在竞争消耗氧化剂的物质,因此实际CODCr降解率是低于100%的。室温时,PS用量对CODCr降解率及色度去除率的影响如图3所示。由图3可见,随PS用量的增加,CODCr降解率及色度去除率都随之增加。从图3(a)可以看出,在pH值为3时,CODCr降解率从PS用量为0.2 g/L时的14.1%增加到PS用量为1 g/L时的38.5%,再增加到4 g/L时的57.5%,之后增加幅度不再明显。而在未调节pH值的条件下,图3(b)显示PS用量从0.2 g/L增加到1 g/L时,CODCr的降解率从0.9%升高到12.2%,继续增加到4 g/L时,CODCr的降解率升高到34.2%,再继续增加PS用量,CODCr降解率仍在升高。这说明了酸性条件可能更易产生有效的SO4-·,而碱性条件下SO4-·需转化成·OH-再进入反应,并且碱性条件下溶液中的OH-会和有机物竞争消耗自由基,因此导致在未调节pH值的弱碱性条件下需要更长的反应时间才能达到和酸性条件下同样的降解效果。
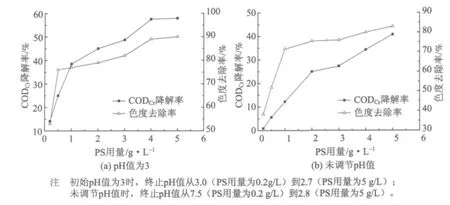
图3 PS用量对CODCr降解率及色度去除率的影响
图3同样显示了色度的去除率随PS用量增加的变化规律。在未调节pH值和pH值为3的条件下,色度去除率分别从PS用量为0.2 g/L时的38.3%和53.0%升高到PS用量为1 g/L时的71.5%和77.0%,继续增加PS用量到4 g/L时,色度的去除率分别达到80.0%和89.0%,之后再增加PS用量,pH值为3时去除率的升高趋势趋于平缓,而未调节pH值时的色度去除率仍在继续增加。考虑到适宜的氧化剂用量可以降低使用成本,因此在未调节pH值和pH值为3时都选取PS用量为4 g/L来进行后续实验。
2.4 降解过程动力学
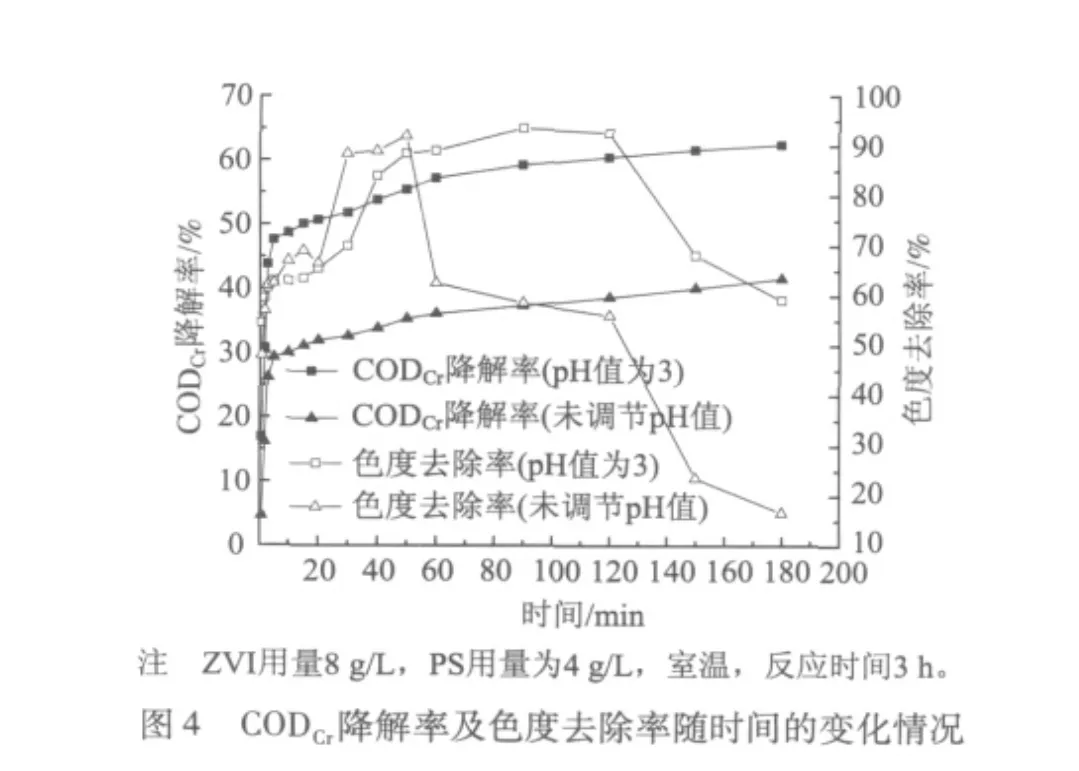
为了揭示SO4-·深度处理造纸废水的降解过程,图4和图5分别考察了在180 min内未调节pH值和pH值为3时CODCr降解率和色度去除率随时间的变化状况及其动力学模式。
从图4可以看出,CODCr降解率随着时间的增加而增加,前3~5 min反应速率很快,之后趋于缓慢。而色度去除率分别在90 min和50 min时达到顶峰然后开始逐渐减少。这是由于Fe2+在生成过程中不断被氧化成Fe3+呈现出黄色,导致色度增加。
ZVI活化PS降解CODCr的反应前3~5 min符合一级动力学反应模式,而第二阶段经过对数据的多次拟合,皆认为其符合二级动力学方程。由图4及图5可以看出,在反应的第一阶段,反应速率很大,仅在3 min时,pH值为3和未调节pH值的条件下CODCr降解率就分别达到了43.8%和26.1%。在反应的第二阶段,由于第一阶段S2O28-的大量消耗,使得第二阶段SO4-·的量急剧减少,加之第二阶段Fe2+的持续生成 (如图6所示),使得过量的Fe2+与有机物竞争消耗SO4-·,共同导致了反应趋势变得平缓,反应速率骤减。其理论也可认为同Bass-mann的高价铁理论[28]相似。Bossmann指出:Fenton试剂氧化反应羟基自由基反应机理为二级动力学反应,而高价铁Fe(VI)反应机理为一级动力学反应。
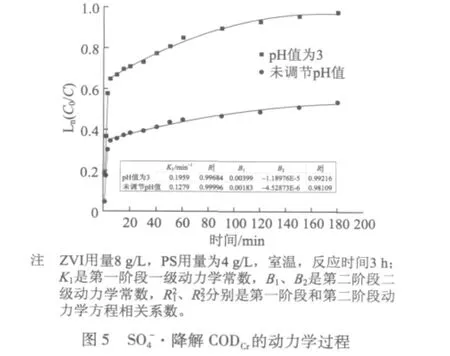
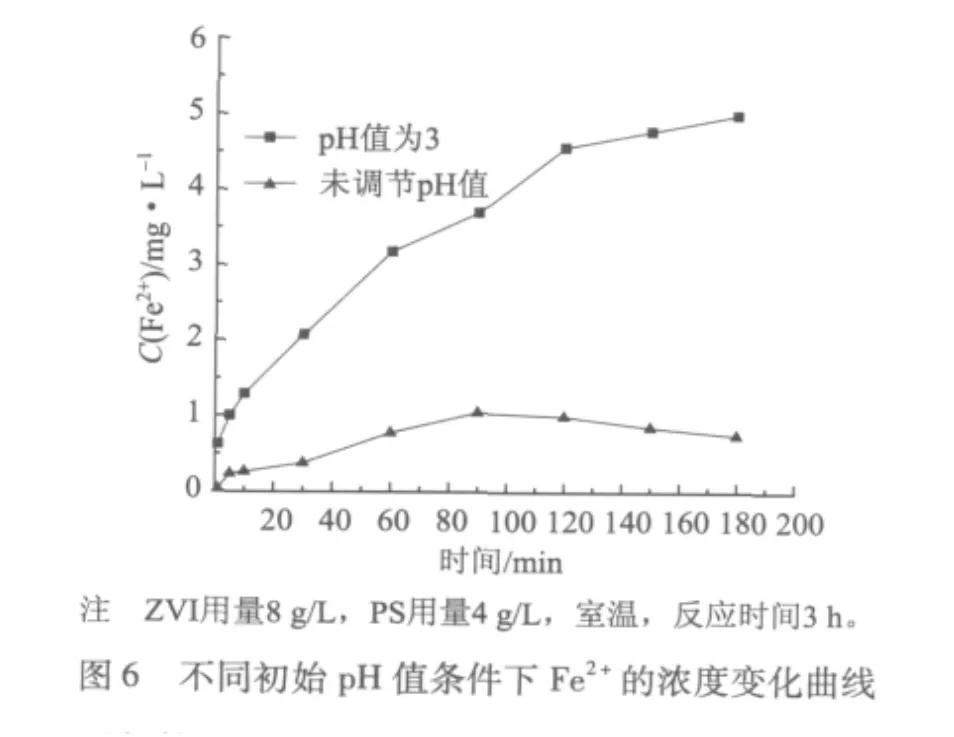
两段的动力学速率常数如图5中内嵌表所示。在初始pH值为3和未调节pH值时第一阶段反应速率常数分别是第二阶段反应速率常数的49倍和70倍。
2.5 处理前后废水中有机污染物的变化
分别对二级出水水样和经过SO4-·氧化降解处理过的水样通过GC-MS气质联用仪检测,检测结果如表2所示。
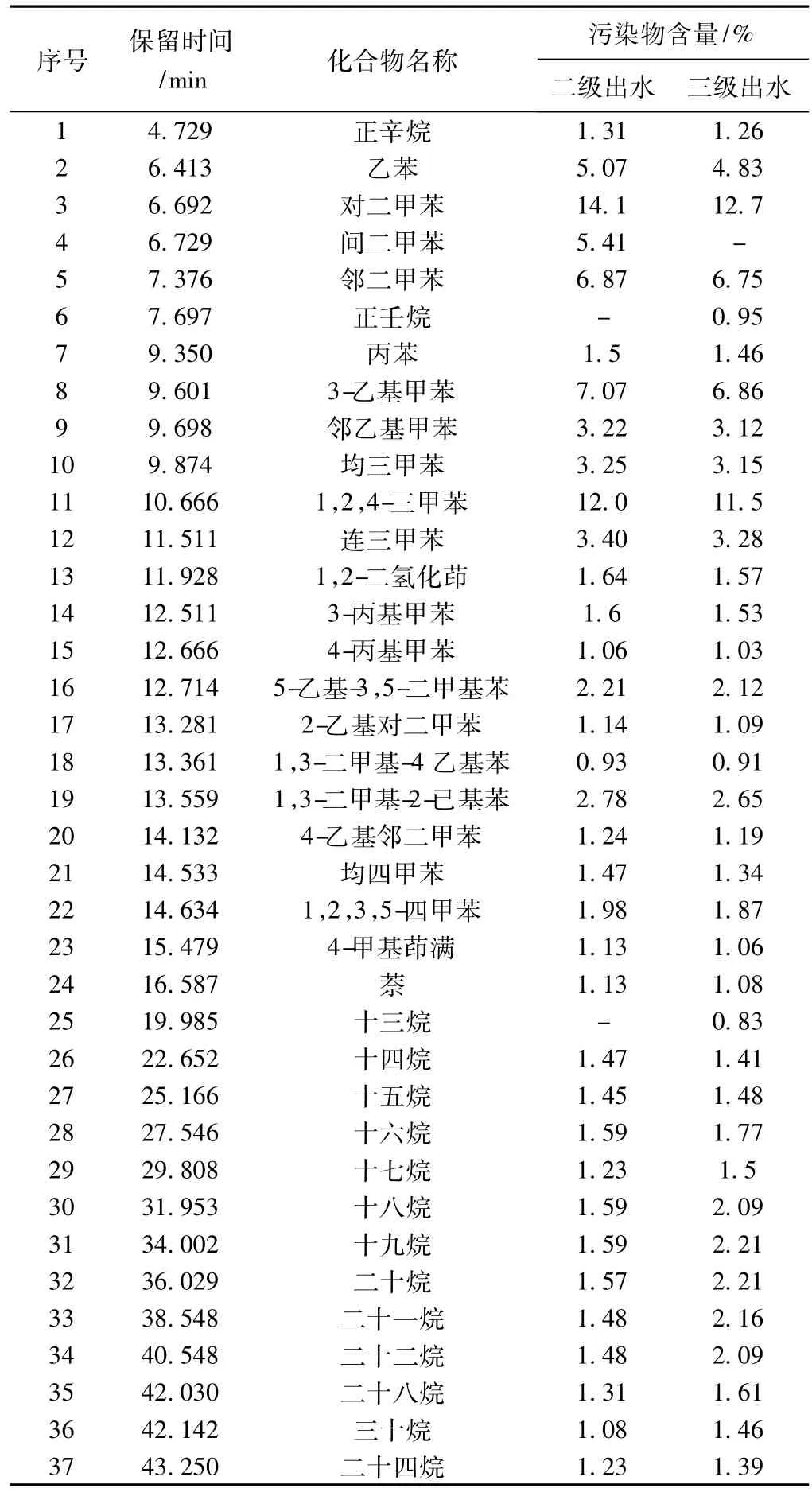
表2 造纸废水二级出水经高级氧化处理前后污染物的变化
从表2可以看出,造纸废水二级生化出水的难降解有机物多为带苯环的物质和长链烷烃类物质。经过SO4-·氧化降解后,废水中苯类物质得到了一定的降解,相对含量有一定的变化,种类基本没变。这可能是由于各种有机污染物竞争消耗SO4-·的结果。烷烃类物质种类及含量明显增加,表明污染物得到了进一步的氧化降解。
3 结论
3.1 硫酸根自由基 (SO4-·)在酸性至中性条件下皆能有效降解造纸废水中的有机污染物。CODCr降解率及色度去除率都随着pH值的升高而降低,在pH值为3时的效果最好。
3.2 在室温条件下,适量的零价铁 (ZVI)可以有效活化过硫酸钠 (PS)产生SO4-·,进而氧化降解废水中有机污染物。当ZVI用量为8 g/L时,处理效果最佳。
3.3 室温下,CODCr的降解率和色度的去除率随氧化剂用量的增加而增加,但达到适宜用量后开始趋于平缓。因此,适量地投加氧化剂不仅可以有效降解有机物,而且可以降低成本。
3.4 降解动力学表明,ZVI活化PS降解造纸废水有机污染物的过程是分两个阶段进行的,第一阶段(前3~5 min)是快速反应阶段,此阶段符合一级动力学过程;第二阶段 (5 min后)是二级动力学过程,此阶段反应趋于缓慢。
3.5 SO4-·氧化降解前后废水污染物变化说明SO4-·能有效降解造纸废水生化出水中难降解的有机污染物,苯类物质相对含量降低和烷烃类物质的明显增加表明污染物得到了有效的氧化降解。
[1] Liang X L,Zhong Y H,Zhu S Y,et al.The decolorization of Acid Orange II in non-homogeneous Fenton reaction catalyzed by natural vanadium-titanium magnetite[J].Journal of Hazardous Materials,2010,181(1/3):112.
[2] Duran A,Monteagudo J M,Amores E.Solar photo-Fenton degradation of Reactive Blue 4 in a CPC reactor[J].Applied Catalysis B-Environmental,2008,80(1/2):42.
[3] Bansal A,Divya N,Jana A K.Performance of Titania based Nano-Photocatalysts on the Degradation of Orange G azo dye[J].Recent Advances in Energy and Environment,2010:140.
[4] House D A.Kinetics and mechanism of oxidation by peroxydisulfate[J].Chem.Review,1962,62:185.
[5] Kolthoff I M,Medalia A I,Raaen HP.The reaction between ferrous iron and peroxides.IV.Reaction with potassium persulfate[J].J.Am.Chem.Soc.,1951,73:1733.
[6] Huang K C,Zhao Z Q,Hoag G E,et al.Degradation of volatile organic compounds with thermally activated persulfate oxidation[J].Chemosphere,2005,61(4):551.
[7] Huang K C,Couttenye R A,Hoag G E.Kinetics of heat-assisted persulfate oxidation of methyl tert-butyl ether(MTBE)[J].Chemosphere,2002,49(4):413.
[8] Liang C J,Bruell C J.Thermally activated persulfate oxidation of trichloroethylene:Experimental investigation of reaction orders[J].Industrial& Engineering Chemistry Research,2008,47(9):2912.
[9] Waldemer R H,Tratnyek P G,Johnson R L,et al.Oxidation of chlorinated ethenes by heat-activated persulfate:Kinetics and products[J].Environmental Science & Technology,2007,41(3):1010.
[10] Yang S Y,Wang P,Yang X,et al.Degradation efficiencies of azo dye Acid Orange 7 by the interaction of heat,UV and anions with common oxidants:Persulfate,peroxymonosulfate and hydrogen peroxide[J].Journal of Hazardous Materials,2010,179(1/3):552.
[11] Lee Y C,Lo S L,Chiueh P T,et al.Microwave-hydrothermal decomposition of perfluorooctanoic acid in water by iron-activated persulfate oxidation[J].Water Research,2010,44(3):886.
[12] Rasoulifard M H,Mohammadi S M,Mahdi D,et al.Desalination And Water Treatment,2011,28(13):115.
[13] Bougie S,Dube J S.Oxidation of dichlorobenzene isomers with the help of thermally activated sodium persulfate[J].Journal of Environmental Engineering And Science,2007,6(4):397.
[14] 张乃东,张曼霞,胡永臻.S2O28-派生氧化法催化降解水中的甲基橙[J].催化学报,2006,27(5):445.
[15] Gayathri P,Praveena Juliya Dorathi R,Palanivelu K.Sonochemical degradation of textile dyes in aqueous solution using sulphate radicals activated by immobilized cobaltions[J].2011,17(3):566.
[16] Liang C J,Bruell C J,Marley M C,et al.Persulfate oxidation for in situ remediation of TCE.I.Activated by ferrous ion with and without a persulfate-thiosulfate redox couple[J].Chemosphere,2004,55(9):1213.
[17] 赵进英,张耀斌,全 燮,等.加热和亚铁离子活化过硫酸钠氧化降解4-CP的研究[J].环境科学,2010,31(5):1233.
[18] 杨世迎,杨 鑫,王 萍,等.过硫酸盐高级氧化技术的活化方法研究进展[J].现代化工,2009,29(4):13.
[19] Cao J S,Zhang W X,Brown D G,et al.Oxidation of lindane with Fe(II)-activated sodium persulfate[J].Environmental Engineering Science,2008,25(2):221.
[20] Oh S Y,Kim H W,Park J M,et al.Oxidation of polyvinyl alcohol by persulfate activated with heat,Fe2+,and zero-valent iron[J].Journal of Hazardous Materials,2009,168(1):346.
[21] Stefansson A.Iron(III)hydrolysis and solubility at 25 degrees[J].Environmental Science& Technology,2007,41(17):6117.
[22] Oh S Y,Kang S G,Chiu P C.Degradation of 2,4-dinitrotoluene by persulfate activated with zero-valent iron[J].Science of the Total Environment,2010,408(16):3464.
[23] Kusic H,Peternel I,Koprivanac N,et al.Iron-Activated Persulfate Oxidation of an Azo Dye in Model Wastewater:Influence of Iron Activator Type on Process Optimization[J].Journal Of Environmental Engineering-ASCE ,2011,137(6):454.
[24] 张成,万金泉,马邕文,等.加热与零价铁活化S2O2-8氧化降解偶氮染料AO7的研究[J].环境科学,2011,32(10):2949.
[25] 李海明,何北海,陈元彩,等.制浆造纸工业废水色度的检测方法及其应用研究[J].中国造纸,2006,25(7):23.
[26] 国家环保局.水和废水监测分析方法[M].3版.北京:中国环境科学出版社,l 989.
[27] Guan Y H,Ma J,Li X C,et al.Influence of pH on the Formation of Sulfate and Hydroxyl Radicals in the UV/Peroxymonosulfate System[J].Environ.Sci.Technol.,2011,45:9308.
[28] Bossmann Stefan H,Oliver Esther,et al.New Evidence against Hydroxyl Radicals as Reactive Intermediates in the Thermal and Photochemically EnHanced Fenton Reactions[J].J.Am.Chem.Soc.,1998,102:5542.

