手性铜试剂在羰基化合物加成反应中的应用
潘明翔 王 维 裴 文
(浙江工业大学化学工程与材料学院,杭州 310014)
综 述
手性铜试剂在羰基化合物加成反应中的应用
潘明翔 王 维 裴 文*
(浙江工业大学化学工程与材料学院,杭州 310014)
介绍了有机铜试剂具有价格低廉、毒性小、配位能力好等的优点,总结了有机铜试剂在不饱和羰基化合物的不对称共轭加成反应中的应用,特别是催化不饱和酯、硫酯、砜、醛和酮等α,β-不饱和羰基化合物的不对称共轭加成反应,提出了手性铜试剂催化不对称共轭加成反应在底物选择上仍然具有一定的局限性,该反应的底物主要集中于酮类化合物,而砜类和醛类化合物报道较少,认为探索出适应性广泛的手性铜催化剂配体将成为研究重点,同时,为了研究新的手性铜催化剂,应该不断深入地研究反应机理。
手性铜试剂;共轭加成反应;羰基化合物
手性铜试剂在不对称共轭加成反应中的应用受到了人们的高度关注,而不对称共轭加成反应是有机合成中的重要反应之一[1]。1941年,Kharash等人首次报道了利用有机铜试剂催化的格式试剂与羰基化合物进行的加成反应[2]。Lippard等人在1988年由环己烯酮进行不对称共轭加成,制得了2-取代的环己酮[3]。
有机铜试剂具有价格低廉、毒性小、配位能力好等优点,近年来,其研究得到了广泛的应用[2]。本文对有机铜试剂催化不饱和酯、硫酯、砜、醛和酮等α,β-不饱和羰基化合物的不对称共轭加成反应进行了综述,以期为化学工作者在今后的研究中具有较好的参考价值。
1 与酯的反应
2007年Beatriz MaciaĀ Ruiz等人使用双二苯基磷酰联萘(Tol-BINAP)/CuI催化 RMgBr和 α,β-不饱和硫代酸酯,尤其是不饱和的脂肪族的硫代酸酯得到了较好的对映选择性(对映选择性ee为99%)[4]:其中,R 为芳基、烃基,R1=甲基、乙基;t-BuOMe为甲基叔丁基醚,Me为甲基。
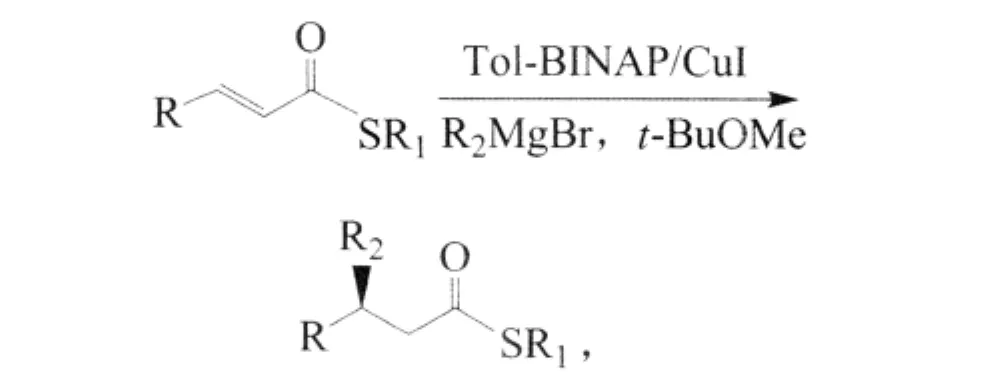
更重要的是,Tol-BINAP/CuI催化许多种格式试剂包括相对不活泼的MeMgBr和位阻较大的格式试剂,并且位阻较大的格式试剂在芳香族和脂肪族的α,β-不饱和硫代酸酯的1,4-加成中获得了很好的对映选择性。
2010年Jack Chang Hung Lee和Dennis G Hall报道了铜催化的含有硼原子的不饱和酯和硫代酸酯的反应(收率为 82%,ee为 98%)[5]:
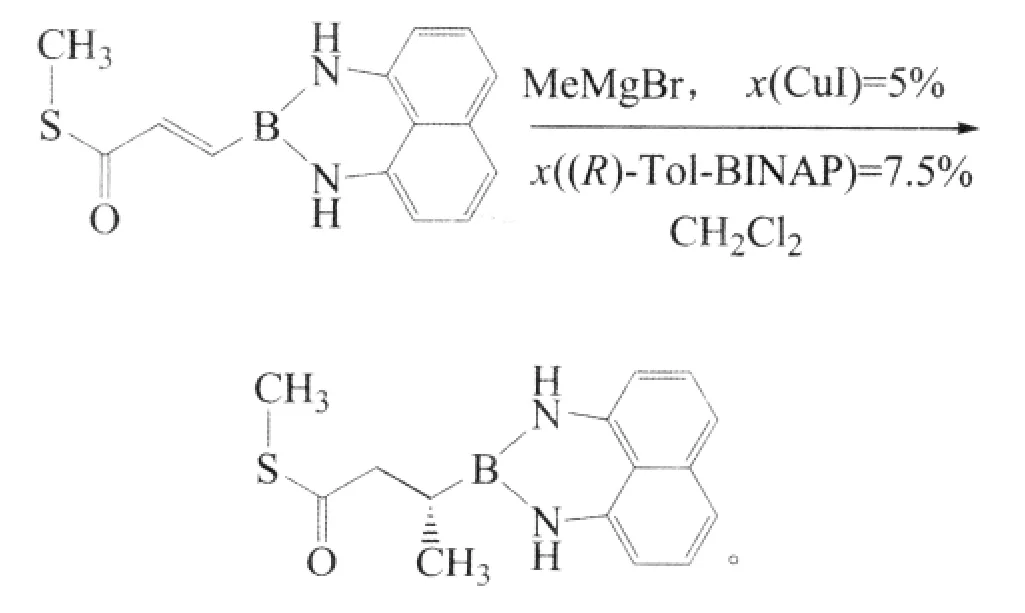
通过条件优化实验发现Tol-BINAP是最合适的双膦配体,CuI是最有效的铜试剂,格式试剂MeMgBr和PhMgBr使得甲基硫代酸酯的衍生物的收率和对映选择性都有所提高。
2 与砜的反应
2008年Pieter H Bos等人使用CuCl/Tol-BINAP催化格式试剂用于α,β-不饱和的2-哌啶砜(产率为97%,ee 为 94%)[6]:
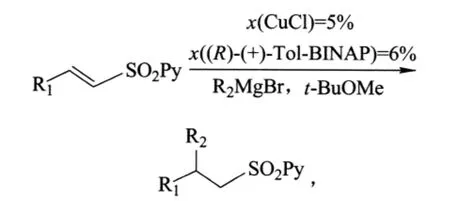
其中,R1、R2为烃基;Py 为吡啶。
这种方法广泛适用于脂肪族类化合物,产率为88%~97%,ee为88%~94%。
3 与醛和酮的反应
Tomiok等自1992年起,报道了一系列关于脯氨酸衍生膦配体的研究用于铜催化的α,β-不饱和酮化合物的不对称共轭加成反应中,反应在-78℃进行,得到了82%的收率和92%的选择性[7-9]:
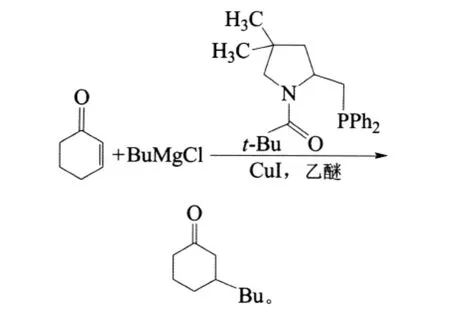
其中,t-Bu为叔丁基,Bu为丁基,Ph为苯基。
2008年Yasumasa Matsumoto等人应用对称的手性氮杂环卡宾做配体,铜试剂催化3-取代的环酮[10]:

Cu(OTf)2为三氟甲磺酸铜,EeMgBr为溴乙烷的格式试剂。
他们通过合成不同的氮杂环卡宾做配体进行筛选,当Cu(OTf)2的摩尔分数为6%,温度在0℃、反应时间在0.5 h时,收率为98%,ee为80%。
虽然对铜催化的环状酮的研究已经比较广泛,但是非环状酮的反应条件仍受到限制,因此,Beatriz Macia′等人使用亚磷酰胺做配体,有机铜试剂催化非环状的 α,β-不饱和酮[11]:
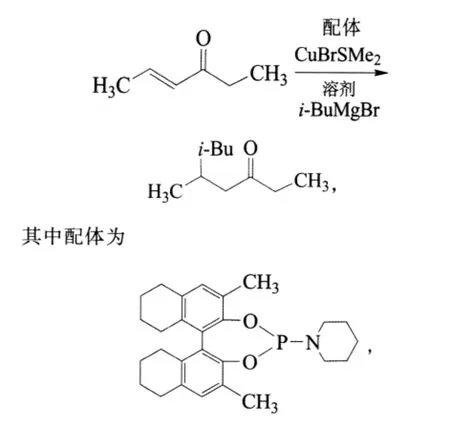
i-BuMgBr为溴异丁烷的格式试剂,i-Bu为异丁基。
试验不同种的格式试剂用于脂肪族和芳香族的非环状酮类化合物,反应温度在-30℃、时间为1 h下,均得到较好的收率和对映选择性。
2009 年 Laëtitia Palais和 Alexandre Alexakis报道了使用单膦配体的有机铜试剂催化格式试剂和环状或非环状的酮,并且尝试使用不同的格式试剂进行反应,在温和的实验条件下,得到ee为86%,转化率100%[12]:

其中,R为正辛基。
2010年Tim den Hartog等人使用Cu-Tol-BINAP作催化剂,用于4-氯代的不饱和酯、硫代酸酯和酮类化合物,其中在低温-78℃的条件下催化酮类化合物,反应时间为16 h,收率可高达84%,ee为96%[13]。 如:
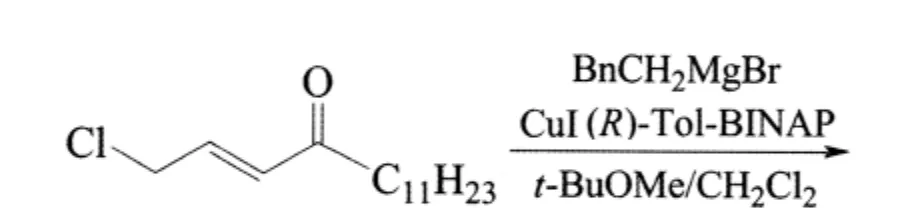
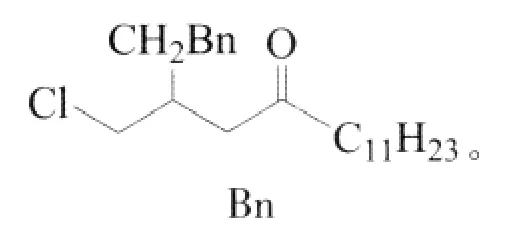
同时,Lae¨titia Palais等人首次报道了铜试剂催化格式试剂和α,β-不饱和醛类化合物的1,4-共轭加成反应,ee最高可达90%,更重要的是将2,4,6-三甲基苯磺酰氯(TMSCl)用于铜试剂催化格式试剂的反应中,使区域选择性得到很大的提高,如以下反应[14]:
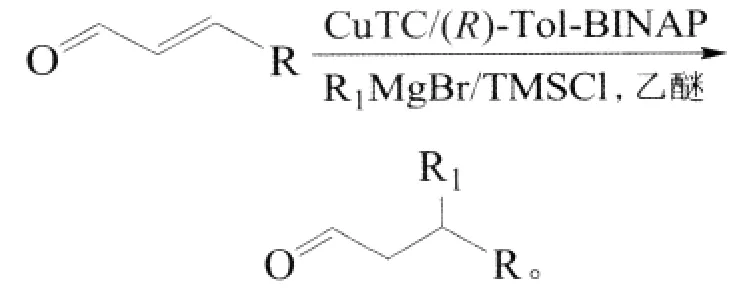
其中,CuTC为噻吩羧酸铜。
4 总结与展望
有机铜试剂催化的加成反应能够得到比较好的结果(包括收率和选择性),该类反应已成为化学家研究的热点领域之一。虽然涌现了很多优秀的配体,但在底物选择上仍然具有一定的局限性,目前反应的底物主要集中于酮类化合物,然而以醛类和砜类化合物为底物的应用报道较少,因此,研究出底物适应性广泛的手性配体将成为研究的重点;同时,为了研究出新型手性铜催化剂,应该不断深入地研究反应机理。随着研究的不断深入,有机铜试剂在催化不饱和羰基化合物的不对称共轭加成反应中必能得到更广泛的应用。
[1]程传玲,汪文良,刘艳芳.金属试剂参与的α,β-不饱和羰基化合物的不对称共轭加成反应研究进展[J].广东化工,2010,37(8):28-29.
[2]Syuzanna R Harutyunyan,Tim den Hartog,Koen Geurts,et al.Catalytic asymmetric conjugate addition and allylic alkylation with grignard reagents[J].Chem Rev,2008,108:2824-2852.
[3]Villacorta G M,Rao C P,Lippard S L.Synthesis and reactivity of binuclear tropocoronand and related organocopper(Ⅰ)complexes.catalytic enantioselective conjugate addition of grignard reagents to 2-cyclohexen-1-one[J].J Am Chem Soc,1988,110:3175-3280.
[4]Beatriz Macia Ruiz,Koen Geurts M,Angeles Fernandez-Ibanez,et al.Highly versatile enantioselective conjugate addition of grignard reagents to α,β -unsaturated thioesters[J].Org Lett,2007,9(24):5123-5126.
[5]Jack Chang Hung Lee,Dennis G Hall.Chiral boronate derivatives via catalytic enantioselective conjugate addition of grignard reagents on 3-boronyl unsaturated esters and thioesters[J].J AM CHEM SOC,2010,132:5544-5545.
[6]Pieter H Bos,Adriaan J Minnaard,Ben L Feringa.Catalytic asymmetric conjugateaddition of grignard reagents to α,βunsaturated sulfones[J].Org Lett,2008,10(19):4219-4222.
[7]Nakagawa Y,Matsumoto K,Tomioka K.Approach to enantioselective conjugate lactam bearing phosophine group[J].Tetrahedron,2000,56:2857-2863.
[8]Kanai M,Koga K,Tomioka K.Enantioselective conjugate addition oforganocuprate using a chiral amidophosphine ligand[J].Tetrahedron Lett,1992,33:7193-7196.
[9]Nakagawa Y,Kanai M,Nagaoka Y,et al.Structure requirements of an external,chiral amidophosphine ligand for asymmetric reaction of an organocopper reagent[J].Tetrahedron Lett,1996,37:7805-7806.
[10]Yasumasa Matsumoto,Ken-ichi Yamada,Kiyoshi Tomioka.C2 symmetric chiral NHC ligand for asymmetric quaternary carbon constructing copper-catalyzed conjugate addition of grignard reagents to 3-substituted cyclohexenones[J].J Org Chem,2008,73:4578-4581.
[11]Beatriz Macia′,M Angeles Fernandez-Ibanez,Natasa Mrsic,et al.Copper-catalyzed enantioselective conjugate addition of Grignard reagents to acyclic enones using monodentate phosphoramidite ligands[J].Tetrahedron Letters,2008,49:1877-1880.
[12]Laëtitia Palais,Alexandre Alexakis.Copper-catalyzed asymmetric conjugate addition with grignard reagents and simplephos ligands[J].Tetrahedron:Asymmetry,2009,20:2866-2870.
[13]Tim den Hartog,Alena Rudolph,Beatriz Macia′,et al.Copper-catalyzed enantioselective synthesis of trans-1-alkyl-2-substituted cyclopropanes via tandem conjugate additionintramolecular enolate trapping[J].J AM CHEM SOC,2010,132(41):14349-14351.
[14]Lae¨titia Palais,Lucille Babel,Adrien Quintard,et al.Copper-catalyzed enantioselective 1,4-addition to α,β -unsaturated aldehydes[J].Org Lett,2010,12(9):1988-1991.
Application of Copper-participated Asymmetric Conjugate Addition of α,β-unsaturated Carbonyl Compounds
Pan Mingxiang,Wang Wei,Pei Wen
(College of Chemical Engineering&Materials Science,Zhejiang University of Technology,Hangzhou,Zhejiang 310014)
Organic Copper-reagent is characterized by less solvent toxicity,better coordination and moderate price.The review was on asymmetric conjugate addition of α,β-unsaturated compounds using Cu-catalysts.It mainly includes α,β-unsaturated thioesters, α,βunsaturated sulfones,α,β-unsaturated aldehydes and enones.The Application of Copper-participated Asymmetric Conjugate Addition is limited due to reactants,The reactants mostly concern on α,β-unsaturated enones, α,β-unsaturated sulfones and aldehydes are still lacking,it is key to develop new ligand of chiral Copper-catalyzed reagent and we should deeply search mechanism to appear new chiral Copper-catalyzed reagent.
Cu-catalysts;asymmetric conjugate addition;carbonyl compounds
TQ032.4
ADOI10.3969/j.issn.1006-6829.2011.05.011
*通讯联系人。E-mail:peiwen58@zjut.edu.cn
2011-04-12

