皮下埋植系统与2型糖尿病治疗
李 艳,郭 晖
吉林大学 白求恩第一医院二部内分泌科,长春130031
糖尿病是一种最常见的内分泌代谢疾病,具有遗传易感性,在环境因素的触发下发病。据世界卫生组织估计,2010年全世界糖尿病患者总数为2.39亿,预计到2050年将突破3亿[1]。糖尿病已成为继肿瘤和心脑血管病之后,威胁人们健康和生命的第三大非传染性疾病。1999年世界卫生组织提出了新的糖尿病分型方法,根据病因的不同分为4个类型,分别为以胰岛β细胞破坏所致胰岛素分泌绝对缺乏为主的1型糖尿病,以胰岛素抵抗伴胰岛β细胞功能障碍为主要病理基础的2型糖尿病,以及特殊类型糖尿病和妊娠糖尿病[2]。1型糖尿病需要终身使用胰岛素治疗,2型糖尿病可根据发病情况选择使用胰岛素治疗。
胰岛素治疗
胰岛素是人胰岛β细胞分泌的体内唯一降血糖激素,在生理状态下有两种分泌形式,即持续性基础分泌和进餐刺激性增高分泌。基础分泌即平均约8~13 min释放一次,以保持一定的胰岛素基础水平,抑制肝糖生成,维持基础状态下血糖的平衡。另一方面,进餐后胰岛素分泌增加可促进葡萄糖的利用和储存,并抑制肝糖输出。胰岛素治疗主要有以下两种形式:
皮下注射皮下注射是临床最常用的胰岛素给药途径,通常使用的是胰岛素笔注射,但是长期注射不仅会给患者带来痛苦及精神负担,还可能引起局部皮下脂肪组织萎缩和硬结,影响胰岛素吸收[3]。最近有资料显示长期皮下注射胰岛素还可能导致局部皮肤发生银屑病[4]。
胰岛素泵(CSⅡ)治疗CSⅡ有可携带的开环式和闭环式两种,现临床应用的主要为前者。开环式系统包括电动机、电池、注射器、警报器、连接管及注射针头等装置。胰岛素泵的最大优点是能模拟生理胰岛素分泌,有波峰波谷,使血糖更平稳,但它也存在一些缺点,如泵故障导致的糖尿病酮症酸中毒、注射部位感染、低血糖和脂肪代谢障碍[5]。
皮下埋植缓释系统
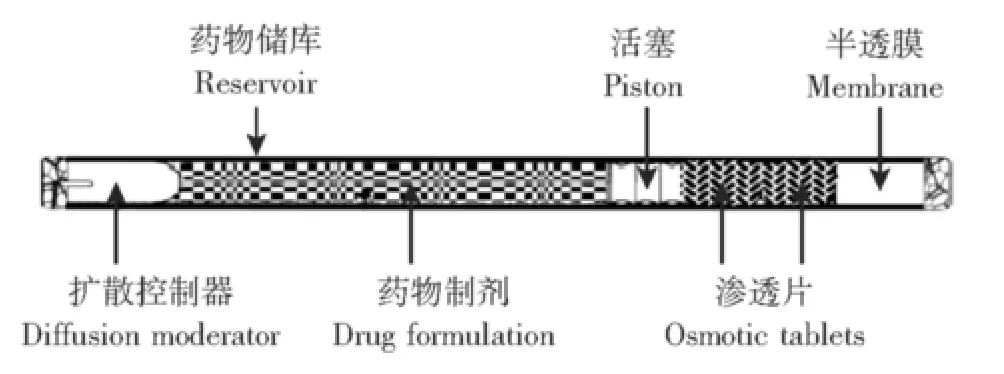
图1 皮下埋植缓释系统结构示意图Fig 1 The structure of DUROS,an implanted delivery system
DUROS是由美国Durect公司开发的皮下埋植缓释系统,是不能被生物降解的小型渗透装置。它以钛合金为材料,以埋植剂技术为基础,仅有火柴棒大小 (4 mm×45 mm),包含一个半透膜、一个渗透引擎 (含两个渗透片)、一个活塞、一个药物储库(160 ul)和一个扩散控制器[6-7](图1)。它可用于递送蛋白质、多肽和其他生物活性大分子药物。这种装置能够保证药物在体内不被降解,长时间保持稳定,持续稳定地输注药物达3~12个月。目前该设备已经成功应用于复杂的动物实验和体外活体实验,并能持续不间断地释放药物[7]。醋酸亮丙瑞林埋植剂Viadur(美国Bayer公司)已被批准用于治疗前列腺癌,它以稳定的速率每天输注120 ug亮丙瑞林,可持续输注12个月[8]。
DUROS组成构件1.半透膜 (聚氨酯膜),其渗透性已被证实可在体内和体外长时间保持稳定[8]。膜的表面积及厚度由严格的规格和生产过程控制。该半透膜用来调节水进入引擎的速率,进而控制活塞的运动和药物的释放速率。2.含有足量氯化钠的渗透引擎,水进入渗透引擎后,氯化钠溶解,渗透片膨胀。输注结束后,未溶解的氯化钠仍然存在。因此在药物输注的整个过程中,渗透引擎与外周组织的渗透压梯度仍然存在 (其值为饱和氯化钠溶液渗透压减去细胞外液渗透压)。3.热塑性弹性体活塞,表面涂有硅油,能灵活移动。4.圆柱形药物储库,以钛合金为原料,可以抗压防水,保持药物的稳定性。5.高密度聚乙烯制成的扩散控制器,上有一孔,该孔是由小直径螺旋槽形成,螺旋结构缩短了孔径的整体长度,可以承受皮下液体的反向压力,并限制其反向流入缓释系统[9]。这些组成构件都在人类植入中应用过,并已经通过美国国际标准化组织10993生物相容性测试。
工作原理渗透引擎与外周组织的渗透压梯度使水通过半透膜进入渗透系统,渗透引擎中的氯化钠吸水后溶解,渗透片膨胀,推动活塞运动,使药物通过扩散控制器的孔释放,释放速度与水进入渗透引擎的速度相等。药物释放速率可通过方程式dm/dt=(A/h)kΔⅡc求得,其中A为渗透膜的表面面积,h为渗透膜厚度,k为膜的通透性,ΔⅡ为渗透引擎与外周组织的渗透压梯度,c为药物浓度。
该皮下埋植缓释系统是为持续输注药物特别设计的,如果A、h、k、ΔⅡ和c一直保持不变,药物成分也保持稳定,就能够维持一个稳定的浓度,药物就能以恒定速率释放[9]。
使用方法这种植入体的插入和移除可以在门诊进行。插入时使用无菌技术,在非惯用手臂内侧的肘上8~10 cm处局部麻醉后,在肱二头肌与肱三头肌间隙处切开约4~5 mm皮肤,用一次性植入器将植入体植入皮下[7]。切口处用无菌伤口缝合带缝合,表面被覆消毒绷带。为方便日后移除,应在植入位置仔细标注。移除时,在上臂用触诊的方法定位植入体,如果不能触及,可用局部超声定位。定位后,先局部麻醉,如果移除时插入新的植入体,植入体的整体路径周围的组织都需要麻醉,但当路径与移除的旧植入体一致时,只需麻醉插入点远端。移除时在植入体的一端用力,使另一端翘起,用无菌技术在翘起的一端切开约4~5 mm的切口,温和施力使翘起的一端从切口露出,必要时可用手术刀切开纤维组织,用弯曲钳协助取出植入体。
植入体插入或移除后,必须观察植入点是否有出血迹象。患者必须在植入后24 h内保持该位置清洁干燥,48 h内避免剧烈运动。植入点愈合后,缝合带可在3 d左右拆除[10]。植入后最常见的局部反应是瘀斑,发生率为33%,大多数可在2周内缓解,仅有2%的患者可能出现局部炎症反应,一般口服抗生素即可治愈。其它副作用包括局部的过敏反应和植入物的脱出,但是出现的几率非常小[8]。
DUROS泵入的药物目前正在研究的是胰高糖素 样 肽-1(human glucagon-like peptide,GLP-1)。GLP-1是一种生理性肽类肠道激素,主要由空肠末端、回肠和结肠中的神经内分泌细胞L细胞分泌。GLP-1可降低血糖的水平,研究表明可用于治疗2型糖尿病[11]。
GLP-1含有30个氨基酸[12],由胰高糖素原C端加工形成。葡萄糖和脂肪酸能刺激GLP-1释放入血,与特异的GLP-1受体作用后发挥效应。GLP-1在体内的分泌为脉冲式分泌,葡萄糖的摄入可增加其脉冲的幅度而不增加频率。GLP-1释放入血后极易被体内的二肽基肽酶Ⅳ (dipeptidyl peptidase-Ⅳ,DPP-Ⅳ)裂解为无生物学活性的代谢产物,其半衰期仅2 min,必须持续静脉滴注或持续皮下注射才能产生疗效。因此目前研究的主要是抵抗DPP-Ⅳ的GLP-1类似物,如利拉鲁肽,可在保留生理活性的同时延长作用时间。
GLP-1的最重要作用之一是增加胰岛素分泌[13-14],但该作用有葡萄糖依赖性,因此不会诱发低血糖[15-17]。GLP-1对胰高糖素的分泌也有调节作用,部分通过增加生长激素释放来抑制胰高糖素分泌,部分则是通过直接作用于α细胞。胰高糖素分泌减少使肝脏葡萄糖输出下降,进而使清晨空腹血糖水平保持正常[15]。用分离的新生大鼠胰岛进行的体外研究表明,GLP-1能够抑制β细胞凋亡,用动物模型所做的体外研究证实,GLP-1通过刺激β细胞新生、生长和增殖使β细胞量增加[18-21]。此外,GLP-1还具有减轻体重、抑制胃排空、减少进食和心血管保护作用[22-26]。
因其具有促胰岛素分泌和抑制胰岛细胞凋亡的作用,且无低血糖等副作用,GLP-1在2型糖尿病的治疗应用中有光明的前景。它主要适用于4类患者。
初发2型糖尿病:研究显示,患者诊断为糖尿病前10年,β细胞功能已开始衰减,确诊为糖尿病时,β细胞功能至少已丧失50%,且即使接受治疗其功能仍继续恶化[27]。GLP-1不仅能通过多种途径控制血糖,还能促进β细胞增殖,抑制β细胞凋亡。在糖尿病前期及早期应用GLP-1,不但能有效控制血糖,延缓并发症的发生,甚至还可逆转β细胞功能衰退,降低2型糖尿病发生率[28]。
超重的2型糖尿病:超重与肥胖是2型糖尿病的重要危险因素,不仅增加心血管并发症的发生,也为选择用药带来困难。传统的降糖药大多不能降低体重,目前使用的胰岛素还有增加体重的不良反应。与之相比,GLP-1既能降糖又能降低体重,对超重的2型糖尿病患者更有益[28]。
血压升高的2型糖尿病:我国糖尿病患者中高血压患病率高达60%[29],糖尿病患者合并高血压可加速并发症发生发展,增加糖尿病的死亡率[30]。糖尿病患者血压应保持在130/80 mmHg(1 mmHg=0.133 kPa)以下,可充分改善心血管疾病和微血管病变的临床状况[31]。GLP-1具有降糖、降压的作用,对改善2型糖尿病患者远期转归十分有益[32]。
老年人2型糖尿病:老年糖尿病患者是低血糖的易感人群,医源性低血糖不仅限制了2型糖尿病降糖达标,影响治疗效果,而且直接危害患者健康,甚至导致严重心脑血管事件,危及生命。GLP-1能避免或减少低血糖事件,特别是避免夜间低血糖的发生,因此非常适用于老年2型糖尿病患者[16]。
DUROS与GLP-1的联合应用
DUROS不同于平时使用的胰岛素泵,它是一个渗透装置,可根据渗透膜两边的压力差调节药物的释放。该装置不能设置时段及剂量,但可根据体内血糖水平的变化调整药物释放。DUROS以恒定的速率释放药物,可能在一定程度上能避免导管堵塞。目前对GLP-1的研究很多,但是临床上尚未真正将GLP-1与DUROS联合用于降糖治疗。两者的联合应用有以下优缺点:
优点DUROS的植入和移除非常简单,且副作用很少。它植入皮下后对患者的日常生活基本没有影响,对大多数患者的生活质量如工作和睡眠质量也不会产生影响[33]。GLP-1只有在血糖升高时才发挥降糖效应,因此比较安全。体外研究发现,GLP-1在DUROS中的稳定性及释放率良好,在37℃条件下储存6个月,GLP-1的纯度维持在90%以上,并以稳定的速率释放[34]。
缺点可能存在药物的长期稳定性、泵的局部排它性、泵膨胀、导管堵塞、资金问题、推广及患者接受度等问题。
综上,DUROS有很多优点,如减少剂量、具有更好的药代动力学及药效学性质、改善了顺应性、减少副作用、消除药物浓度波动及提高疗效等,但由于是有创治疗,且价格昂贵,还存在导管堵塞的问题,因此尚未在临床普及,但是将来可能会成为2型糖尿病患者理想的治疗选择。
[1]卫生部疾病控制司,中华医学会糖尿病学分会.中国糖尿病防治指南 [EB/OL].[2010-7-15].http://wenku.baidu.com/view/aab3fa0b79563c1ec5da710c.html.
[2]Alberti KG,Zimmet PZ.Definition,diagnosis and classification of diabetes mellitus and its complications.Part 1:diagnosis and classification of diabetes mellitus provisional report of a WHO consultation[J].Diabet Med,1998,15(7):539-553.
[3]Perciun R.Ultrasonographic aspect of subcutaneous tissue dystrophies as a result of insulin injections[J].Med Ultrason,2010,12(2):104-109.
[4]Wanq P,Ran Y.Subcutaneous injection of isophane protamine biosynthetic human insulin induced psoriasis at the injection site[J].Eur J Dermatol.[2011-7-7].http://www.jle.com/en/revues/medecine/ejd/e-docs/00/04/69/A9/resume.phtml.
[5]Potti LG,Haines ST.Continuous subcutaneous insulin infusion therapy:a primer on insulin pumps[J].J Am Pharm Assoc(2003),2009,49(1):e1-e13.
[6]Messing EM,Manola J,Sarosdy M,et al.Immediate hormonal therapy compared with observation after radical prostatectomy and pelvic lymphadenopathy in men with node-positive prostate cancer[J].N Engl J Med,1999,341(24):1781-1788.
[7]Fowler JE Jr,Gottesman JE,Reid CF,et al.Safety and efficacy of an implantable leuprolide delivery system in patients with advanced prostate cancer[J].J Urol,2000,164(3 Pt 1):730-734.
[8]Marks LS.Luteinizing hormone-releasing hormone agonists in the treatment of men with prostate cancer:timing,atternatives,and the 1-year implant[J].Urology,2003,62(6 Suppl 1):36-42.
[9]Wright JC,Tao Leonard S,Stevenson CL,et al.An in vivo/in vitro comparision with a leuprolide osmotic implant for the treatment of prostate cancer[J].J Control Release,2001,75(1-2):1-10.
[10]Moul JW,Civitelli K.Managing advanced prostate cancer with Viadur(leuprolide acetate implant)[J].Urol Nurs,2001,21(6):385-388,393-394.
[11]Toft-Nielsen MB,Madsbad S,Holst JJ.Continuous subcutaneous infusion of glucagon-like 1 lowers plasma glucose and reduces appetite in type 2 diabetic patients[J].Diabetes Care,1999,22(7):1137-1143.
[12]Holst JJ.The physiology of glucagon-like peptide 1 [J].Physiol Rev,2007,87(4):1409-1439.
[13]Orskov C,Holst JJ,Nielsen OV.Effect of truncated glucagon-like peptide-1[proglucagon-(78-107)amide]on endocrine secretion from pig pancreas,antrum,and nonantral stomach[J].Endocrinology,1988,123(4):2009-2013.
[14]Mojsov S,Weir GC,Habener JF.Insulinotropin:glucagonlike peptide I(7-37)co-encoded in the glucagon gene is a potent stimulator of insulin release in the perfused rat pancreas[J].J Clin Invest,1987,79(2):616-619.
[15]Drucker DJ.The biology of incretin hormones[J].Cell Metab,2006,3(3):153-165.
[16]Degn KB,Brock B,Juhl CB,et al.Effect of intravenous infusion of exenatide(synthetic exendin-4)on glucose-dependent insulin secretion and counterregulation during hypoglycemia[J].Diabetes,2004,53(9):2397-2403.
[17]Nauck MA,Heimesaat MM,Behle K,et al.Effects of glucagon-like peptide 1 on counterregulatory hormone responses,cognitive functions,and insulin secretion during hyperinsulinemic,stepped hypoglycemic clamp experiments in healthy volunteers [J].J Clin Endocrinol Metab,2002,87(3):1239-1246.
[18]Xu G,Kaneto H,Lopez-Avalos MD,et al.GLP-1/exendin-4 facilitates beta-cell neogenesis in rat and human pancreatic ducts[J].Diabetes Res Clin Pract,2006,73(1):107-110.
[19]Movassat J,Beattie GM,Lopez AD,et al.Exendin 4 upregulates expression of PDX 1 and hastens differentiation and maturation of human fetal pancreatic cells[J].J Clin Endocrinol Metab,2002,87(10):4775-4781.
[20]Liu Z,Habener JF.Glucagon-like peptide-1 activation of TCF7L2-dependent Wnt signaling enhances pancreatic beta cell proliferation[J].J Biol Chem,2008,283(13):8723-8735.
[21]Chen J,Couto FM,Minn AH,et al.Exenatide inhibits beta-cell apoptosis by decreasing thioredoxin-interacting protein[J].Biochem Biophys Res Commun,2006,346(3):1067-1074.
[22]Lovshin JA,Drucker DJ.Incretin-based therapies for type 2 diabetes mellitus[J].Nat Rev Endocrinol,2009,5(5):262-269.
[23]Timmers L,Henriques JP,de Kleijn DP,et al.Exenatide reduces infarct size and improves cardiac function in a porcine model of ischemia and reperfusion injury [J].J Am Coll Cardiol,2009,53(6):501-510.
[24]Noyan-Ashraf MH,Momen MA,Ban K,et al.GLP-1R agonist liraglutide activates cytoprotective pathways and improves outcomes after experimental myocardial infarction in mice[J].Diabetes,2009,58(4):975-983.
[25]Nikolaidis LA,Mankad S,Sokos GG,et al.Effects of glucagon-like peptide-1 in patients with acute myocardial infarction and left ventricular dysfunction after successful reperfusion[J].Circulation,2004,109(8):962-965.
[26]Sokos GG,Nikolaidis LA,Mankad S,et al.Glucagon-like peptide-1 infusion improves left ventricular ejection fraction and functional status in patients with chronic heart failure.J Card Fail,2006,12(9):694-699.
[27]UK Prospective Diabetes Study Group.U.K.prospective diabetes study 16.Overview of 6 years’therapy of type II diabetes:a progressive disease [J].Diabetes,1995,44(11):1249-1258.
[28]Kendall DM,Cuddihy RM,Bergenstal RM.Clinical application of incretin-based therapy:therapeutic potential,patient selection and clinical use[J].Eur Intern Med,2009,20 Suppl 2:S329-S339.
[29]陈国伟.高血压与糖尿病 [J].中国实用内科杂志,2002,22(4):199-200.
[30]UK Prospective Diabetes Study Group.Efficacy of atenolol and captopril in reducing risk of macrovascular and microvascular complications in type 2 diabetes [J].BMJ,1998,317(7160):713-720.
[31]Marshall SM,Flyrbjerg A.Prevention and early detection of vascular complications of diabetes [J].BMJ,2006,333(7566):475-480.
[32]Haluzík M,Urbanová M,Trachta P.Treatment of type 2 diabetes mellitus with GLP-1 antagonists [J].Vnitr Lek,2011,57(4):411-415.
[33]Fowler JE Jr,Viadur Study Group.Patient-reported experience with the Viadur 12-month leuprolide implant for prostate cancer[J].Urology,2001,58(3):430-434.
[34]Rohloff CM,Alessi TR,Yang B,et al.DUROS technology delivers peptides and proteins at consistent rate continuously for 3 to 12 months [J].J Diabetes Sci Technol,2008,2(3):461-467.

