高效毛细管电泳分离测定水中的乙酸和氯代乙酸
朱金花,陈兴国,刘绣华
(1.河南大学化学化工学院,河南开封 475004; 2.兰州大学化学化工学院,甘肃兰州 730000)
高效毛细管电泳分离测定水中的乙酸和氯代乙酸
朱金花1,2,陈兴国2,刘绣华1
(1.河南大学化学化工学院,河南开封 475004; 2.兰州大学化学化工学院,甘肃兰州 730000)
用邻苯二甲酸氢钾(p H=5.4)缓冲液作为电泳的背景电解质,以十六烷基三甲基溴化铵作为电渗流抑制剂,用甲基叔丁基醚作为萃取剂处理水样,建立了一种测定水中的乙酸和氯代乙酸的简单灵敏的毛细管区带电泳(紫外检测)法.测定结果表明,分析物的迁移时间和峰面积的日内相对标准偏差分别低于0.33%和4.45%,日间相对标准偏差分别低于0.87%和9.67%.
乙酸;氯代乙酸;毛细管电泳;分离;测定
Abstract:A simple and sensitive capillary zone electrophoresis method has been established to determine acetic acid and chloroacetic acid in water by using potassium hydrogen phthalate(p H=5.4)as the background electrolyte,hexadecyltrimethylammonium bromide as electroosmotic flowing inhibitor,and methyl tert-butyl ether as the extractant to treat water sample.It was found that acetic acid and chloroacetic acid in water could be determined with relative standard deviation of migration time and corrected peak area below 0.33%and 4.45%(intra-day),or below 0.87%and 9.67%(inter-day).
Keywords:acetic acid;chloroacetic acids;capillary electrophoresis;separation;determination
氯代乙酸是卤代乙酸(HAAs)的一种.一氯乙酸(MCA)、二氯乙酸(DCA)和三氯乙酸(TCA)总称氯代乙酸,是环境中分布广泛的污染物[1].氯代乙酸是饮用水的源水在氯化消毒处理过程中产生的副产物[2-3].MCA通过呼吸道和裸露的皮肤被人体吸收,如果皮肤接触的浓度较高,将导致皮肤和眼部的疾病.毒理学研究表明DCA和 TCA具有致癌性[4-6].由于 HAAs对环境和人类的影响,对它们的测定引起了广泛的关注[7-8].美国国家环保局公布实施的饮用水第一阶段控制法案[9]中规定五种 HAAs总的最高允许质量浓度为60μg/L.研究表明,由于饮用水消毒副产物控制法案的提出,使得传统的消毒方式发生改变.新的消毒方法虽然能使消毒副产物的总量有所下降,但 HAAs的浓度显著增加,成为已确定的消毒副产物中含量较多的一种[10-11].在所测定的 HAAs中,DCA和 TCA的含量较高[10].
氯代乙酸的定量分析方法很多,其中主要有化学衍生后用气相色谱(GC)分析[10,12-15].衍生测定法虽然具有灵敏、准确等优点,但由于所用的衍生试剂有较强的毒性,使其应用受到较大的限制.因此,人们相继建立了测定氯代乙酸的反向离子对色谱法(RP-IPC)和高效液相色谱法法(HPLC)[1,16].但是这些分析方法的分离时间比较长,而且检测限较高.
毛细管电泳(CE)是近年来发展起来的一种高效、快速的新型分离技术,因其具有分离模式多、试剂消耗量少、分离时间短等优点,而被广泛应用于分析化学和生物医药及环境科学中.由于氯代乙酸自身没有紫外吸收,需要用间接紫外检测的方法进行测定.最常用的间接紫外法的背景吸收物质是邻苯二甲酸氢钾.但是电泳法测定 HAAs时,灵敏度较低,不能满足环境中痕量测定的要求.Martínez等人分别用萃取和电迁移进样的方法对HAAs进行了富集,极大地降低了检测限[17-18].但其所用的间接紫外背景吸收物质和固相微萃取柱价格昂贵,限制了其实际应用.为进一步降低电泳检测氯代乙酸的检测限,本文作者采用液液萃取(LL E)的方式对样品中氯代乙酸进行萃取,电迁移进样的方式对分析物进行进一步富集,建立了测定水中氯代乙酸的毛细管电泳新方法,极大地提高了氯代乙酸的检测灵敏度.
1 实验部分
1.1 仪器
Waters Quanta 4000毛细管电泳仪(Milford,MA,USA).紫外检测波长为254 nm.使用Maxima 820 Chromatograph Workstation进行数据采集.石英毛细管为40.0 cm ×75μm(河北永年光导纤维厂),有效长度为32.4 cm.阴极进样.实验温度为20.0±0.5℃.缓冲液的p H值用0.2 mol/L NaOH或0.2 mol/L HCl调节,由p HS-3B型酸度计(上海精密科学仪器厂)测定.毛细管第一次使用前依次用0.1 mol/L NaOH冲洗10 min、蒸馏水冲洗10 min、缓冲溶液冲洗10 min.两次运行之间毛细管用缓冲溶液冲洗3 min.
1.2 试剂
MCA、甲基叔丁基醚(MTBE)、丙酮和乙酸(HAc)购自天津化学试剂厂,DCA购于 Sigma-Aldrich公司,TCA和十六烷基三甲基溴化铵(CTAB)购自上海化学试剂公司,邻苯二甲酸氢钾购自西安化学试剂公司.所用试剂均为分析纯,所有实验用水均为超纯水.
1.3 标准品溶液和缓冲溶液的配制
标准品的储备液用超纯水制备,质量浓度分别为200 mg/L.使用时用超纯水稀释至所需浓度.背景电解质溶液由0.1 mol/L邻苯二甲酸氢钾、5 mmol/L CTAB和水按不同体积混合而成.所有溶液使用前均用0.45μm的滤膜(上海新亚净化器件厂)过滤.
1.4 样品预处理
液液萃取过程参考文献[19]进行.将50 mL自来水或者游泳池水的p H值用2 mol/L的NaOH调到11.5,将溶液转移到分液漏斗中,加入7.5 mL MTBE,振荡5 min,静置分层.弃去有机相,将水相的p H值用浓硫酸调至0.5,加入10 g氯化钠,振荡至全部溶解.再加入2.5 mL MTBE,继续振荡5 min.分层后,收集有机相.重复上述萃取过程两次,合并有机相.通氮气使有机相挥发完全后,加入300μL超纯水溶解萃取后的氯代乙酸,用0.45μm滤膜过滤后直接进样分析.
2 结果与讨论
2.1 分离条件的优化
在氯代乙酸质量浓度为10 mg/L、乙酸质量浓度为2 mg/L、重力进样(10 cm,20 s)条件下,考察了缓冲溶液p H值、分离电压、邻苯二甲酸氢钾和CTAB的浓度对分离效果的影响.结果表明,缓冲溶液p H值小于5.0时,HAc和 TCA很难分开,并且 HAc的峰和系统峰部分重叠;当缓冲p H值大于6.0时,MCA和DCA的峰重叠,因此选择p H值5.0~6.0为缓冲p H值的优化区间.考虑分离度、待测物的峰形和峰面积,选择5.4作为缓冲液的最佳p H值.还考察了分离电压在-5 kV~-15 kV变化时对分离行为的影响.结果表明,分离电压升高,分析物的迁移时间缩短,体系电流增大,综合考虑迁移时间和电流选择-10 kV作为最佳分离电压.实验结果还表明,邻苯二甲酸氢钾和CTAB的浓度对待测物的分离行为影响不大,综合考虑峰形和灵敏度,确定邻苯二甲酸氢钾和CTAB的最佳浓度分别为12.5 mmol/L和0.5 mmol/L.综合考虑,最佳的分离条件为:12.5 mmol/L邻苯二甲酸氢钾,0.5 mmol/L CTAB,p H值5.4,分离电压-10 kV.最佳分离条件下标准品混合液的电泳谱图如图1A所示.
2.2 富集条件的优化
许多研究证明电迁移进样能对样品进行预富集[20-22].由于电离,乙酸和氯代乙酸在p H值 5.4时带负电荷,可以用电动进样的方式对待测物进行富集.富集效率与进样电场强度和分析物自身性质有关.这种富集方法的最大优点是操作简单,不需要对仪器进行改动.在上述最佳的分离条件下,考察了进样电压和进样时间对分析物富集效果的影响.结果表明分析物的峰高随进样时间的增长而增高.当进样时间超过10 s时,分析物峰高不再增加,峰形变宽.因此,选择10 s作为最佳的进样时间.实验结果还表明,进样电压为-5 kV时,富集效果最好,故选择-5 kV为最佳进样电压.在上述最佳富集条件下标准品混合物的电泳谱图如图1B所示.

图1 重力进样模式和电迁移进样模式下标准品谱图Fig.1 Eelectropherograms of the four acids
2.3 工作曲线、检测限和重现性
在上述最佳条件下,各分析物的回归方程和检测限如表1所示.由表1可见,电迁移进样极大地降低了分析物的检测限,可以满足水中痕量氯代乙酸测定的要求.分析物峰面积和迁移时间的重现性见表2.连续5次运行所获得的迁移时间和峰面积的相对标准偏差(RSD)分别为:0.25%~0.33%和2.34%~4.45%(日内);0.64%~0.87%和7.22%~9.67%(日间).
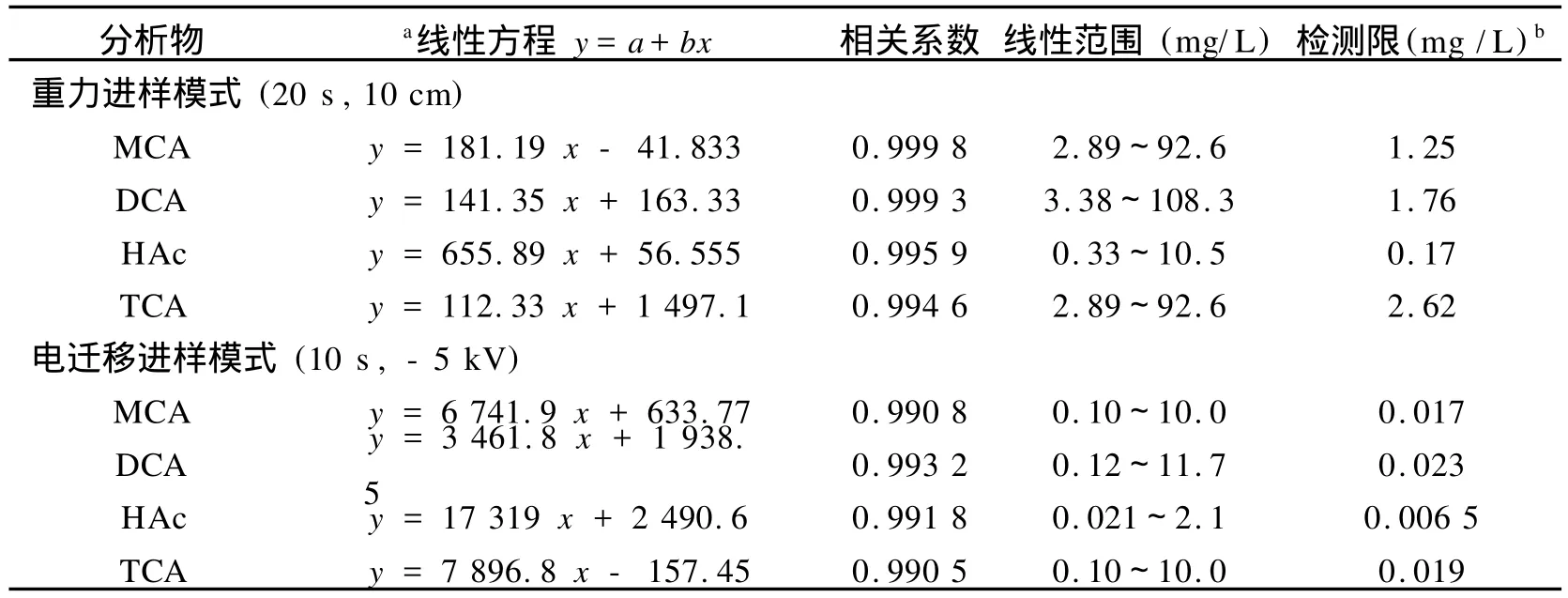
表1 回归方程和检测限Table 1 The results of regression analysis on calibration curves and the detection limits
2.4 样品分析
用电迁移进样模式对兰海泳池水和实验室自来水进行了分析.在对样品进行处理前直接进样,除了一个较大的干扰峰外,没有检测到待测物的峰.所以样品需要进一步浓缩并消除干扰峰.样品按照1.4中所述方法进行萃取后,直接进样分析,电泳谱图如图2所示.通过比较迁移时间和标准加入法对实际样品电泳图中各组分的峰进行确认.各组分的含量及RSD如表3所示.由表3可见,水样中DCA和 TCA的含量较其他两种待测物的含量高,且游泳池水中氯代乙酸的含量比自来水中氯代乙酸含量高,可能是游泳池中的水加氯消毒所至,但是两种水样中氯代乙酸的总含量都没有超过美国环保局规定所允许的最高质量浓度(60μg/L).

表2 电迁移进样模式下分析物的重现性Table 2 Repeatability of analytes in CE

图2 样品的电泳谱图Fig.2 Electropherogram of samples

表3 样品中氯乙酸的含量Table 3 Contents of the four analytes in real samples
3 结论
作者所建立的方法可以用于同时分离测定水中的氯代乙酸,方法简单、重现性好,对水中氯代乙酸的测定和水质监控具有一定的实用价值.
[1]LOOS R,BARCELO D.Determination of haloacetic acids in aqueous environments by solid-phase extraction followed by ion-pair liquid chromatography-electrospray ionization mass spectrometric detection[J].J Chromatogr A,2001,938(1/2):45-55.
[2]DOMINO M M,PEPICH B V,MUNCH D J,et al.Optimizing the determination of haloacetic acids in drinking waters[J].J Chromatogr A,2004,1035(1):9-16.
[3]AKHTAR P,TOO C O,WALLACE G G.Detection of haloacetic acids at conductive electroactive polymer-modified mi-croelectrodes[J].Anal Chim Acta,1997,341(2/3):141-153.
[4]BERG M,MULL ER S R,MU HL EMANN J,et al.Concentrations and mass fluxes of chloroacetic acids and trifluoroacetic acid in rain and natural waters in Switzerland[J].Environ Sci Technol,2000,34(13):2675-2683.
[5]SCOTT B F,MACTAVISH D,SPENCER C,et al.Haloacetic acids in Canadian lake waters and precipitation[J].Environ Sci Technol,2000,34(20):4266-4272.
[6]RICHARD A M,HUNTER III E S.Quantitative structure-activity relationships for the developmental toxicity of haloacetic acids in mammalian whole embryo culture[J].Teratology,1996,53(6):352-360.
[7]SARZANINI C,BRUZZONITI M C,MENTASTI E.Preconcentration and separation of haloacetic acids by ion chromatography[J].J Chromatogr A,1999,850(1/2):197-211.
[8]MAGNUSON M L,KEL TY C A.Microextraction of nine haloacetic acids in drinking water at microgram per liter levels with electrospray-mass spectrometry of stable association complexes[J].Anal Chem,2000,72(6):2308-2312.
[9]US EPA.National primary drinking water regulation:Interim enhanced surface water treatment[S/OL].1998,63(241):69477-69521.[2010-12-01]http://water.epa.gov/lawsregs/rulesregs/sdwa/mdbp/ieswtrfr.cfm.
[10]WILLIAMS D T,L EBEL GL,BENOIT F M.Disinfection by-products in Canadian drinking water[J].Chemosphere,1997,34(2):299-316.
[11]SINGER P C,OBOL ENSKY A,GREINER A.DBPs in chlorinated North Carolina drinking waters[J].J Am Water Works Assoc,1995,87(10):83-92.
[12]COWMAN G A,SINGER P C.Effect of bromide ion on haloacetic acid speciation resulting from chlorination and chloramination of aquatic humic substances[J].Environ Sci Technol,1996,30(1):16-23.
[13]BENANOU D,ACOBAS F,SZTAJNBOK P.Analysis of haloacetic acids in water by a novel technique:simultaneous extraction derivatization[J].Water Res,1998,32(9):2798-2806.
[14]RICHARDSON S D,THRUSTON Jr A D,CAU GHRAN T V.Identification of new ozone disinfection byproducts in drinking water[J].Environ Sci Technol,1999,33(19):3368-3377.
[15]HUNTER E S,ROGERS E H,SCHMID J E,et al.Comparative effects of haloacetic acids in whole embryo culture[J].Teratology,1996,54(2):57-64.
[16]VICHOT R,FURTON K G.Variables influencing the direct determination of haloacetic acids in water by reversed-phase ion-pair chromatography with indirect UV detection[J].J Liq Chromatogr,1994,17(20):4405-4429.
[17]MARTINEZ D,FARRE J,BORRULL F,et al.Capillary zone electrophoresis with indirect UV detection of haloacetic acids in water[J].J Chromatogr A,1998,808(1/2):229-235.
[18]MARTÍNEZ D,BORRULL F,CALULL M.Evaluation of different electrolyte systems and on-line preconcentrations for the analysis of haloacetic acids by capillary zone electrophoresis[J].J Chromatogr A,1999,835(1/2):187-196.
[19]DALVI A G I,A1-RASHEED R,JAVEED M A.Haloacetic acids(HAAs)formation in desalination processes from disinfectants[J].Desalination,2000,129(3):261-271.
[20]WESTON A,BROWN P R,JANDIK P,et al.Optimization of detection sensitivity in the analysis of inorganic cations by capillary ion electrophoresis using indirect photometric detection[J].J Chromatogr A,1992,608(1/2):395-402.
[21]J IMIDAR M,HARTMANN C,CONSEMENT N,et al.Determination of nitrate and nitrite in vegetables by capillary electrophoresis with indirect detection[J].J Chromatogr A,1995,706(1/2):479-492.
[22]GUAN Fu Yu,WU Hui Fang,LUO Yi.Sensitive and selective method for direct determination of nitrite and nitrate by high performance capillary electrophoresis[J].J Chromatogr A,1996,719(2):427-433.
Separation and determination of acetic acid and chloroacetic acid in water by efficient capillary electrophoresis
ZHU Jin-hua1,2,CHEN Xing-guo2,LIU Xiu-hua1
(1.College of Chemistry and Chemical Engineering,Henan University,Kaif eng475004,Henan,China;
2.College of Chemistry and Chemical Engineering,L anzhou University,L anzhou730000,Gansu,China)
O 675.8
A
1008-1011(2011)02-0056-05
2010-10-14.
朱金花(1982-),女,博士,从事色谱分离科学技术研究.

