盐酸川芎嗪滴眼液在兔眼房水中的药动学研究
何梅凤, 邓新国,2*, 吴 伟, 高 杨,2
(1.中山大学中山眼科中心;2.中山大学眼科学国家重点实验室,广东广州510060)
川芎嗪是从中药川芎的根茎中提取的有效成分,具有扩张血管、抗血小板聚集、改善组织微循环、抗脂质过氧化、抗自由基、Ca2+阻滞、抗组织纤维化等药理作用,临床应用广泛[1-2]。近年来,其在眼科疾病的防治也取得了一定的疗效,具有较好的应用前景[3-4]。有研究[5]表明,川芎嗪经腹腔注射后能进入兔眼组织,但存在眼内组织消除快的缺点,而全身用药的次数又受患者的依从性和药物不良反应等因素的影响,从而使其在眼科临床使用受到一定的影响。因此,将其开发成眼局部应用剂型具有重要的意义。目前,国内外还未见有关川芎嗪局部滴眼后眼内药代动力学的报道,本研究通过盐酸川芎嗪局部应用兔眼后,考察其房水药代动力学情况,为川芎嗪眼局部应用提供理论依据。
1 试验材料
1.1 仪器 Agilent 1100高效液相色谱仪,包括G1314A紫外检测器,G1316A柱温箱,G1329A带温控自动进样器,G1311A四元泵,G1322A真空脱气机(美国安捷伦公司);Agilent 1100化学工作站;离心机(上海安亭科学仪器厂)。
1.2 试药 盐酸川芎嗪对照品(中国药品生物制品检定所,批号:110817-200305);盐酸川芎嗪原料药(西安力邦制药有限公司,批号:061001B);盐酸川芎嗪滴眼液(自制,5 mL∶25 mg);玻璃酸钠(山东福瑞达生物化工有限公司,批号:0508111);甲醇为色谱纯,其它试剂为分析纯。
1.3 动物 新西兰白兔27只,健康无眼疾,雌14只,雄13只,体质量2.0~2.4 kg,由广东医用动物实验中心提供。
2 方法与结果
2.1 实验动物分组 将27只新西兰白兔,随机分为9组,每组3只(6眼)。
2.2 给药及样品采集方法 将家兔固定在兔箱内,轻轻拉开眼睑使与眼球成袋状,用微量加样器滴入盐酸川芎嗪滴眼液50μL,再轻轻放开下眼睑,使药物不会溢出。给药后,分别于 0、2.5、5、15、30、60、120、180、240 min采取耳缘静脉空气栓处死家兔,立即抽取房水150μL置1.5 mL离心试管中,于-20℃冰箱保存备用。
2.3 色谱条件 色谱柱为Diamonsil C18不锈钢柱(250 mm ×4.6 mm,5 μm),流动相为甲醇-水(62 ∶38),体积流量0.9 mL/min,紫外检测波长为280 nm,柱温为20℃,进样量40μL。
2.4 对照品溶液的配制 精密称取盐酸川芎嗪对照品8 mg,以甲醇为溶媒定容于10 mL量瓶,即得质量浓度为0.8 mg/mL的对照品贮备液,密封放冰箱备用。对照品工作液在使用前由以上贮备液稀释制得。
2.5 样品处理 分别取不同时间组白兔房水各150 μL,解冻后,旋涡振荡1 min,12 000 r/min离心5 min,取上清液100μL,加入100μL色谱甲醇,旋涡振荡1 min,12 000 r/min离心5 min,取上清液,进样40μL。
2.6 系统适应性试验
2.6.1 方法专属性 在以上色谱条件下,盐酸川芎嗪的保留时间为6.7 min,与眼组织中内源性物质及其它杂质分离良好。色谱图见图1。
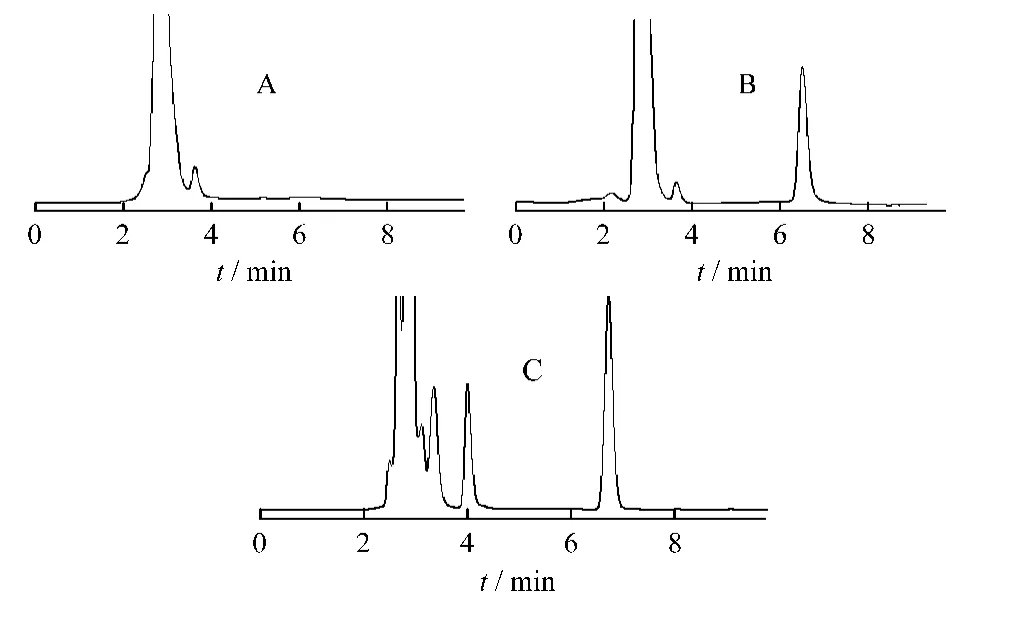
图1 盐酸川芎嗪色谱图Fig.1 Chromatogram of ligustrazine hydrochloride
2.6.2 标准曲线制备 精密吸取空白房水适量,与上述对照品贮备液稀释制得的不同质量浓度对照品工作液适量混合,配制成盐酸川芎嗪质量浓度为40、20、10、2、1、0.5、0.25 和 0.025 μg/mL 的空白房水川芎嗪溶液,按2.5项方法进行处理进样,将峰面积值(A)对浓度值(C)作线性回归,所得标准曲线为:C=0.009 43A -0.027 08,r=0.999 9,表明盐酸川芎嗪在质量浓度为20~0.012 5μg/mL范围内线性关系良好。
2.6.3 回收率和精确度试验 精密称取盐酸川芎嗪对照品适量,分别配制 0.25、2.00 和 20.00 μg/mL 3个质量浓度的盐酸川芎嗪空白房水液,按2.5项下操作并进行分析,求得盐酸川芎嗪在空白房水中的回收率。在同一天和5 d间(每天一批)对以上3个质量浓度的盐酸川芎嗪空白房水液分别处理5批后进样分析,分析日内和日间的RSD。房水中盐酸川芎嗪低、中、高3种浓度回收率及精密度结果见表1。
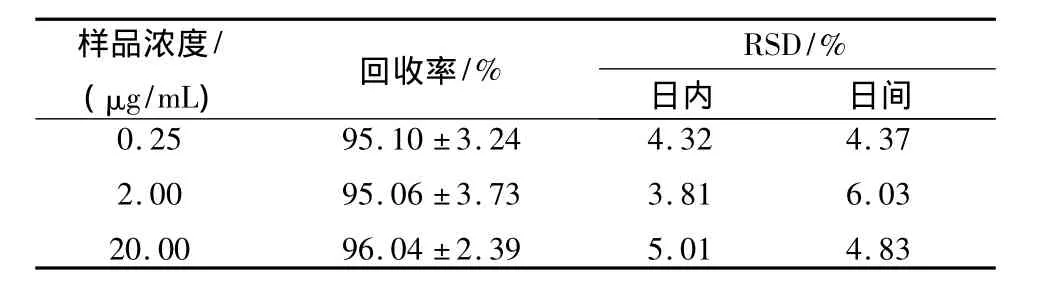
表1 兔眼房水中盐酸川芎嗪回收率和精密度(n=5)Tab.1 Recovery and accuracy of ligustrazine hydrochloride in the humor aqueous of rabbits(n=5)
2.6.4 稳定性考察 精密称取盐酸川芎嗪对照品适量,分别配制0.25、2.00 和 20.00 μg/mL 3 个质量浓度的盐酸川芎嗪空白房水液,分别考察样品于冰箱 -20 ℃存放0、2、4、8、12 d 后,样品经处理放置0、4、8、12、24 h 后盐酸川芎嗪的稳定性。结果 3 个质量浓度的RSD<8%,表明样品在12 d内冰冻保存稳定,处理后24 h内进样分析不影响结果。
2.7 房水中盐酸川芎嗪的浓度 兔眼局部滴用盐酸川芎嗪滴眼液后,川芎嗪能快速进入兔眼房水,5 min达高峰,然后逐渐下降,在4 h其浓度已非常低。具体结果见图2。
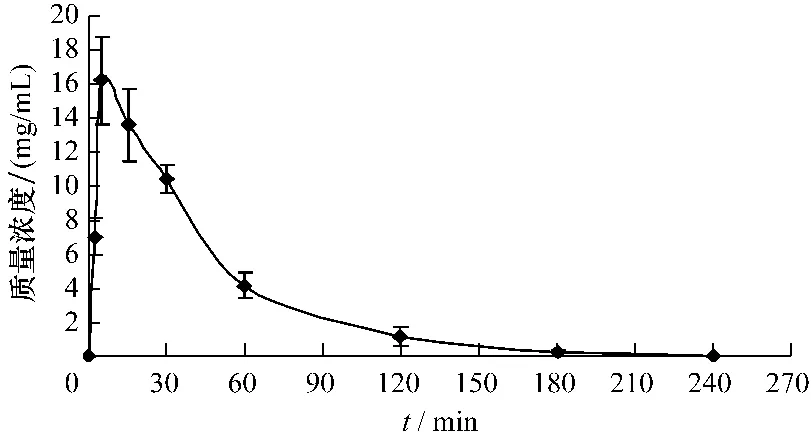
图2 兔眼滴用盐酸川芎嗪滴眼液后房水的药时曲线Fig.2 Mean concentration-time curves of ligustrazine hydrochloride in aqueous humor of rabbits after topical adm inistration
2.8 房水中的药代动力学模型拟合及相关参数盐酸川芎嗪滴眼液局部应用后在兔眼房水中的房室模型及药代动力学参数采用DSA2.1.1版软件进行拟合。结果表明,盐酸川芎嗪浓度在正常白兔房水中呈二室模型,达峰时间快,峰浓度较高,但消除也较快。具体药代动力学参数见表2。
表2 兔眼局部滴用盐酸川芎嗪后盐酸川芎嗪在房水中的药动学参数( ± s,n=6)Tab.2 The pharmackinetic parameters of ligustrazine hydrochloride in aqueous humor of rabbits after topical adm inistration( ± s,n=6)
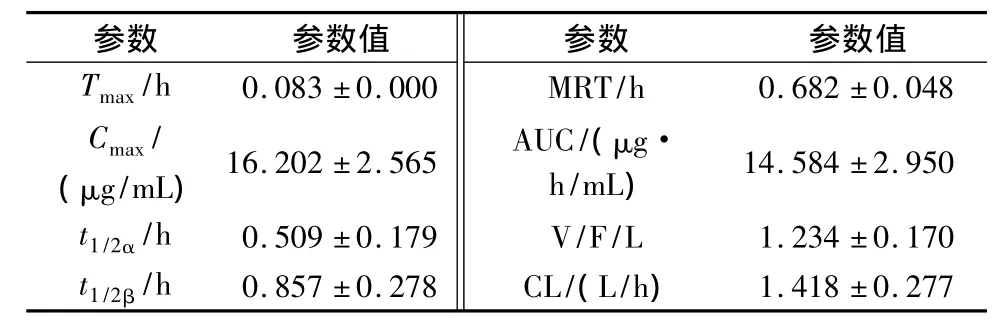
表2 兔眼局部滴用盐酸川芎嗪后盐酸川芎嗪在房水中的药动学参数( ± s,n=6)Tab.2 The pharmackinetic parameters of ligustrazine hydrochloride in aqueous humor of rabbits after topical adm inistration( ± s,n=6)
参数 参数值T max/h 0.083 ±0.000 C max/(μg/mL)16.202 ±2.565 t1/2α/h 0.509 ±0.179 t1/2β/h 0.857 ±0.278参数 参数值MRT/h 0.682 ±0.048 AUC/(μg·h/mL) 14.584 ±2.950 V/F/L 1.234 ±0.170 CL/(L/h)1.418 ±0.277
3 讨论
由于眼内容物的容量有限,可供采集的标本量较少,因此,测定眼组织中某药物成分时,选择的检测方法要求有足够的灵敏度。在含川芎嗪的生物样本中,选用甲醇-水作为流动相测定血中川芎嗪已有报道,对样本的处理以往多选用二氯甲烷或三氯甲烷[6-7],近年也有采用甲醇、甲醇和二氯甲烷混合溶液、乙腈或非那西丁乙腈溶液处理生物样本后对盐酸川芎嗪进行测定的报道[5,8-10]。本实验先将房水样本经高速离心,再经甲醇简单处理后,采用高效液相色谱法测定川芎嗪浓度,比单一离心或甲醇处理样本沉淀蛋白质更完全,杂质峰更少,且样品稀释比(1∶1)好,日内、日间变异小,回收率大于95%。结果表明,该方法具有特异、灵敏、快速等优点,适用于对房水中川芎嗪的测定。
目前,临床应用的川芎嗪制剂主要是注射剂、片剂及胶囊剂,国内外尚未见有川芎嗪眼用制剂的报道。本研究,我们将盐酸川芎嗪制成滴眼液,并通过盐酸川芎嗪滴眼液单剂量滴用兔眼后,采用高效液相色谱法测定了不同时间房水中的川芎嗪,考察了其眼内吸收和代谢情况。实验结果表明,其质量浓度在正常白兔房水呈二室模型,川芎嗪局部应用兔眼后,具有较强的眼内穿透性,能快速进入兔眼房水,5 min达峰浓度,而消除也较快,4 h其浓度已非常低。此结果与以往研究报道[5]的川芎嗪经腹腔注射后在房水中的药代动力学特点相比,眼局部用药后在房水的达峰时间较快,消除速度也稍快。因此,将川芎嗪制成眼局部用缓释制剂,延长其在眼内的滞留时间,是一项值得进一步探讨的课题。
[1]李 勤,李秉芝,刘 宏.川芎嗪注射液的药理作用和临床应用[J].医学综述,2009,15(10):1402-1405.
[2]闻智鸣.川芎嗪、丹参、银杏达莫注射液治疗糖尿病肾病的探讨[J].中成药,2005,27(12):1421-1423.
[3]叶明花.近五年川芎嗪眼科应用研究概述[J].江西中医学院学报,2006,18(3):78-80.
[4]何梅凤,吴 伟,邓新国.川芎嗪在眼科应用的研究进展[J].中草药,2007,38(8):附 4-6.
[5]邓新国,张清炯,贾小芸,等.川芎嗪全身用药在兔眼不同部位的药代动力学结果比较[J].药物分析杂志,2006,26(6):721-725.
[6]张竟超,董伟林.高效液相色谱法测定血中磷酸川芎嗪的浓度[J].天津医科大学学报,2000,6(1):34-35.
[7]冯 悦,王锦玲,马宏敏.川芎嗪在豚鼠血液、脑脊液和耳蜗外淋巴液中的分布[J].听力学及言语疾病杂志,2004,12(2):101-103.
[8]Li L L,Zhang Z R,Gong T,et al.Simultaneous determination of gastrodin and ligustrazine hydrochloride in dog plasma by gradient high-performance liquid chromatography[J].JPharm Biomed A-nal,2006,41(4):1083-1087.
[9]张国平,郭 莹,张 莉,等.灌胃养阴通脑颗粒大鼠血浆中川芎嗪的 HPLC 法测定[J].中草药,2007,38(5):690-692.
[10]耿新辉,陈方剑,于晶晶,等.磷酸川芎嗪滴丸药物动力学研究[J].蚌埠医学院学报,2007,32(4):403-405.

