一枝黄花高效液相指纹图谱研究
茅向军, 许乾丽, 鲍家科, 林瑞超, 戴 忠
(1.贵州省药品检验所,贵州贵阳550004;2.中国药品生物制品检定所,北京100050)
一枝黄花为菊科植物一枝黄花Solidago decurrens Lour.的干燥全草。秋季花果期采挖,除去泥沙,晒干。具有清热解毒,疏散风热的功效。用于喉痹,乳蛾,咽喉肿痛,疮疖肿毒,风热感冒[1-2]。本品也为贵州省少数民族用药[3]。据报道[4-5],一枝黄花中主要含黄酮类、皂苷类等成分。黄酮类化合物,已鉴定的成分有:芦丁、山柰酚-3-芦丁糖苷、异槲皮苷、山柰酚-葡萄糖苷等。对一枝黄花指纹图谱的研究尚未见报道。为了更好地评价一枝黄花药材质量均匀性和稳定性,提高其质量控制标准,本实验收集了不同产地的一枝黄花药材,采用高效液相色谱法,建立了一枝黄花药材的指纹图谱分析方法。
1 仪器与材料
1.1 仪器与试剂 岛津LC-20A液相色谱仪,LC solution色谱工作站,二级管阵列检测器,恒温柱箱,自动进样器;《中药色谱指纹图谱相似度评价系统A版》(国家药典委员会)。
芦丁(批号:100080-200707),绿原酸(批号:110753-200413)对照品均由中国药品生物制品检定所提供,供定量测定用,乙腈和甲醇为色谱纯,水为重蒸馏水,其余试剂均为分析纯。
1.2 药材 10批样品采自贵州、四川、浙江、福建等地,由贵阳中医学院陈德媛研究员鉴定为菊科植物一枝黄花Solidago decurrens Lour.的干燥全草。
2 方法与结果
2.1 色谱条件 Shimadzu VP-ODSC18色谱柱(150 mm ×4.6 mm,5 μm);柱温 30℃;乙腈 -0.4%磷酸(70∶30)为A流动相,0.4%磷酸为B流动相,进行线性梯度洗脱,0~25 min,A由7%线性改变至28%,25~40 min,A 线性改变至35%,40~50 min,A线性改变至64%,50~60 min,A线性改变至100%,保持至70 min;检测波长285 nm;体积流量:1 mL/min;进样量10μL。理论板数按绿原酸计不低于4 000,按芦丁计不低于6 000,色谱图见图1。
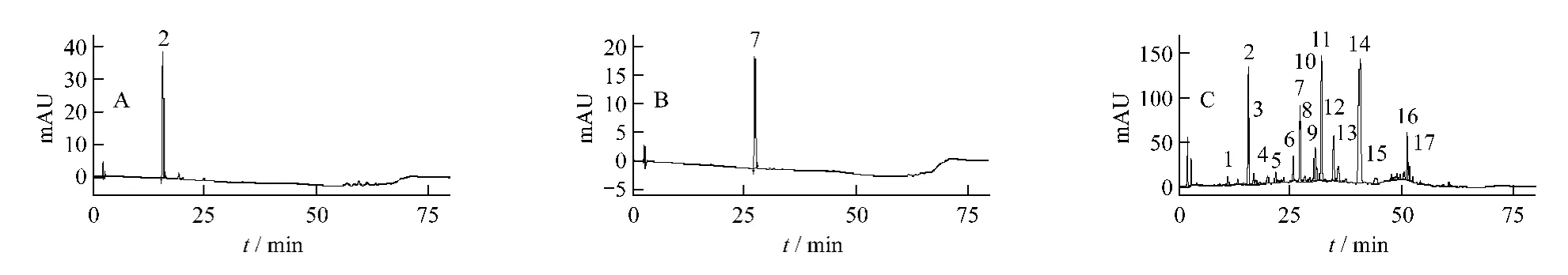
图1 一枝黄花的HPLC图谱Fig.1 HPLC chromatograms of Solidaginis Herba
2.2 对照品溶液的制备 分别精密称取绿原酸和芦丁对照品适量,加甲醇制成质量浓度分别为0.022 6、0.020 69 mg/mL 的溶液,即得。
2.3 供试品溶液的制备 取本品粉末(过3号筛),精密称取2 g,置100 mL具塞锥形瓶中,精密加70%甲醇50 mL,称定质量,加热回流40 min,取下,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,用微孔滤膜(0.45μm)滤过,即得。
2.4 方法学考察
2.4.1 精密度实验 取同一供试品溶液10μL,注入液相色谱仪,连续进样6次,测定峰面积并记录色谱图,结果17个共有峰保留时间和峰面积RSD均小于3%,保留时间和峰面积值均无明显变化,符合指纹图谱技术要求。
2.4.2 稳定性试验 精密吸取同一供试品溶液10 μL,分别于 0、2、6、10、14、18 h 各测定一次。结果17个共有峰的保留时间的RSD均在0.3%以内,峰面积值的RSD均小于3.0%。说明供试品溶液至少在18 h内稳定性良好。
2.4.3 重复性试验 精密称取同一批号一枝黄花6份,按2.3项下方法制备供试品溶液,测定。结果其色谱峰保留时间的RSD均在0.3%以内,峰面积的RSD均在5%以内。
2.4.4 主要色谱峰的建立 分别精密吸取对照品溶液及供试品溶液各10μL,注入高效液相色谱仪,记录60 min的色谱图。检测指认,结果10批一枝黄花药材的指纹图谱,与对照品绿原酸和芦丁的色谱峰相对应的位置上有主要色谱峰,两峰峰面积之和约占总峰面积20%左右。60 min内10批样品有17个共有峰。在2、7、11、14号峰(保留时间约在15.5、27.2、32.0 和 40.7 min)的位置更具特征性,为主要共有峰,2号峰对应为绿原酸的色谱峰,7号峰对应为芦丁的色谱峰。因此,最终确定了17个色谱峰为共有指纹峰,见图1,以7号峰芦丁峰为参比计算,共有指纹峰的相对保留时间见表1,主要共有峰峰面积百分数见表2。
2.4.5 样品指纹图谱相似度分析 将10批药材按上述方法制备供试品溶液,按上述色谱条件进行分析,记录HPLC色谱图,并使用国家药典委员会《中药指纹图谱相似度评价系统》2004年A版软件进行处理,得到标准指纹图谱。见图2,表3。
由以上结果可知10批一枝黄花药材的HPLC图谱的相似度均大于0.8,基本符合中国药典中药质量标准研究制定技术要求,所建立的一枝黄花HPLC对照指纹图谱合格,可作为当地药材的标准图谱。
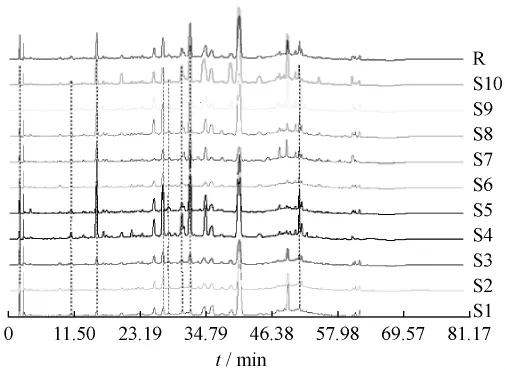
图2 10批一枝黄花的HPLC指纹图谱Fig.2 HPLC fingerprint chromatogram for ten batches of Solidaginis Herba
3 小结与讨论
实验结果显示一枝黄花S4、S5、S7和S8号样品相似度均达到0.90以上,说明这4批药材的指纹图谱具有较高的相似性,其余样品相似度较低,可能与采收时间和成熟程度等因素有关,也说明了中药材成分的复杂性。另外,由于样品采集的地点较少,同一产地的样品数也较少,因此,产地与样品相似度的关系有待进一步的研究。
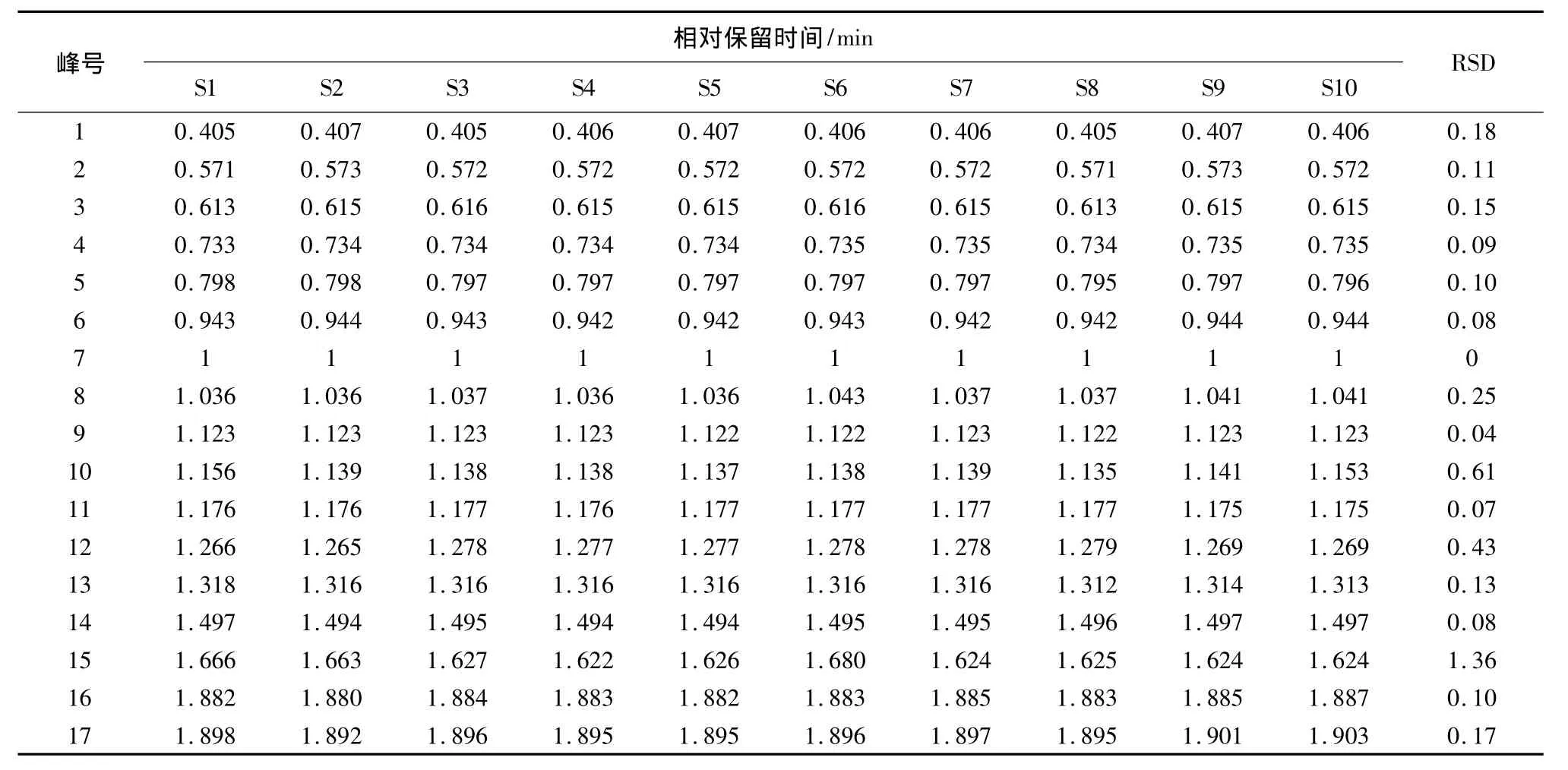
表1 10批一枝黄花样品共有指纹峰的相对保留时间Tab.1 Relative retention time of common fingerprint peaks for ten batches of Solidaginis Herba

表2 一枝黄花指纹图谱主要指纹峰面积的相对百分数Tab.2 Relative percentage content ofmain fingerprint peak areas in HPLC fingerprint chromatogram for Solidaginis Herba

表3 10批一枝黄花药材的相似度结果Tab.3 Sim ilarity evaluation results for ten batches of Solidaginis Herba
在色谱条件优化过程中,考察了甲醇-0.4%磷酸,甲醇 -0.4% 醋酸,乙腈 -0.4%磷酸,乙腈-0.4%磷酸,乙腈-甲醇 -0.4% 磷酸,乙腈-甲醇-0.4%醋酸等系统,最后确定了乙腈-0.4%磷酸系统梯度洗脱的条件,该系统比其它系统分离度好,峰形对称性好,基线稳定;采用二极管阵列检测器对检测波长进行考察,记录190~700 nm范围的HPLC图谱,用等高线法确定285 nm为检测波长,在该波长下一枝黄花色谱中色谱峰较多,基线平稳,信息丰富。
[1]国家药典委员会.中华人民共和国药典:1977年版一部[S].北京:人民卫生出版社,1978:1.
[2]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:3.
[3]贵州省药品监督管理局编.贵州省中药材、民族药材质量标准(2003年版)[M].贵阳:贵州科技出版社,2003:4.
[4]江苏新医学院.中药大辞典:上册[M].上海:上海科学技术出版社,2000:8.
[5]李晓岚,裘名宜,刘素鹏.一枝黄花的化学成分、药理活性及临床应用[J].时珍国医国药,2008,19(1):93.
[6]张 勇,孙冬梅.咽痛灵合剂的薄层色谱鉴别方法研究[J].时珍国医国药,2007,18(11):2811.
[7]徐智勇,崔小兵,李 伟,等.加拿大一枝黄花不同部位总黄酮及芦丁的含量测定[J].中华实用中西医杂志,2008,21(14):1224.
[8]尹雄章,宋娅玲,黄泽中.RP-HPLC法测定一枝黄花中槲皮素的含量[J].中国药师,2007,10(3):259.
[9]石 海,孙传梅,孙 晋,等.一枝黄花抗感颗粒质量标准研究[J].贵阳中医学院学报,2007,29(2):20.
[10]史秀峰,谢 燕,李国文.一枝黄花漱口液质量标准研究[J].中南药学,2008,6(2):195.

