强碱性阴离子交换树脂在浓海水提溴中的应用
王滢秀,毕彩丰,赵 宇,左 健,孙建强
(中国海洋大学化学化工学院海洋化学理论与工程技术教育部重点实验室,山东青岛266100)
强碱性阴离子交换树脂在浓海水提溴中的应用
王滢秀,毕彩丰**,赵 宇,左 健,孙建强
(中国海洋大学化学化工学院海洋化学理论与工程技术教育部重点实验室,山东青岛266100)
研究201×7、201×4、D201 3种阴离子交换树脂对人工浓海水中的溴离子吸附性能,结果表明,201×7树脂的吸附效果最好。该树脂的静态饱和吸附量达到25.94 mg·g-1,流速为2.3 mL·min-1时的动态饱和吸附量为13.42 mg·g-1,因此选择201×7树脂作为吸附剂。通过静态吸附实验,测得298 K时吸附速率常数k298=1.7×10-3s-1;热焓ΔH=67.75 kJ·mol-1;在解吸过程中,确定了柠檬酸钠溶液作为解吸剂。201×7树脂吸附溴离子的过程符合Freundlich吸附等温式。通过动态吸附实验,研究了海水流速对201×7树脂吸附溴离子的影响。探讨了201×7树脂吸附溴离子的机理,结果表明,溴离子在201×7树脂上的吸附机理主要是Br-与—N+(CH3)3之间的静电作用。
201×7树脂;溴离子;浓海水;吸附;解吸
溴被广泛应用于医药、农药、染料、感光材料、制冷剂、阻燃剂、防爆剂、国防、钻井等多个领域,是一种重要的工业原料。地球上99%的溴都存在于海水中,海水中溴浓度约为65 mg·L-1。目前世界溴产量的60%以上来源于海水,海水提溴成了提溴工业的重要支柱。
海水淡化后会产生大量浓海水,这种浓海水中含有丰富的元素和化合物资源。目前,对浓海水的处理是直接排入大海,不仅造成资源浪费,还会污染环境。因此,从海水淡化后产生的浓海水中提溴,既可以实现资源再利用,还可以保护环境[1,10]。
目前国际上研究的提溴方法大体可以分为:空气吹出法、蒸汽蒸馏法、溶剂萃取法、离子交换树脂法、吸着剂法、膜分离法等6种。我国90%以上溴素生产采用空气吹出法,此方法需要消耗大量的酸液,且流程复杂,成本较高。而离子交换树脂法可以克服空气吹出法的缺点,适于含溴量低的原料液,可以直接生产溴化物产物,具有投资少、易操作、流程少的优点。因此,利用离子交换树脂吸附海水中溴离子的方法提取溴具有重要的学术价值和应用前景[2-5]。
传统的树脂吸附法的工艺流程包括:酸化、氧化、吸附、解吸附等过程,即是将海水酸化后,利用氯将其中的溴离子氧化为单质溴,然后利用树脂对其进行吸附,此方法同样需要消耗大量酸液,成本高,工艺复杂。本文采用价廉易得的201×7强碱性阴离子交换树脂吸附浓海水中的溴离子,研究了该树脂对溴离子的吸附性能和吸附机理。结果表明,201×7树脂对溴离子具有良好的吸附性,避免了大量酸的消耗,工艺流程简单,降低了生产成本,有望为其工业应用提供一条新途径[6-10]。
1 实验部分
1.1 仪器及试剂
201×7、201×4强碱性苯乙烯系阴离子交换树脂、D201大孔强碱性阴离子交换树脂,蚌埠市天星树脂有限责任公司生产。其他试剂均为分析纯。
WFJ2000型紫外可见分光光度计(上海尤尼柯仪器有限公司);AVATAR-360红外光谱分析仪(美国NICOL ET公司);Φ8.5×275 mm离子交换柱。
1.2 树脂预处理
取适量树脂于烧杯中,用4倍量去离子水浸泡24 h以上,使之充分溶胀,然后用去离子水清洗至流出液澄清。再用1.0 mol·L-1NaOH溶液浸泡8 h以上,水洗至中性。之后用2.0 mol·L-1HCl溶液浸泡8 h以上,水洗至中性,使树脂充分转为Cl型,晾干备用[11]。
1.3 人工海水的配制
由于实验需要,本文采用浓海水配方[1,10]如表1所示,按表1溶解下述试剂,然后加水至总重量为10 000 g。

表1 10 000 g人工海水配方Table 1 Formula of artificial seawater
1.4 实验方法
1.4.1 静态吸附实验 取一定量已转型的树脂于锥形瓶中,加入一定量含溴离子质量浓度为128.26 mg·L-1的人工浓海水,298 K下,于恒温摇床上以120 r/min的转速吸附,每隔一定时间测定其中的溴离子浓度,计算溶液中所含溴离子的质量,直至溶液中溴离子的质量不再减少。累计时间,可得各树脂对人工浓海水的静态饱和吸附时间。
取一定量已转型的树脂于锥形瓶中,加入一定量含溴离子质量浓度为128.26 mg·L-1的人工浓海水, 298 K下,于恒温摇床上以120 r/min的转速振荡至饱和吸附,取样0.5 mL分析测定溴离子浓度。绘制静态吸附曲线,并利用公式计算静态吸附量Q、吸附率E和分配比D:
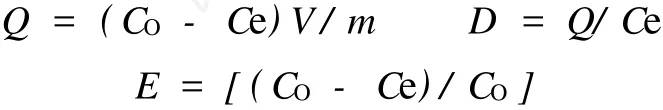
式中,CO是起始溶液中溴离子的质量浓度(mg·L-1); Ce是平衡溶液中溴离子的质量浓度(mg·L-1);V是溶液的体积(mL);m是树脂的质量(g)。
1.4.2 动态吸附实验 准确量取一定量树脂装入离子交换柱中,将人工海水以一定流速通过离子交换柱,按一定体积定容每阶段流出液,测定溶液中溴离子的浓度,利用公式计算动态吸附量Q′,绘制动态吸附曲线。
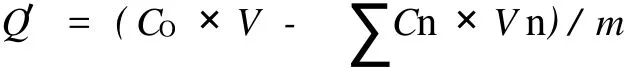
式中,CO为浓海水中溴离子的初始浓度;V为通过海水的总体积;Cn为每阶段流出液的溴离子浓度; Vn为每阶段流出液的体积。
1.4.3 解吸附实验 取一定量树脂,加入一定量人工海水,按静态吸附实验进行,测定平衡后溴离子浓度。分离出水相,向吸附饱和后的树脂中加入一定量解吸溶液,振荡平衡后测定溶液中溴离子浓度。
1.4.4 树脂吸附机理表征 取适量未吸附溴离子和已吸附饱和的树脂,晾干并经低温干燥后,研磨成粉末,用KBr压片法,摄制红外谱图。
1.4.5 分析方法 采用甲基橙分光光度法测定溴离子质量浓度[9-10,12]。 D201大孔强碱性阴离子交换树脂和201×4强碱性苯乙烯系阴离子交换树脂进行实验,3种树脂的功能基均为—N+(CH3)3。
取经处理过的各树脂1.0 g,加入300 mL含溴离子质量浓度为128.26 mg·L-1的人工浓海水,298 K下,于恒温摇床上固定转速至吸附饱和,取0.5 mL溶液测定溴离子浓度,计算各树脂的饱和吸附量,结果见表1。从表1结果表明,201×7树脂对人工海水中的溴离子吸附量优于其他2种树脂,达到25.94 mg·g-1树脂,并且饱和吸附时间也较短,因此以下实验均采用201×7树脂进行。

表2 3种树脂对溴离子的饱和吸附量Table 2 Capacities of static saturation adsorption for bromid ion in seawater by three resins
2 结果与讨论
2.1 树脂的选择
本实验选用了文献报道较多的对溴有较好吸附效果的树脂:201×7强碱性苯乙烯系阴离子交换树脂、
2.2 201×7树脂的静态吸附实验
2.2.1 静态饱和吸附量 取201×7湿树脂1.0 g,分次加入已知质量浓度的人工海水,在298 K下以120 r/min的转速吸附至饱和,取0.5 mL溶液测定溴离子的质量浓度,换算成溶液中的溴离子总量,直至溴离子总量不再减少。经累计计算,可得201×7树脂对人工海水中溴离子的静态饱和吸附时间为40 min,静态饱和吸附量为25.94 mg·g-1。
2.2.2 吸附速率曲线及速率常数的测定 取1.0 g 201×7树脂,在298 K 300 mL含溴离子质量浓度为128.26 mg·L-1的人工浓海水中进行吸附实验。每隔一定时间测定溶液中溴离子的含量,直至平衡。经体积校正后计算反应时间为t时每克树脂的吸附量Qt,绘制Qt与时间t的吸附速率曲线,如图1所示。将实验数据用公式-ln(1-F)=kt处理,式中F=Qt/Q∞, Qt和Q∞分别为反应时间t和吸附平衡时每克树脂的吸附量,k是吸附速率常数。以-ln(1-F)对t作图,如图2所示,由直线斜率求得201×7树脂吸附溴离子的表观速率常数k298=1.7×10-3s-1。经线性拟合求得相关系数R2=0.996 3。Boyd等认为若-ln(1-F)~t成线性关系,说明液膜扩散为吸附过程的主控步骤[13]。
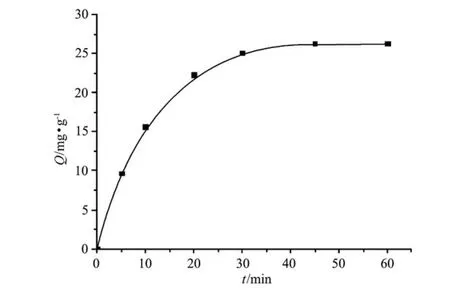
图1 吸附速率曲线Fig.1 Sorption rate curve
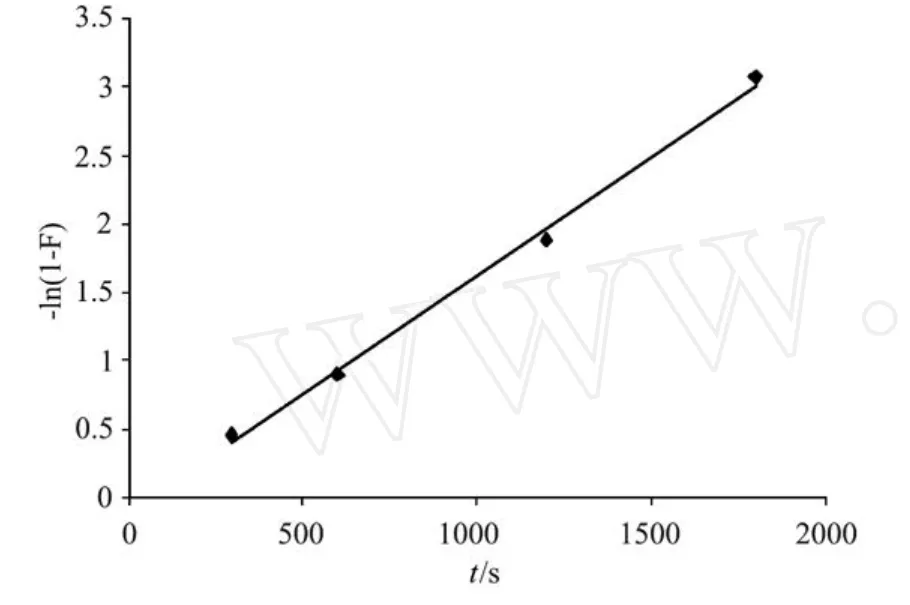
图2 速率常数的测定Fig.2 Determination of apparent rate constant
2.2.3 等温吸附曲线 取5份0.5 g 201×7树脂分别于具塞锥形瓶中,在298 K下,各加入300 mL含溴离子质量浓度分别为60、80、100、120、140 mg·L-1的人工海水中吸附至平衡。测定平衡浓度Ce(mg·L-1),换算成相应的吸附量Q(mg·g-1)。按照Freundlich等温吸附公式Q=K(Ce)1/n,式中K、1/n为Freundlich常数,两边同时取对数得到公式lgQ=(1/n)lgCe+lgK,以lgQ对lgCe作图,得到一条直线,结果如图3所示,直线斜率为1/n=0.128 2,相关系数R2=0.982 2。

图3 201×7树脂对溴离子的等温吸附曲线Fig.3 Freundlich isotherm curve
由图可知,201×7树脂对人工海水中溴离子的吸附行为较符合Freundlich吸附等温式。实验中得到1/n=0.128 2,即n=7.8,n值在2~10之间,表明201×7树脂对人工海水中溴离子的吸附容易进行[14]。2.2.4温度对吸附的影响及热焓的测定 取4份1.0 g 201×7树脂,在300 mL含溴离子质量浓度为128.26 mg·L-1的人工海水中吸附至平衡,测得温度在288、298、308、318 K时树脂吸附溴离子分配比的变化。以lgD对1/T×103作图,结果如图4所示,直线相关系数R2=0.999 1。
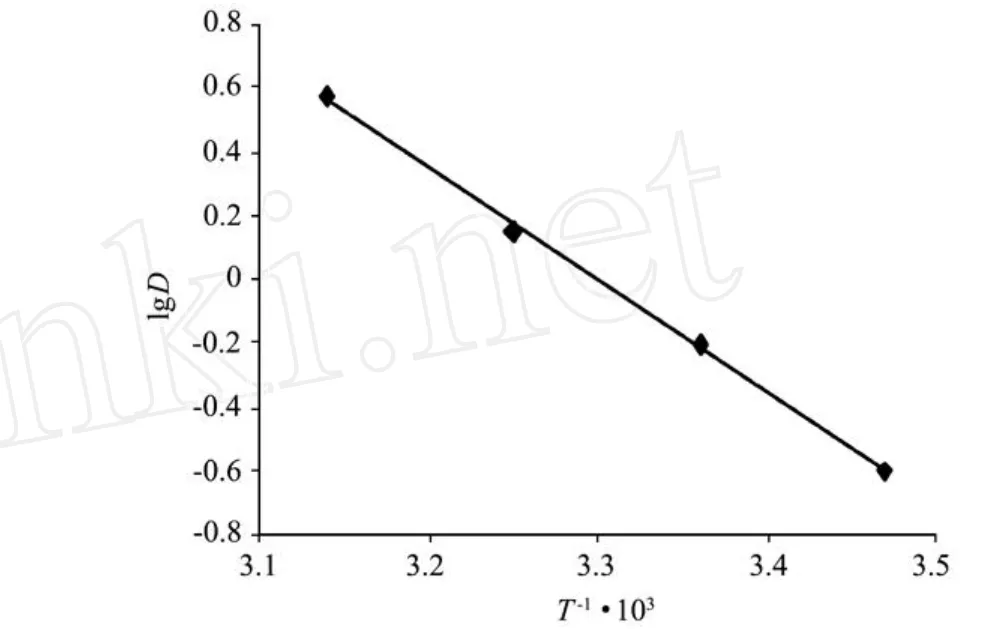
图4 温度对分配比的影响曲线Fig.4 Influenxe of temperature on distribution ratio
由图可知,在288~318 K温度范围内,升高温度对吸附有利。又根据温度系数法公式并根据图4中的直线斜率K=-3.538 2,求得ΔH= 67.75 kJ·mol-1。因此可知201×7树脂对人工海水中溴离子的吸附过程是吸热过程。
2.3 201×7树脂的动态吸附实验
2.3.1 动态饱和吸附量 取201×7树脂3.0 g,装入离子交换柱中,然后将含溴离子质量浓度为128.26 mg·L-1的人工浓海以一定的流速通过离子交换柱,定容流出液。从每阶段的流出液中取0.5 mL溶液测定溴离子的质量浓度,直至流出液质量浓度与流入液质量浓度相同时停止实验,绘制流出曲线,如图5所示。经累计计算,可得该流速下该树脂的动态饱和吸附量为13.42 mg·g-1。
2.3.2 流速对树脂吸附性能的影响 取201×7树脂
3.0 g装入离子交换柱中,在常温下通入含溴离子质量浓度为128.26 mg·L-1的人工浓海水,调节流速分别为2.3、3.4、5.4 mL·min-1,通入量均为1 200 mL,定容流出液,测定溴离子浓度,绘制流出曲线,结果如图6所示。
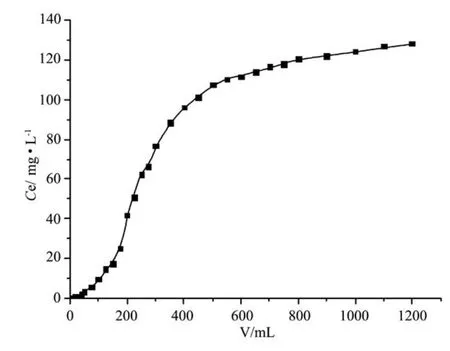
图5 动态吸附的流出曲线Fig.5 Flow curve of dynamic adsorption
由图6可知,不同流速时,201×7树脂对浓海水的吸附情况不同:流速越快,吸附的时间越短,树脂的吸附量越少,处理浓海水的量越小,穿透点也越提前。因为流速增快,溶液与树脂床接触时间减少,使离子交换进行不彻底,不能充分吸收就流出树脂床,故穿透点提前,树脂吸附率下降。
2.4 解吸附实验

图6 不同流速的吸附曲线Fig.6 Flow curve of dynamic adsorption in different velocity
2.4.1 解吸剂的选择 取已吸附溴离子的201×7树脂各1.0 g,分别加入1 mol·L-1NaCl溶液、1 mol·L-1NaOH溶液、1 mol·L-1KNO3溶液和1 mol·L-1柠檬酸钠溶液各300 mL,于恒温摇床上解吸40 min后,取0.5 mL溶液测定溴离子质量浓度,计算解吸率,结果见表3。
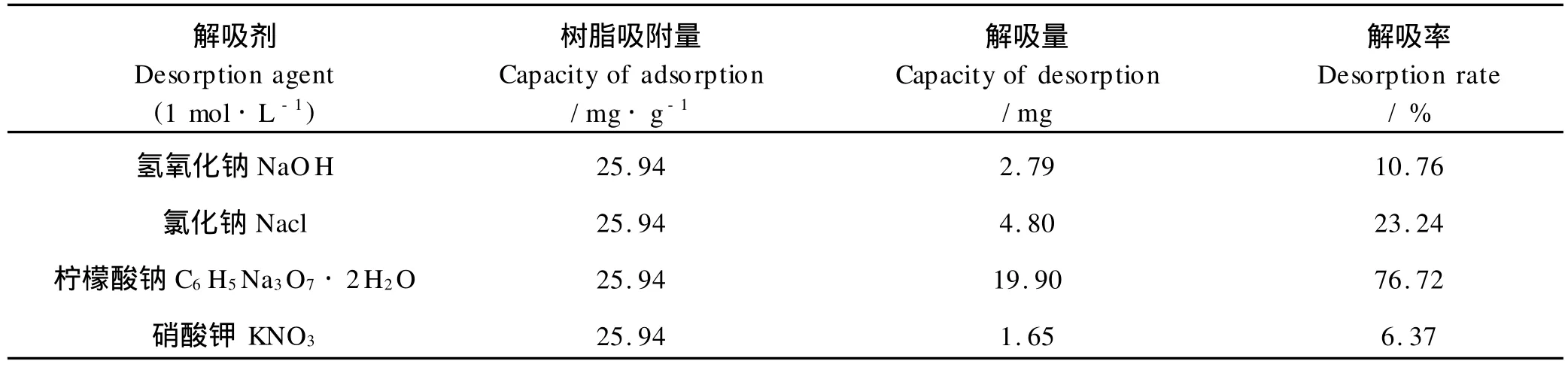
表3 各种解吸剂的解吸结果Table 3 Desorption results of different desorption agents
由表3可知,1 mol·L-1柠檬酸钠溶液对201×7树脂的解吸率最高,故选择柠檬酸钠为解吸剂。
2.5 201×7树脂吸附溴离子的红外谱图
根据实验方法对吸附溴离子前后的201×7树脂摄制红外谱图,如图7、8所示。
通过对比吸附溴离子前后201×7树脂红外谱图的变化及参考文献[15-18],可以看出,201×7树脂吸附溴离子前后的红外谱图基本一致,主要特征峰的位置及峰形变化不大。从而排除了树脂与溴离子发生化学反应的可能性[19]。根据强碱性阴离子交换树脂对常见阴离子的亲和顺序:柠檬酸根>SO42->CrO42->I-> HSO4->NO3->C2O42->Br->CN->HSO3-> NO2->Cl->HCOO->CH3COO->OH->F-可知,树脂对Br-比对Cl-的亲和能力强[20],再根据树脂结构可以证明,溴离子在201×7树脂上的吸附机理主要是Br-与—N+(CH3)3之间的静电作用。

图7 201×7树脂吸附溴离子前红外谱图Fig.7 Infrared spectrum of 201×7 resin before adsorbing bromine ion
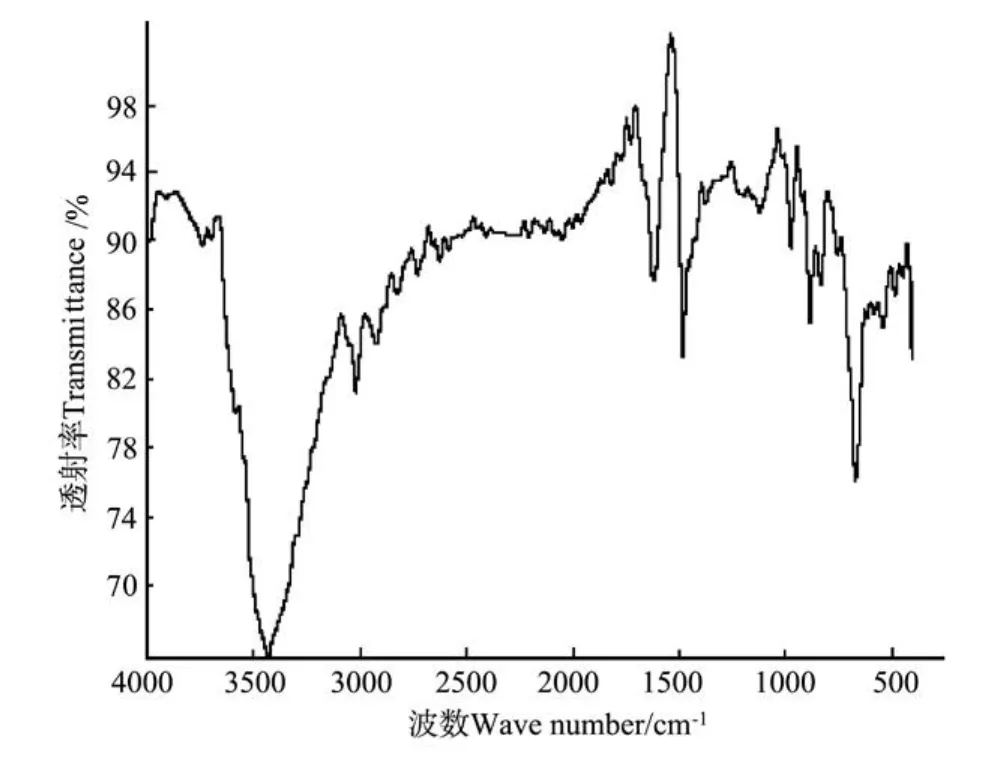
图8 201×7树脂吸附溴离子后红外谱图Fig.8 Infrared spectrum of 201×7 resin after adsorbing bromine ion
3 结论
本文通过研究201×7树脂对人工浓海水中溴离子吸附、解吸性能及吸附机理,得到如下结论:
(1)通过实验确定了201×7强碱性阴离子交换树脂是一种较适合于吸附海水中溴离子的树脂。该树脂在298K时对海水中溴离子的静态饱和吸附量为25.94 mg·g-1。流速为2.3 mL·min-1时的动态饱和吸附量为13.42 mg·g-1。
(2)通过静态吸附实验测得,在298 K时,201×7树脂对人工海水中溴离子的吸附速率常数k298=1.7×10-3s-1;热焓ΔH=67.75 kJ·mol-1。201×7树脂对人工海水中溴离子的吸附行为较符合Freundlich吸附等温式,吸附容易进行。
(3)通过动态吸附实验可知,海水流速越快,穿透体积越小,树脂的吸附量越小。
(4)实验确定了一种解吸效果良好的解吸剂为柠檬酸钠,解吸浓度为1 mol·L-1,解吸率达76.72%。
(5)通过对比吸附溴离子前后201×7树脂的红外谱图变化,可知201×7树脂与溴离子没有发生化学反应,也没有官能团的变化,因此可以推测,溴离子在201× 7树脂上的吸附机理主要是Br-与—N+(CH3)3之间的静电作用。
[1] 张宁,苏营营,苏华,等.冷冻离心法处理浓海水研究[J].盐业与化工,2008,37(4):25-28.
[2] 王和锋,孙婷,黄根华.海水提溴技术的研究进展[J].中国新技术新产品,2009:02-02.
[3] 闫树旺,安莲英,唐明林,等.离子交换法从卤水富集溴的技术进展综述[J].海湖盐与化工,1994,23(6):14-17.
[4] 刘兴芝,蒋维棋,宋玉林.D201BR树脂的寿命及应用于海水提溴的研究[J].离子交换与吸附,1952,8(2):183-187.
[5] 毕东峰,倪其明.D201BR树脂的性能及应用于苦卤提溴的研究[J].离子交换与吸附,1990,6(2):131-136.
[6] 王汝志,王伟.空气吹出法提溴工艺的两点改进[J].海盐湖化工,1998,28(1):31.
[7] 郝福锦,吕晓龙,王国强,等.膜法提溴过程的研究与对比[J].化工进展,2009,28(6):927-932.
[8] 朱昌洛,寇建军.树脂吸附法由卤水中提溴[J].矿产综合利用, 2003(5):13-16.
[9] 侯杰.三种壳聚糖对海水溴离子的吸附性能的研究[D].青岛:中国海洋大学,2009.
[10] 谢海英.D201大孔强碱性阴离子交换树脂从浓海水中提溴的研究[D].杭州:浙江工业大学,2009.
[11] 王广珠,汪德良,崔焕芳.[M].北京:化学工业出版社,2005.
[12] 瞿建国,冯敏.甲基橙分光光度法测定环境中空气及工业废气中的游离溴[J].环境污染与防治,2000,22(3):44-46.
[13] Boyd G E,Adamson A W,Myers Jr.L S.The exchange adsorption of ions from aqueous solutions by organic zeolitesⅡ.kinetics[J].Am Chem Soc,1947(69):2836-2848.
[14] 北川浩,铃木廉一郎.吸附的基础与设计[M].鹿政理译.北京:化学工业出版社,1983:28-29.
[15] 孟令芝,龚淑玲,何永炳.有机波谱分析[M].武汉:武汉大学出版社,2003:194-249.
[16] 廖赞,兰新哲,朱国才.201×7强碱性阴离子交换树脂对氰化物的吸附性能及吸附机理[J].分析与环保,2008,29(7):46-50.
[17] 施林妹,莫建军.D201×4树脂对金(Ⅲ)的吸附[J].无机化学学报,2007,5:911-914.
[18] 王慧君,熊春华,姚彩萍,等.D201×4树脂对钼(Ⅵ)的性能及机理[J].有色金属,2006,58(4):29-32.
[19] 谢祖芳,何星存,夏金虹,等.苦味酸在聚酰胺树脂上的吸附热力学及动力学[J].化学研究,2003,14(4):53-56.
[20] 许晓文,杨万龙,沈含照.定量分析化学[M].天津:南开大学出版社,1991:507-521.
[21] 姜志新,谌竟清,宋正孝.离子交换分离工程[M].天津:天津大学出版社,1992.
Abstract: The paper primarily discusses the adsorption property of 201×7、201×4 and D201 anion exchange resins for bromid ion in dense seawater.The results show that the 201×7 resin has a good adsorptivity for bromid ion.The capacity of static saturation adsorption for bromid ion in seawater is 25.94 mg·g-1,and the capacity of dynamic saturation adsorption at a velocity is 13.42 mg·g-1.Therefore,201×7 strongly basic anion exchange resin is selected for bromid ion adsorption.The absorption rate constant isk298= 1.7×10-3s-1.TheΔHof adsorption is 67.75 kJ·mol-1.Through the experiment,sodium citrate is selected as desorption agent.The absorption of bromid ion on 201×7 resin follows the Freundlich isotherm. Furthermore,the influence of flow rate on adsorption is examined.The paper primarily discusses the adsorptive mechanics of 201×7 resin for bromid ion.It shows that the adsorptive mechanics of 201×7 resin for bromid ion is electrostatic effect between Br-and-N+(CH3)3.
Key words: 201×7 resin;bromid ion;dense seawater;adsorption;desorption
责任编辑 徐 环
The Application of Strongly Basic Anion Exchange Resin in Bromine Extraction from Dense Seawater
WANG Ying-Xiu,BI Cai-Feng,ZHAO Yu,ZUO Jian,SUN Jian-Qiang
(Key Laboratory of Marine Chemistry Theory and Technology,Ministry of Education,College of Chemistry and Chemical Engineering,Ocean University of China,Qingdao 266100,China)
TQ085+.47
A
1672-5174(2011)06-081-06
2010-08-30;
2011-04-06
王滢秀(1986-),女,硕士生。E-mail:wyx1986120@163.com
E-mail:bcfeng@ouc.edu.cn

