肺原发恶性纤维组织细胞瘤20例
黄崇标 辛亮 崔焱 齐大亮
恶性纤维组织细胞瘤(malignant fibrous histiocytoma,MFH)起源于间叶组织,通常好发与四肢和腹膜后,以席纹状排列的多形性纤维细胞和组织细胞为特点,是成人最常发生的软组织肉瘤之一,约占所有软组织肉瘤的10%[1]。虽然75%深部MFH可以转移到肺部[2],但是肺原发的MFH实为罕见,约占肺恶性肿瘤的0.02%-0.30%[3]。检索文献发现国内仅报道百余例[4,5]。
1 材料与方法
1.1 一般情况 天津医科大学附属肿瘤医院胸外科自1986年3月-2008年12月共收治肺原发恶性纤维组织细胞瘤28例,其中病历资料完整的20例,男性15例,女性5例。年龄范围40岁-76岁,中位年龄61.6岁。病例入组要求:有完整的临床资料,包括一般情况、病理诊断及治疗方式,能随访至患者目前生存状态或者死亡时间。
1.2 方法 全部患者均经手术病理诊断为肺原发MFH。20例患者中16例行根治性切除术(其中肺叶切除术14例,全肺切除术2例),3例行姑息性切除术,1例行开胸切检术。9例行术后辅助化疗,方案为铂类联合阿霉素、依托泊甙、环磷酰胺、氮唏咪胺等,化疗2个-6个周期。
1.3 统计学处理方法 采用SPSS 16.0软件进行统计学分析。生存期计算自手术日起至死亡时间或者末次随访日(2010年10月)。用Kaplan-Meier曲线及COX回归分析性别、肿瘤大小、肿瘤分型及化疗对术后生存期的影响,P<0.05为有统计学差异。
2 结果
2.1 临床特点 本组患者主要症状为咳嗽咳痰(7/20)、痰中带血(4/20)、胸痛(3/20)、胸闷(2/20)、发热等(2/20),有2例患者无任何症状和体征,为体检时发现。17例行痰细胞学检查,全部为阴性。12例行纤维支气管镜检查,1例管腔受压狭窄,但咬检结果为阴性。20例全部行胸部CT检查,中心型6例,周围型14例,右上肺3例,右中叶4例,右下肺6例,左上肺2例,左下肺5例,肿瘤大小2.0 cm-15.0 cm,直径5 cm以下的8例,直径在5 cm-10 cm之间的8例,10 cm以上的4例。14例边缘较规整,2例边缘可见毛刺征,1例见浅分叶,1例多发肺内转移,1例胸腔积液,1例侵犯肋骨。12例行碘普罗胺造影剂强化CT检查,均有中度强化,2例中心坏死。4例纵隔淋巴结肿大。
全部病例均经术后病理诊断为肺原发性MFH。其中,席纹状-多形性型16例,粘液型3例,炎性型1例。15例手术标本行免疫组化检查,结果为CD68(+),Vimentin(+)。4例纵隔淋巴结肿大病例中2例有纵隔淋巴结转移。
2.2 术后生存率 全组无手术死亡。采用门诊定期复查、信访和电话相结合的方式,自手术日起随访至患者死亡或者截止日期2010年10月。中位随访期3年。全组生存期3个月-85个月,中位生存期12.5个月,1年、2年及3年生存率分别为55.0%、25.0%和10.0%。1例患者生存期达到85个月。患者死亡原因分别为:局部复发6例,胸膜转移2例,脑转移3例,全身广泛转移7例及其他原因2例。生存曲线见图1所示,从该生存曲线可以看出,生存率在10个月-25个月间下降趋势最明显,说明肺原发性MFH患者术后在10个月-25个月间复发转移乃至死亡的风险最大。
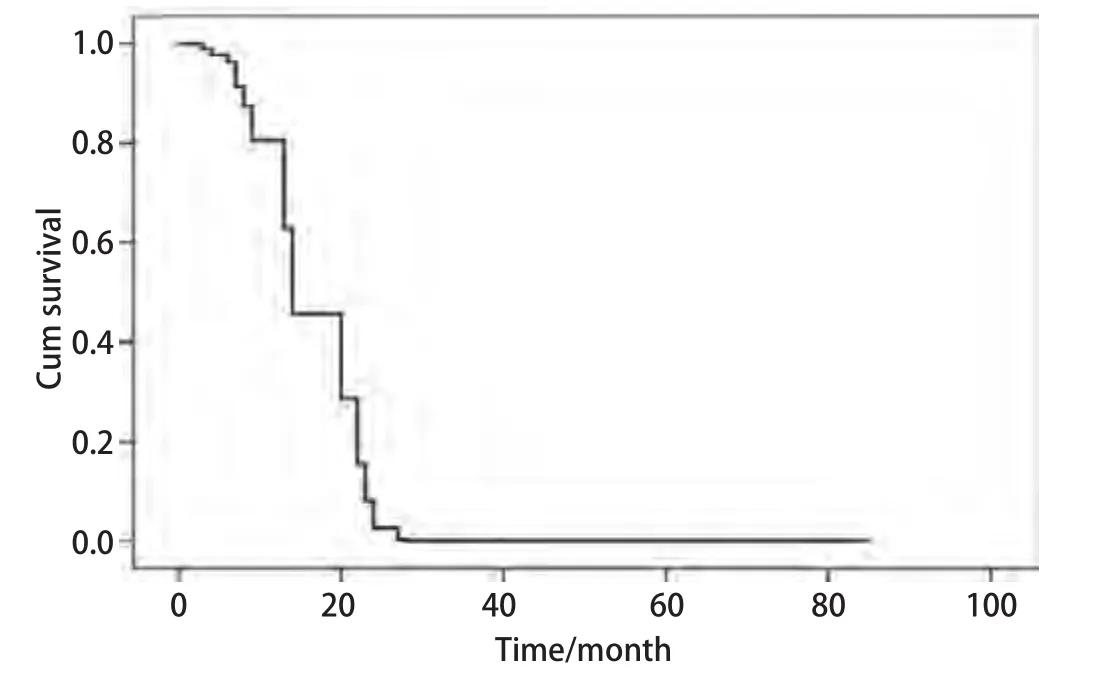
图1 全组肺原发性MFH生存曲线Fig 1 Survival curve of 22 MFH patients
2.3 影响肺原发MFH预后的因素分析 对全组肺原发MFH患者进行单因素分析,结果显示,影响其中位生存期的因素有肿瘤大小(χ2=12.255, P=0.002)及肿瘤分型(χ2=22.819, P=0.021),肿瘤<5 cm组2年生存率为50%,而肿瘤≥5 cm组2年生存率为8.3%;周围型和中心型2年生存率分别为28.6%和6.7%。患者性别、化疗对中位生存期无明显影响(表1)。对影响肺原发MFH患者预后的单因素进行COX多因素综合分析(表2),结果显示肿瘤大小及位置为肺原发MFH患者生存期的独立影响因素。
3 讨论
恶性纤维组织细胞瘤是一种高度恶性的起源于间叶组织的肿瘤,首先由O’Brien等[6]在1964年作为一种独立类型的恶性肿瘤来进行描述。MFH好发于四肢、躯干及腹膜后,是成人最常发生的肉瘤之一,约占所有软组织肉瘤的10%。虽然肺脏是MFH最容易转移的器官之一,但是肺原发性MFH非常罕见,文献报道期发病率约为肺原发恶性肿瘤的0.02%-0.30%[3],我院胸外科从1986年-2008年间共收治肺部恶性肿瘤13,000余例,肺原发MFH占肺部恶性肿瘤的0.21%。肺原发MFH以中老年男性多见,儿童病例尚未见报道。本组患者中位年龄为61.6岁,男性患者占75.0%。肺原发MFH常见的临床症状有咳嗽咳痰、咯血(痰中带血)、胸痛、胸闷及发热等,一些少见的症状,如肺栓塞、低血糖、肥大性肺性骨关节病及粒细胞缺乏症等也有所报道[7],但这些均无特异性,加之影像学检查也无特异性表现,因此,一般术前较难诊断,容易误诊为原发性肺癌,本组病例术前均未能确诊,有18例术前考虑为原发性肺癌。MFH起源于间叶组织,在气管及肺泡外生长,因此,痰脱落细胞学检查及气管镜刷片细胞学检查结果一般为阴性。
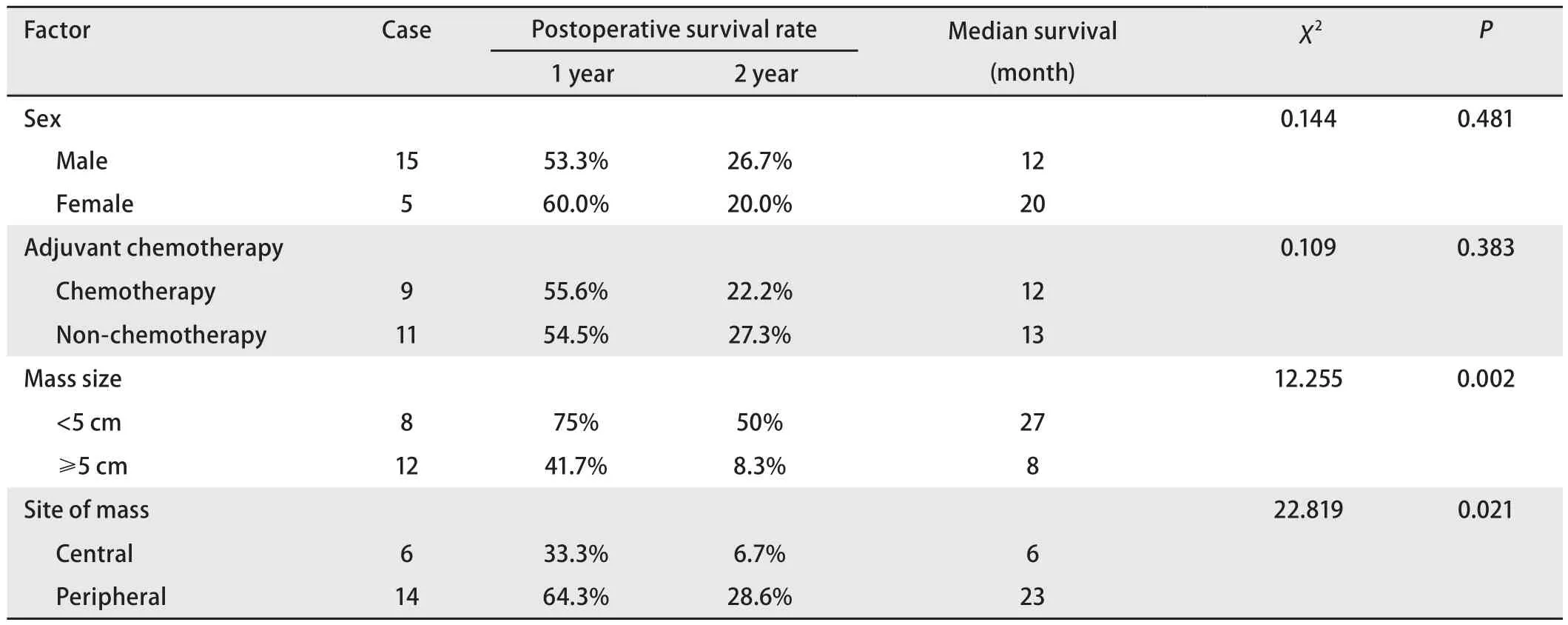
表1 影响肺原发MFH患者预后的单因素分析Tab 1 Monofactorial analysis of prognosis of MFH patients

表2 影响肺原发MFH患者生存期的多因素分析Tab 2 Multivariate COX regression analysis of OS of MFH patients
本组患者肿瘤大小2.0 cm-15 cm,直径5 cm的占60%,周围型占70%,大多为形态规则界限较清楚的实性肿物,这可能与肿瘤生长速度较快,成膨胀性生长形成假包膜有关。肺原发MFH较少发生纵隔及肺门淋巴结转移,本组仅4例出现纵隔淋巴结肿大,术后病理证实仅2例阳性,与文献报道较为一致。MFH容易侵犯邻近组织及脏器,本组患者有1例发生胸膜转移,1例肺内多发转移,1例侵犯肋骨。12例行强化CT检查发现均有中度强化。总结本组病例,肺原发性MFH的一些影像学特点可能有助于术前临床诊断:瘤体较大的实性肿物;以中下叶多见、多为外周型;边缘较光滑形态较规整;大多呈中度强化;较少发生纵隔淋巴结转移。
肺原发MFH显微镜下以席纹状的多形性纤维细胞及组织细胞为特征,其病理表现和其它部位的MFH无明显差异,其组织起源被认为是原始的间质细胞向不同方向分化形成。MFH缺乏特异性抗原,但是MFH瘤细胞一般对CD68、Vimentin呈阳性反应,而对CK、Actin、S100、Desmin呈阴性反应[1],可以用免疫组化鉴别MFH和一些其它的软组织肉瘤。MFH的诊断需要取材充分,一般的穿刺取材较难和其它软组织肉瘤鉴别[3]。
肺原发MFH较少发生淋巴结转移,血行转移较常见,患者死因多为远处转移或者局部复发。最容易发生远处转移的器官为脑和骨。肺原发MFH的预后较差,文献报道相差较大,徐志龙等[8]报道肺原发MFH的1年生存率为60%,3 年生存率为42%,5年生存率为33%;而Rzyman等[9]报道大部分患者于术后1年内死亡。本组患者1年、3年及5年生存率分别为55.0%、10.0%和5.0%,大部分患者于2年内死亡,患者死亡原因分别为远处转移和局部复发。有学者[10]认为术后辅助放疗的作用有限,但是可用于病变侵及胸壁及非根治性手术的术后治疗。另有学者[11]认为术后辅助化疗有助于延长患者生存期。本组患者进行单因素分析后发现术后辅助化疗并没有明显改善预后。鉴于病例数较少,更确切的结论需要多中心大样本进一步研究。MFH的主要治疗手段目前仍然是手术,改善预后关键在于早期发现及及时治疗[12]。本组病例发现,<5 cm组的预后明显较≥5 cm组的好,多因素COX分析肿瘤大小为影响预后的独立因素,这可能是因为瘤体较小一般说明病程仍处于早期,发生侵犯附近脏器和远处转移的几率较小,根治的可能性较大。肿瘤的位置是另一个影响预后的独立因素,周围型较中央型患者中位生存期明显延长。这可能是因为中央型患者更容易早期侵犯气管、大血管等重要脏器。
综上所述,肺原发MFH是一种高度恶性的肉瘤,预后差。无特异性临床表现,早期诊断较困难。早期行根治性手术是取得较好疗效的关键,辅助性放化疗疗效尚不确切。

