硅锌矿在(NH4)2SO4-NH3-H2O体系中的浸出机理
刘智勇, 刘志宏, 曹志阎, 李启厚, 杨天足
(中南大学 冶金科学与工程学院,长沙 410083)
氧化锌矿属次生矿,通常产于铅锌硫化矿床的氧化带中。目前,锌主要以硫化矿为原料,采用湿法生产。随着硫化锌矿资源的消耗,氧化锌矿已成为锌冶金的重要原料。
我国西南、西北等地氧化锌矿资源丰富,但其品位低、难选、高硅、高碱性脉石,且含锌矿物组成复杂,主要有菱锌矿(ZnCO3)、水锌矿(Zn5(CO3)2(OH)6)、异极矿(Zn4(Si2O7)(OH)2·H2O)和硅锌矿(Zn2SiO4)等多种属典型的难冶锌资源。
氧化锌矿的处理工艺有高温还原挥发以及硫酸、苛性碱和氨浸出等多种。高温还原挥发可实现锌的富集,但能耗高、设备寿命短及环境污染严重[1−4]。在氧化锌矿硫酸液的浸出中,硅部分溶解形成溶胶,导致液固分离困难,需控制浸出液中硅酸的聚合,部分工艺已用于生产,如快速浸出、中和絮凝工艺等[5−8];部分仍处于研究阶段,如微波辅助浸出[9]、高压酸浸工艺[10]。这些方法皆可获得易于液固分离的矿浆,但浸出条件控制严格、技术难度大。此外,由于酸耗过高,高碱性脉石的低品位氧化锌矿不宜采用酸浸。苛性碱浸出可获得较高的锌浸出率,但选择性差,在浸出中,硅、铝和铅等均大量溶解,后续的溶液净化、碱再生及锌回收等过程难度较大[11−15]。氨法浸出选择性强、原料适应性广、工艺简单,适宜于处理高硅、高碱性脉石的氧化锌矿[16−18],但研究表明,当矿石中硅酸盐类锌矿物含量较高时,锌浸出率偏低[14,19−22]。
目前,对硅酸盐类锌矿物在氨浸中的行为,尚缺乏系统严谨的研究。已有研究均以含多种锌矿物的氧化锌矿为对象,根据浸出实验结果推断,基于热力学[23]或动力学[24]原因,硅酸盐类锌矿物在氨浸体系中难以浸出。但这些结论均未得到可靠的实验事实支持。对纯硅酸盐类锌矿物的氨浸机理及其速率控制规律,目前尚未见研究报道。为此,本文作者系统研究了纯硅锌矿在(NH4)2SO4-NH3-H2O体系下的浸出,以期揭示浸出反应机理,进而阐明其难以浸出的内在原因。
1 实验
1.1 实验原料
硅锌矿样品系以云南兰坪天然异极矿为原料,在1 100 ℃下煅烧3 h制备得到,煅烧反应方程为

异极矿及其煅烧产物硅锌矿样品的XRD谱如图1所示。表1所列为硅锌矿样品的主要化学组成。硅锌矿样品经破碎、筛分后备用,如无特别说明,浸出实验样品粒度为96~109 μm,其SEM像如图2所示。

图1 矿样的XRD谱Fig.1 XRD patterns of ore samples
实验所用氨水、硫酸铵、硅酸钠等试剂均为分析纯,水为去离子水。
图1及表1结果表明,异极矿样品煅烧后,已完全脱水转化为硅锌矿(JCPDF No.83−2270),样品杂质含量较低,基本为硅锌矿纯矿物,其 XRD谱及化学成分与文献[11, 16]中的一致。由图2可看出,硅锌矿样品形貌为类球形,颗粒大小均匀,疏松多孔,是由微细粒子组成的多孔团聚体。

表1 硅锌矿样品的主要化学成分Table 1 Chemical compositions of willemite sample (mass fraction, %)

图2 粒度为96~109 μm的硅锌矿样品SEM像Fig.2 SEM images of willemite sample with particle size of 96~109 μm
1.2 实验方法
浸出实验在2 L三口瓶中进行,瓶上3个开口分别用于装设温度计、机械搅拌器(2片半径为25 mm桨叶)和取样。三口瓶置于恒温水浴中,水浴温度控制在设定值(波动范围±1 ℃)。按预定的总氨浓度及 NH4+和NH3摩尔比配制1 L浸出液,置于三口瓶中,预热到实验温度,开启搅拌,加入硅锌矿样品开始浸出。浸出结束后,取10 mL矿浆离心分离,分别取浸出液及渣样分析检测。
实验测定了SiO2在(NH4)2SO4-NH3-H2O体系中的饱和溶解度,其方法为按预定组成配制溶液,将其预热至实验温度恒温,开启搅拌,加入过量硅酸钠,每隔10 h取上清液检测其中SiO2浓度,当其值不随时间变化后,即为溶液中SiO2饱和浓度。每组实验重复4次取平均值。
1.3 分析测试
用硅钼蓝分光光度法测定浸出液中 SiO2浓度;EDTA络合滴定法测定浸出液中锌浓度,并据此计算锌的浸出率;采用Rigaku-TTRIII型X 射线衍射仪(Cu靶,Kα,λ=0.154 06 nm)对样品进行物相分析;采用JSM−6360LV 型扫描电镜(SEM)观察样品的形貌;采用EDS−GENESIS 60S型X射线能谱仪测定固体产物表面主要元素成分。
2 结果及讨论
2.1 总氨浓度对锌浸出率的影响
在矿样粒径96~109 μm、n(NH4+)/n(NH3)为1、温度323 K、液固质量比200:1、搅拌速率350 r/min的条件下,考察了总氨浓度对锌浸出率的影响,其结果如图3所示。

图3 总氨浓度对锌浸出率的影响Fig.3 Effect of total ammonia concentration on zinc leaching efficiency
由图3可见,总氨浓度对锌浸出率的影响非常显著。在总氨浓度7 mol/L条件下,经180 min浸出,锌的浸出率达到53.31%,随着时间延长,锌的浸出率几乎没有变化;而当总氨浓度降低到4 mol/L时,浸出300 min,锌的浸出率仅为22.79%。由图3还可看出,达到一定锌浸出率后,浸出趋于停滞。产生这一现象的原因,既可能归因于浸出产物硅胶对矿石表面的包裹,也可能是由于浸出液中SiO2浓度达到饱和而抑制了浸出。
对在总氨浓度为7 mol/L、浸出时间300 min的条件下得到的浸出渣进行了SEM-EDS分析,其结果如图4所示。同时,在n(NH4+)/n(NH3)=1、温度323 K条件下,测定了 (NH4)2SO4-NH3-H2O体系中 SiO2的饱和溶解度随总氨浓度的变化,并与浸出终点时浸出液中SiO2浓度进行比较,其结果如图5所示。

图4 浸出渣的SEM像和EDS谱Fig.4 SEM image (a)and EDS spectrum (b)of leaching residue
由图4可见,在浸出过程中,并未产生SiO2胶体对矿石颗粒表面的包裹,因而可以排除上述导致浸出趋于停滞的第一种原因。
由图5可看出,不同总氨浓度下SiO2溶解度趋于一致,无明显变化;浸出终点时,浸出液中SiO2浓度达到或接近饱和。需要指出的是,当总氨浓度从 5 mol/L上升到7 mol/L时,与锌浸出率增幅较大(见图3)不同的是,SiO2浓度(SiO2浸出率)并无明显变化。可见,当溶液中SiO2浓度达到饱和时,将从溶液中析出,若SiO2从溶液中析出速率缓慢,则会使浸出过程减慢,甚至趋于停滞。

图5 总氨浓度对浸出液中 SiO2浓度及其饱和溶解度的影响Fig.5 Effects of total ammonia concentration on silica concentration and its saturated solubility in leaching solution
2.2 温度对锌浸出率的影响
在矿样粒径 96~109 μm、总氨浓度 5 mol/L、n(NH4+)/n(NH3)为1、液固质量比200:1、搅拌速率350 r/min的条件下,考察了温度对锌浸出率的影响,其结果如图6所示。由图6可见,反应温度对硅锌矿浸出过程有显著影响。在上述实验条件下浸出 300 min,当浸出温度从 303 K上升到333 K时,锌浸出率从12.4%提高到46.3%。还可看出,在不同温度下达到一定锌浸出率后,浸出趋于停滞。

图6 温度对锌浸出率的影响Fig.6 Effect of temperature on zinc leaching efficiency
为揭示温度影响的机理,在总氨浓度 5 mol/L、n(NH4+)/n(NH3)为1的条件下,测定了(NH4)2SO4-NH3-H2O体系中SiO2饱和溶解度随温度的变化,并与浸出终点时浸出液中SiO2浓度比较,其结果如图7所示。
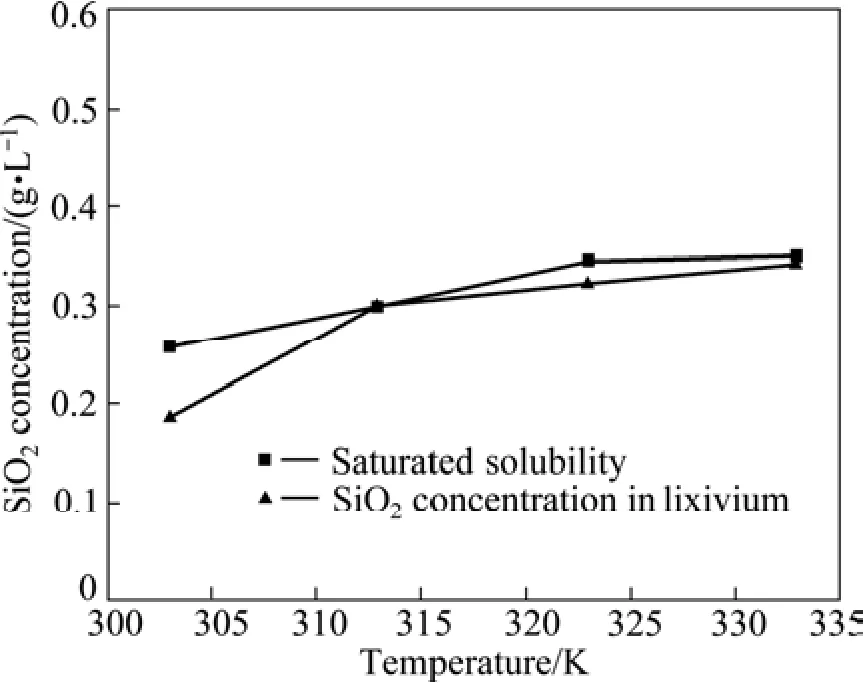
图7 温度对浸出液中SiO2浓度及其溶解度的影响Fig.7 Effects of temperature on SiO2 concentration and its saturated solubility in leaching solution
由图7可见,不同温度下浸出后的溶液中,SiO2浓度已达到或趋于饱和。同时,随温度升高,SiO2在浸出体系中的饱和溶解度虽有增加,但并不显著,从303 K升温至333 K, SiO2在浸出体系中的饱和溶解度提高约75%,其结果如图6所示,相应地,锌浸出率提高 270%。由此可以推断,高温下锌浸出率较高的原因,并不完全归因于SiO2溶解度的提高,而可能的主要原因在于高温下SiO2从溶液中析出速度较快。
2.3 液固质量比对锌浸出率的影响
在矿样粒径 96~109 μm、总氨浓度 7 mol/L、n(NH4+)/n(NH3)为1、温度323 K、搅拌速率350 r/min、浸出时间300 min的条件下,考察了液固质量比对锌浸出率及浸出液中SiO2浓度的影响,其结果如图8所示。

图8 液固质量比对锌浸出率及浸出液中SiO2浓度的影响Fig.8 Effects of mass ratio of liquid to solid on zinc leaching efficiency and SiO2 concentration in leaching solution
由图8可见,锌浸出率随液固质量比增加而显著提高。在液固质量比为 5的条件下,锌浸出率仅为2.72%;而当其增加到 500时,锌浸出率上升到84.15%。 图 8所示还表明,不同液固质量比下浸出300 min后,浸出液中SiO2的浓度趋于一致,波动在0.20~0.35 g/L之间,达到或接近浸出体系在该条件下SiO2饱和浓度(0.338 g/L)。这一结果提示,硅锌矿在(NH4)2SO4-NH3-H2O体系下的浸出过程,主要受制于浸出液中 SiO2的饱和程度,低液固质量比下,SiO2的溶解使其在浸出液中迅速趋于饱和,制约了硅锌矿的进一步浸出,使得锌的浸出率很低;而在高液固质量比下,由于浸出样品中硅的总量较少,只有达到较高的浸出率,浸出液中SiO2才趋于饱和,因此,能达到较高的锌浸出率。
对不同液固质量比下锌和 SiO2的浸出率进行比较,其结果如图9所示。由于浸出样品为纯硅锌矿,因此,若溶解产物均稳定存在于溶液中,浸出中锌与硅的浸出率应基本一致。但图9结果表明,在不同液固比下,硅的浸出率均比锌的低,这进一步表明,随浸出进行,SiO2在浸出液中过饱和后,可能以无定形SiO2从溶液中析出,但无定形SiO2析出过程较缓慢,制约了浸出过程的进行。

图9 液固质量比对锌和硅浸出率的影响Fig.9 Effects of mass ratio of liquid to solid on zinc and silica leaching efficiency
2.4 浸出液初始SiO2浓度对锌浸出率的影响
研究表明,硅锌矿在(NH4)2SO4-NH3-H2O体系中难以浸出,归因于SiO2在浸出液中较低的溶解度和过慢的析出速度。为验证此点,在矿样粒径96~109 μm、总氨浓度7 mol/L、n(NH4+)/n(NH3)为1、液固质量比200:1、温度323 K、搅拌速率350 r/min的条件下,考察了浸出液中初始SiO2浓度对锌浸出率的影响,其结果如图10所示。
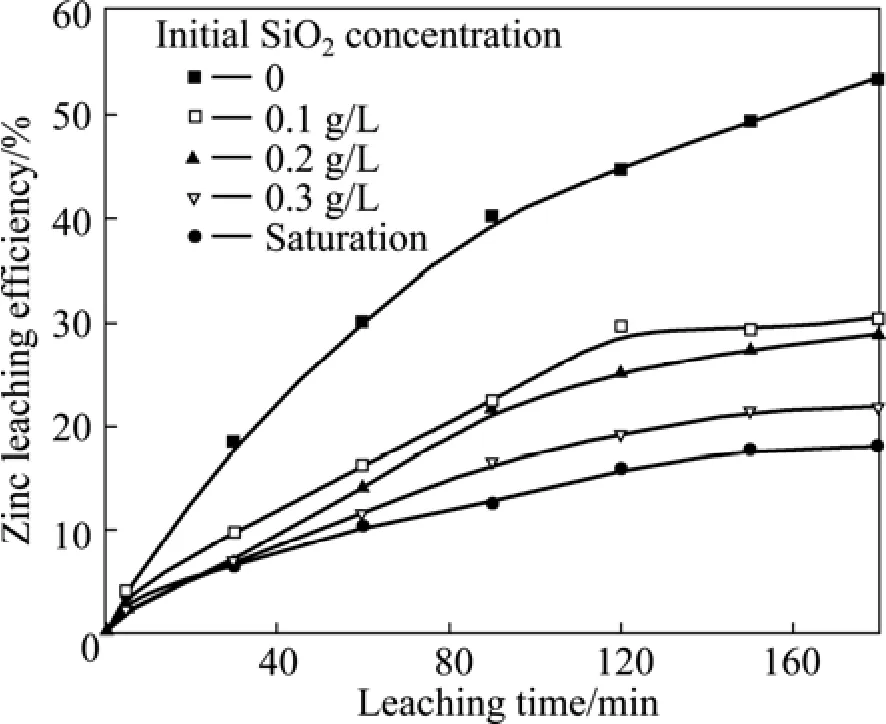
图10 浸出液中SiO2初始浓度对锌浸出率的影响Fig.10 Effect of initial SiO2 concentration in lixivium on zinc leaching efficiency
图10表明,随浸出液中初始SiO2浓度的增加,锌浸出率显著降低,进一步证实了硅锌矿在(NH4)2SO4-NH3-H2O体系中的浸出主要受SiO2溶解度制约的结论。值得一提的是,当浸出液中初始 SiO2浓度达到饱和时,浸出180 min后,锌的浸出率也能达到18.10%,由此可以推断,浸出过程中,溶解于溶液中的SiO2会发生过饱和析出,但其速度缓慢。
2.5 硅锌矿在(NH4)2SO4-NH3-H2O 体系中的浸出反应
根据以上研究结果,推断出硅锌矿在(NH4)2SO4-NH3-H2O体系中的浸出反应为
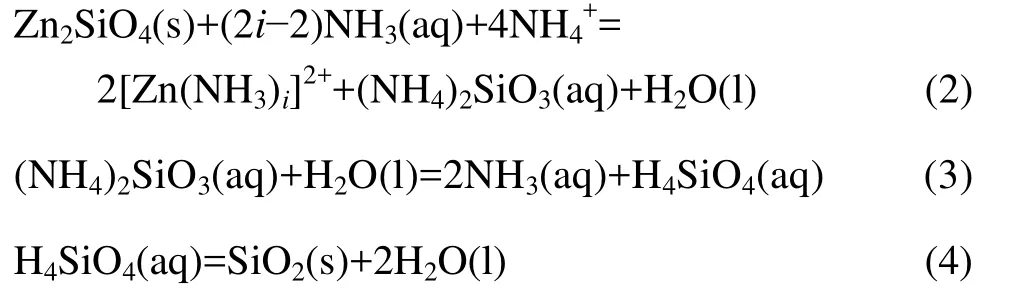
总反应为

式中:i=1~4。浸出中,Zn(II)与NH3形成配合物进入溶液,硅首先形成(NH4)2SiO3进入溶液,(NH4)2SiO3不稳定,发生双水解,生成NH3与H4SiO4(aq),当溶液中SiO2浓度达到饱和后会转化为无定形SiO2沉淀。
3 结论
1) 硅锌矿在(NH4)2SO4-NH3-H2O体系中可以浸出。 温度、总氨浓度、液固质量比以及浸出液初始SiO2浓度对锌浸出率均有不同程度的影响,其中,液固质量比和初始SiO2浓度的影响尤为显著。
2) SiO2在(NH4)2SO4-NH3-H2O体系中饱和溶解度较小,随温度及体系组成不同,波动在0.3 g/L左右。浸出中,硅锌矿中的硅溶解进入浸出液,并逐步趋于饱和,使得浸出速率减慢,甚至趋于停滞,是硅锌矿在(NH4)2SO4-NH3-H2O体系中难以浸出的主要原因。
3) 浸出中,当浸出液中 SiO2过饱和后,可从溶液中析出,但这一过程过于缓慢,制约了浸出过程的进行。
[1]郭兴忠, 张丙怀, 阳海彬, 杨 辉. 熔融还原处理低品位氧化锌矿的研究[J]. 矿冶工程, 2003, 23(1): 57−60.GUO Xing-zhong, ZHANG Bing-huai, YANG Hai-bin, YANG Hui. Melting-reduction of low-grade zinc oxide ores[J]. Mining and Metallurgical Engineering, 2003, 23(1): 57−60.
[2]MATTHEW I G, ELSNER D. The processing of zinc silicate ores—A review[J]. Metallurgical and Materials Transactions B,1977, 8(1): 85−91.
[3]蒋继穆. 我国铅锌冶炼现状与持续发展[J]. 中国有色金属学报, 2004, 14(S1): 52−62.JIANG Ji-mu. Status and sustainable development of lead and zinc smelting industry in China [J]. The Chinese Journal of Nonferrous Metals, 2004, 14(S1): 52−62.
[4]杨天足, 任 晋, 刘伟锋, 窦爱春, 刘 伟, 张杜超. Zn(Ⅱ)-Glu2−-CO32−-H2O体系热力学平衡分析[J]. 中国有色金属学报,2009, 19(6): 1155−1161.YANG Tian-zu, REN Jin, LIU Wei-feng, DOU Ai-chun, LIU Wei, ZHANG Du-chao. Thermodynamics equilibrium analysis of Zn(Ⅱ)-Glu2−-CO32−-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2001, 19(6): 1155−1161.
[5]MATTHEW I G, ELSNER D. The hydrometallurgical treatment of zinc silicate ores[J]. Metallurgical and Materials Transactions B, 1977, 8(1): 73−83.
[6]KUMAR R, BISWAS A K. Zinc recovery from zawar ancient siliceous slag[J]. Hydrometallurgy, 1986, 15(3): 267−280.
[7]BODAS M G. Hydrometallurgical treatment of zinc silicate ore from Thailand[J]. Hydrometallurgy, 1996, 40(1/2): 37−49.
[8]ESPIARI S, RASHCHI F, SADRNEZHAAD S K.Hydrometallurgical treatment of tailings with high zinc content[J]. Hydrometallurgy, 2006, 82(1/2): 54−62.
[9]HUA Y, LIN Z, YAH Z. Application of microwave irradiation to quick leach of zinc silicate ore[J]. Minerals Engineering, 2002,15(6): 451−456.
[10]李存兄, 魏 昶, 樊 刚, 杨秀丽, 徐宏胜, 邓志敢, 李旻廷,李兴彬. 高硅氧化锌矿加压酸浸处理[J]. 中国有色金属学报,2009, 19(9): 1678−1683.LI Cun-xiong, WEI Chang, FAN Gang, YANG Xiu-li, XU Hong-sheng, DENG Zhi-gan, LI Min-ting, LI Xing-bin. Pressure acid leaching of high silicon zinc oxide ore[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(9): 1678−1683.
[11]SANTOS F M F, PINA P S, PORCARO R, VICTOR A O,CAELOS A S, VERSIANE A L. The kinetics of zinc silicate leaching in sodium hydroxide [J]. Hydrometallurgy, 2010,102(1/4): 43−49.
[12]CHEN Ai-liang, ZHAO Zhong-wei, JIA Xi-jun, LONG Shuang,HUO Guang-shen, CHEN Xing-yu. Alkaline leaching Zn and its concomitant metals from refractory hemimorphite zinc oxide ore[J]. Hydrometallurgy, 2009, 97(3/4): 228−232.
[13]CHEN Ai-liang, ZHAO Zhong-wei, JIA Xi-jun, LONG Shuang,HUO Guang-shen, CHEN Xing-yu. Mechanochemical leaching of refractory zinc silicate (hemimorphite)in alkaline solution[J].Hydrometallurgy, 2009, 99(3/4): 255−258.
[14]杨大锦, 朱华山, 陈加希. 湿法提锌工艺与技术[M]. 北京:冶金工业出版社, 2007: 56−73.YANG Da-jing, ZHU Hua-shan, CHEN Jia-xi. Zinc hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 2007:56−73.
[15]刘凤林, 金作美, 王励生. 高硅硫化锌精矿氧化焙烧中硅酸锌生成反应的动力学[J]. 中国有色金属学报, 2001, 11(3):514−517.LIU Feng-lin, JIN Zuo-mei, WANG Li-sheng. Kinetics of formation reaction of Zn2SiO4during roasting high silica-containing sphalerite concentrate[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(3): 514−517.
[16]SOUZA A D, PINA P S, LIMA E V O, SILVA C A, LEAO V A.Kinetic of sulphuric acid leaching of a zinc silicate calcine[J].Hydrometallurgy, 2007, 89(3/4): 337−345.
[17]HARVEY T G. The hydrometallurgical extraction of zinc by ammonium carbonate: A review of the Schnabel process [J].Mineral Processing and Extractive Metallurgy Review, 2006,27(4): 231−279.
[18]FILIPPOU D. Innovative hydrometallurgical processes for the primary processing of zinc[J]. Mineral Processing and Extractive Metallurgy Review, 2004, 25(3): 205−252.
[19]MENG X, HAN K N. The principles and applications of ammonia leaching of metals—A review[J]. Mineral Processing and Extractive Metallurgy Review, 1996, 16(1): 23−61.
[20]唐谟堂, 欧阳民. 硫铵法制取等级氧化锌[J]. 中国有色金属学报, 1998, 8(1): 118−121.TANG Mo-tang, OU Yang-min. Preparation of grade zinc oxide by using ammonium sulfate and ammonia complex leaching process[J]. The Chinese Journal of Nonferrous Metals, 1998,8(1): 118−121.
[21]张保平, 唐谟堂, 杨声海. 氨法处理氧化锌矿制取电锌[J]. 中南大学学报: 自然科学版, 2003, 34(6): 619−623.ZHANG Bao-ping, TANG Mo-tang, YANG Sheng-hai. Treating zinc oxide ores using ammonia-ammonium chloride to produce electrolysis zinc[J]. Journal of Central South University: Natural Science, 2003, 34(6): 619−623.
[22]杨声海, 唐谟堂, 邓昌雄, 张顺应. 由氧化锌烟灰氨法制取高纯锌[J]. 中国有色金属学报, 2001, 11(6): 1110−1113.YANG Sheng-hai, TANG Mo-tang, DENG Chang-xiong,ZHANG Shun-ying. Making high-purity zinc from zinc oxide fume dusts[J]. The Chinese Journal of Nonferrous Metals, 2001,11(6): 1110−1113.
[23]朱 云, 胡 汉, 苏云生, 杨保民. 难选氧化锌矿氨浸动力学[J].过程工程学报, 2002, 2(1): 81−85.ZHU Yun, HU Han, SU Yun-sheng, YANG Bao-min. Kinetics of leaching poorly floated zinc oxide ore with ammonia[J]. The Chinese Journal of Process Engineering, 2002, 2(1): 81−85.
[24]曹琴园, 李 洁, 陈启元. 机械活化对异极矿碱法浸出及物理性能的影响[J]. 中国有色金属学报, 2010, 20(2): 354−362.CAO Qin-yuan, LI Jie, CHEN Qi-yuan. Effects of mechanical activation on alkaline leaching and physicochemical properties of hemimorphite[J]. The Chinese Journal of Nonferrous Metals,2010, 20(2): 354−362.

