超声引导下经皮肾造瘘术对重度肾积水患肾功能的评价
曲仕浩
(广东珠海市第二人民医院泌尿外科,珠海市 519020)
肾积水是由泌尿系统本身及其周围的器官病变引起尿路梗阻,尿液从肾盂排出受阻,蓄积后肾内压力增高,肾盂肾盏扩张,肾实质功能减退,继而引起肾功能异常,严重的可导致患肾功能衰竭[1]。肾积水是临床常见病症,准确评价肾功能及预测梗阻解除后肾功能的可复性,是临床上亟待解决的问题。随着介入性超声技术的不断发展,超声引导下经皮肾造瘘术(percutaneous nephrostomy,PCN)已经成为治疗肾积水简便而有效的方法之一。本院对重度肾积水患者行PCN治疗,并对患肾功能进行评价,现报告如下。
1 资料与方法
1.1 一般资料 本组患者为2007年9月至2011年1月在我院确诊为重度肾积水并且接受PCN治疗48例病人,其中男性31例,女性17例,年龄27~69岁,平均(46.4±6.7)岁。其中行单侧PCN治疗43例,双侧5例(占10.4%),患肾共53个。
1.2 仪器 应用MINDRAY-M5型彩超诊断仪,探头频率3.5 MHz。经皮肾造瘘术应用帮拓猪尾巴引流导管组(直接穿刺型),型号513-310-002-000。
1.3 手术方法 根据拟穿刺肾盏的方向及位置,患者取肾区腹侧垫高的完全俯卧位或仅患侧垫高30°的腹斜位。应用彩超仪对患侧肾脏进行仔细扫查,选择合适穿刺路径,确定穿刺角度和深度。常规消毒铺巾,2%利多卡因局部浸润麻醉,穿刺部位通常选择在腋后线与十二肋下缘交点下方2 cm处。穿刺时嘱患者中度吸气后屏住呼吸,18G穿刺针经引导架进针约5~10 cm,到达肾盂中下盏无回声区后退出针芯,见到淡黄色尿液流出后沿穿刺针送入金属导丝。导丝进入肾盂后退出穿刺针,用筋膜扩张器沿导丝依次扩张穿刺通道至12F,扩张后沿导丝送入PTCD引流管,拔出导丝,皮肤缝线固定PTCD管以防脱落,在超声观察下调整引流管的位置确保引流通畅[2]。
1.4 术后随诊 术后1~7 d记录每日24 h引流尿量,并检测尿液pH值;术后第7天彩超测量肾动脉血流阻力指数及肾实质厚度,评价肾功能恢复情况。术后1个月拔管,了解患者是否有出血、感染、临近脏器损伤,肾造瘘管引流不畅、位置不当及脱落等情况。
1.5 分组标准 依据患肾24 h引流尿量及尿pH值[3]进行分组。肾功能恢复组:24 h引流尿量 >600 mL,尿pH<6.0;肾功能改善组:24 h引流尿量200~600 mL,尿pH值为6.1~7.1;肾无功能组:24 h引流尿量 <200 mL,尿pH >7.1。
1.6 统计学分析 数据应用SPSS 13.0软件进行统计学分析,计量资料以均数±标准差(s)表示,组间比较用方差分析,组内PCN治疗前后肾动脉血流阻力指数及肾实质厚度比较用配对t检验。检验水准α=0.05,P<0.05认为差异有统计学意义。
2 结果
2.1 经皮肾造瘘术后分组情况 经皮肾造瘘术后,次日开始连续7 d记录每日24 h引流尿量,并检测尿液pH值,计算平均值。依据分组标准,将53个积水肾按照24 h引流尿量及尿pH值分入恢复组(n=24)、改善组(n=18)及无功能组(n=11)。
2.2 各组经皮肾造瘘术前后肾动脉血流阻力指数、肾实质厚度比较 术前彩超检测患肾肾动脉血流阻力指数RI,无功能组显著高于恢复组和改善组,差异有统计学意义(P<0.01);改善组略高于恢复组,差异无统计学意义(P>0.05)。术后彩超检测患肾肾动脉血流RI,无功能组显著高于改善组及恢复组,改善组高于恢复组,差异均有统计学意义(P<0.01)。术前和术后彩超检测患肾肾实质厚度,无功能组显著低于改善组及恢复组,改善组低于恢复组,差异均有统计学意义(P<0.01)。见表1。
恢复组、改善组及无功能组术后肾动脉血流RI与术前比较均有降低,差异均有统计学意义(P<0.01),恢复组和改善组降低程度显著。三组术后肾实质厚度与术前相比,均有不同程度的增厚,恢复组和改善组增加显著,差异均有统计学意义(P<0.01)。见表1。
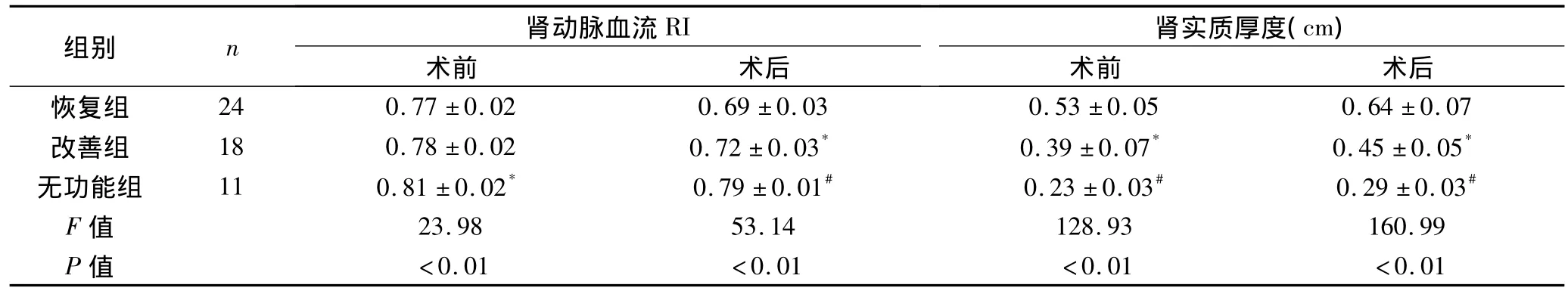
表1 各组经皮肾造瘘术前后肾动脉血流RI、肾实质厚度比较
2.3 术后治疗及随诊 无功能组11个患肾经全肾切除术后病理证实,肉眼观积水肾肾盂肾盏均扩张,肾实质明显萎缩变薄,肾锥体萎缩;镜下观肾小管失去原来与肾表面的垂直排列而改为平行排列,萎缩后间质呈现结缔组织增生及淋巴细胞浸润,肾小球也出现萎缩并发生纤维化及玻璃样变,肾皮质内肾小球、肾小管结构消失或少见。恢复组及改善组在保留肾脏并解除梗阻原发病灶后,术后1个月复查肾功能及超声,与术前相比均有不同程度好转。所有患者置管均一次性成功,成功率100%,术后无出血、感染及临近脏器损伤等并发症;5例出现肾造瘘管引流不畅,调整引流管位置后改善;4例引流管脱落,重新置管后成功。
3 讨论
随着介入超声技术的发展,超声介导下经皮肾造瘘术在临床的应用越来越广泛[4]。超声能够清晰显示肾盏的位置和肾实质的厚度,直接引导穿刺的角度和深度,可确保穿刺定位的准确性,避免了大血管、周围脏器损伤及肾脏贯通伤等严重并发症的发生[5]。本研究中53个患肾经皮肾造瘘术管均一次性成功,成功率为100%,5例出现肾造瘘管引流不畅,调整引流管位置后改善;4例引流管脱落,重新置管后成功,术后无出血、感染及临近脏器损伤等并发症发生。
经皮肾造瘘术是治疗肾积水简便而有效的方法,尤其在因梗阻而造成的肾功能受损时是首选的治疗方法,能够快速解除肾脏因梗阻导致压力增高引起的肾功能损伤。重度肾积水功能受损程度不同,经治疗后功能恢复程度亦不同。本研究依据经皮肾造瘘术后患肾24 h引流尿量及尿pH值进行分组,评价患肾功能及治疗效果。结果显示,恢复组、改善组及无功能组,各组间术前及术后肾动脉血流的阻力指数、肾实质厚度比较均有统计学差异(P<0.01),各组内术后与术前比较均有不同程度的改善(P<0.01)。经皮肾造瘘术后患肾24 h引流尿量>600 mL,尿pH<6.0,超声术前测量肾实质厚度>0.5 cm,肾动脉血流RI<0.8,肾功能恢复好;24 h引流尿量<200 mL,尿pH>7.1,肾实质厚度 <0.3 cm,肾动脉血流 RI>0.8,患肾功能不可恢复,患肾经全肾切除术后病理证实肾无功能。
超声引导下经皮肾造瘘术能够及时引流尿液,有效改善肾功能;依据术后引流尿量、尿pH、肾动脉血流阻力指数及肾实质厚度,能够准确评价患肾功能。引流期间可以通过检测患肾尿量、尿pH值、尿比重及尿生化等,指导下一步治疗[6]。手术成功率高、创伤小、安全、可靠,具有较高临床应用价值。
[1]吴在德,吴肇汉.外科学[M].第7版.北京:人民卫生出版社,2008:670-673.
[2]马腾骧.实用泌尿外科手术技巧[M].天津:科学技术出版社,2002:896-914.
[3]Ibrahim A,Fahal AH.Recovery of radiologically functionless obstructed kidneys[J].Br J Urol,1984,56(2):113 -115.
[4]Gupta S,Gulati M,Uday Shankar K,et al.Percutaneous nephrostomy with real-time sonographic guidance[J].Acta Radiol,1997,38(3):454-457.
[5]Martino P.Ultrasound-guided percutaneous nephrostomy[J].Arch Ital Urol Androl,2000,72(4):324 -327.
[6]张清桂.经皮肾穿刺造瘘术在肾后性肾衰竭中的应用[J].微创医学,2008,3(3):277 -278.

