磁性多壁碳纳米管吸附水中硝基苯酚异构体的研究
熊振湖,胡 品,王 璐
(天津城市建设学院 a. 天津市水质科学与技术重点实验室;b. 环境与市政工程系,天津 300384)
磁性多壁碳纳米管吸附水中硝基苯酚异构体的研究
熊振湖a,b,胡 品a,b,王 璐a,b
(天津城市建设学院 a. 天津市水质科学与技术重点实验室;b. 环境与市政工程系,天津 300384)
研究了利用磁化多壁碳纳米管(MWCNTs)吸附水中硝基苯酚三种异构体(邻硝基苯酚、间硝基苯酚和对硝基苯酚)的过程,考察了 MWCNTs投加量、溶液 pH值等因素对吸附过程的影响.结果表明:硝基苯酚三种异构体的吸附量随磁性MWCNTs投加量的增加而增大,并且吸附剂量增加到一定阶段后,硝基苯酚三种异构体的吸附量达到平衡.磁性MWCNTs的量为0.8,g/L,且三种异构体的初始浓度为30,mg/L时,它们在水溶液中的去除率为80%~90%左右,而且随溶液pH的增加,各异构体的去除率都呈现先增大后下降的趋势.因此,磁性MWCNTs适合对三种硝基苯酚异构体的吸附.
磁性MWCNTs;硝基苯酚;异构体;表征;吸附
苯酚的硝基衍生物(邻硝基苯酚、间硝基苯酚、对硝基苯酚)是一类有毒且在水环境中很难降解的持久性有机污染物,对人的健康和水生物的生长与繁殖都会构成严重威胁.由于硝基的钝化作用,生物与化学的方法难以降解废水中的硝基苯酚,而吸附法作为水中有机污染物的处理方法之一,得到了人们的普遍关注[1].广泛用于去除水中酚类污染物的吸附剂是活性炭[2-3],但活性炭的主要缺点是高价格和再生的费用[4].
多壁碳纳米管(multi-wall carbon nanotubes,简称MWCNTs)作为一种新型的炭材料,自被发现以来就引起了人们的热切关注.它不仅具有活性炭优良的吸附性能,而且比表面积远高于活性炭.许多研究者将MWCNTs用于吸附水中的重金属离子[5]与有机污染物[2].然而,MWCNTs一般是以纳米级颗粒悬浮在水中,将它们从水介质中收集起来比较困难.为此,近年来人们将磁性分离技术与MWCNTs的优良吸附性能相结合,去除水中的药物[3]、偶氮染料[6]等污染物,在吸附之后用普通的磁铁就可以方便地将磁性MWCNTs从水介质中分离出来.虽然已有人使用MWCNTs吸附水中苯酚的衍生物[7],但目前还没有采用磁性 MWCNTs吸附水中硝基苯酚异构体的报道.鉴于此,本研究中采用湿式化学方法,将原位生成的Fe3O4纳米颗粒填入MWCNTs的管径中,并部分地包覆在MWCNTs表面.在利用TEM等方法表征磁性 MWCNTs基础上,系统地考察了吸附剂的投加量、pH等因素对吸附过程的影响.
1 实验部分
1.1 试剂与仪器
MWCNTs购自中国科学院成都有机化学有限公司,其内径为 3~5,nm,外径为 8~15,nm,长度约为50,µm,外表面积约为 200,m2/g.分析纯的(NH4)2Fe(SO4)2·6H2O 与 NH4Fe(SO4)2·12H2O、三种硝基苯酚异构体购自天津江天化学品公司.硝基苯酚的本体溶液用二次蒸馏水制备,其浓度为100,mg/L,使用前将其稀释到所需浓度.其它试剂为分析纯.
HZQ-QG振荡器(中国哈尔滨东联电子技术开发有限公司)、紫外-可见分光光度计(北京普析通用仪器有限责任公司).MWCNTs的透射电子显微(TEM)图像通过200 kV加速电压的JEM-2011电子显微镜(JEOL,Japan)获取.采用D/max,2550,X-射线衍射仪(RigaKu,Japan)获取磁性 MWCNTs的 X-射线衍射图谱.
1.2 磁性MWCNTs的合成
根据文献[8]方法对MWCNTs进行活化:在250,mL四口瓶中加入1.5,g原始MWCNTs和150,mL硝酸,在水浴中 60,℃恒温、恒速搅拌 12,h,反应结束后,自然冷却至室温;反应过的碳纳米管沉到瓶底,然后进行抽滤,再用蒸馏水反复洗涤至中性,将洗好的碳纳米管在 100,℃的烘箱中干燥 4,h,最后将处理好的碳纳米管放入干燥器中备用.
磁性 MWCNTs的合成要点是在碱性条件下,使Fe2+、Fe3+反应生成磁性氧化铁颗粒沉淀在 MWCNTs表面和内部.典型制备过程为[9]:在一个250,mL四口烧瓶中加入100,mL蒸馏水以及1.25,g,NH4Fe(SO4)2·12H2O 和 0.85,g(NH4)2Fe(SO4)2·6H2O,超声处理10,min使反应物完全溶解,再加入 0.5,g羧化MWCNTs,超声振荡的同时逐滴加入事先配制好的8,mol/L氨水溶液,保持混合液的pH值在11~12,使铁的氧化物逐渐沉淀下来;此后,将反应体系放置在50,℃恒温水浴中搅拌0.5,h;反应结束,用磁铁从溶液中分离生成的磁性 MWCNTs,蒸馏水与无水乙醇分别洗涤 3次,过滤出产物,置入真空干燥箱中去除水分,然后放入干燥器内备用于吸附实验.
1.3 间歇吸附实验
以间歇方式进行吸附实验.将一定量的磁性MWCNTs分别加入到200,mL已知初始浓度的邻硝基苯酚、间硝基苯酚和对硝基苯酚的溶液中,用0.1,M,H2SO4或NaOH调节悬浮液的 pH值后,将混合物置于一台可调节温度与速度的振荡器中,以150,r/min振摇,规定时间取样,磁铁分离磁性MWCNTs后,用紫外-可见光分光光度计测定上清液中溶液的吸光度,并计算单位吸附剂对吸附质的吸附量,公式为

式中:q为吸附量,mg/g;V为溶液体积,mL;C0和 Ce分别为吸附前和吸附平衡时溶液中吸附质的质量浓度,mg/L;m为 MWCNTs的用量,g.
1.4 分析方法
将三种硝基苯酚各自配制成浓度为 1,3,5,,10,,15,20,mg/L的六种溶液,采用UV-2550紫外-可见分光光度计在最大吸收波长(邻硝基苯酚 279,nm,间硝基苯酚274,nm,对硝基苯酚317,nm)下测定不同浓度所对应的吸光度,根据吸光度与浓度的关系做出相应溶液的标准工作曲线,以及所对应的相关系数R2.
在吸附反应的不同时间内取样,将所取上清液经过0.45,µm膜过滤,注射到比色皿中,用紫外-可见分光光度计测定吸附前溶液的吸光度以及所取上清液的吸光度,根据二者吸光度之差和标准曲线,得出吸附前后的溶液浓度与各硝基苯酚异构体的去除率.
2 结果与讨论
2.1 磁性MWCNTs的表征
图1a是未经处理的原始MWCNTs的TEM图像,可以发现原始 MWCNTs相互纠缠在一起,并且是末端开口的;图 1b显示的是磁性化的 MWCNTs,可清楚地发现Fe3O4纳米颗粒已经包覆在MWCNTs的表面,而且 MWCNTs的内部也填充有 Fe3O4纳米颗粒.由此可推断形成了MWCNTs/Fe3O4纳米复合物.产生这一现象的原因是浸渍中的毛细管力可以克服水的表面张力,使 Fe2+与 Fe3+进入到 MWCNTs的内部而生成 Fe3O4.另外,硝酸的氧化处理可以使MWCNTs被切断,从而形成开口端和表面功能基团,这也有助于铁离子进入MWCNTs的内部以及包覆在其表面.

图1 TEM图像
为证实磁性 MWCNTs对有机污染物的吸附能力,将少量磁性 MWCNTs加入到一定量的偶氮染料中性红溶液中,二者混合为黑色悬浮液(见图2a).将吸附混合物超声5,min后,溶液的颜色由红色迅速变浅至无色,在外置磁铁吸引下,吸附了中性红的磁性MWCNTs很快沉积到玻璃瓶的底部或侧壁(见图 2b和图 2c),这就证实了磁性 MWCNTs具有磁性和吸附能力.

图2 外置磁铁从溶液中分离磁性MWCNTs
2.2 磁性MWCNTs投加量对吸附的影响
图 3给出了硝基苯酚异构体的初始浓度为30,mg/L时,磁性 MWCNTs投加量的变化对吸附率的影响.在25,℃,pH为 6.0,吸附时间为 1,h条件下,分别称取 0.12,0.14,0.15,0.16,0.18,0.20,g 磁性 MWCNTs加入到 200,mL初始浓度为 30,mg/L溶液中,吸附一段时间,用磁铁分离固相与液相,测定溶液的吸光度,分析溶液中剩余药物的浓度,考察磁性 MWCNTs分别对邻硝基苯酚、间硝基苯酚、对硝基苯酚去除率的影响.
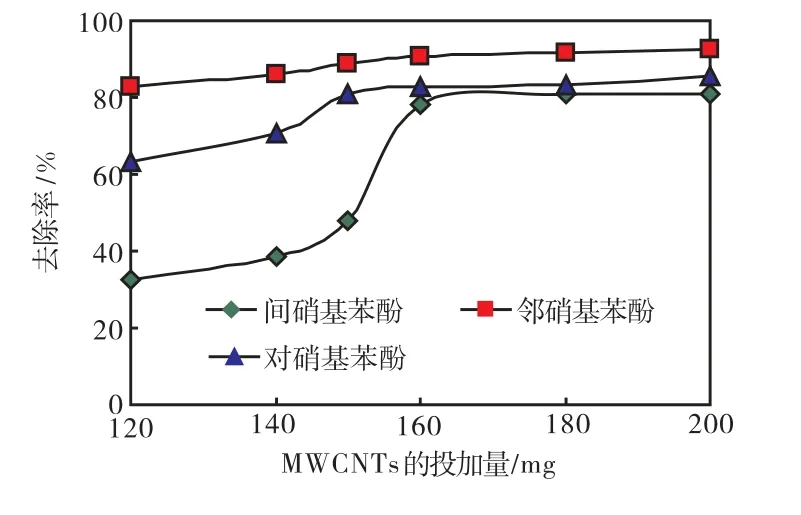
图3 磁性MWCNTs用量对邻硝基苯酚的吸附曲线
由图 3可见:在上述反应条件下,当 MWCNTs的投加量为 0.12,g时,间硝基苯酚的去除率较低,只有30%左右;随着MWCNTs投加量的增大,间硝基苯酚的去除率增加,在MWCNTs的投加量为0.16,g时,去除率接近 80%.当 MWCNTs投加量为 0.12,g(0.6,g/L)时,对硝基苯酚的去除率为 64%;随着MWCNTs投加量增加到 0.16,g,对应的去除率达到80%,并且接近吸附平衡.对于邻硝基苯酚,在MWCNTs的投加量为0.12,g时,其去除率达到82%;随着 MWCNTs投加量增加到0.16,g,邻硝基苯酚的去除率缓慢增加到 92%,达到平衡吸附.综合考虑三种硝基苯酚的去除过程,将适宜的 MWCNTs投加量选定为0.16,g(0.8,g/L).
MWCNTs投加量的增加导致硝基苯酚去除率增大的原因在于:在稀的悬浮液中,MWCNTs呈现分散状态,此时增加 MWCNTs的量不仅加大了参与吸附的 MWCNTs外表面积(有大量的吸附位点),而且增加了参与吸附的官能团数量.但MWCNTs的量增加到一定程度,去除率的增加趋于平缓并达到平衡,原因可能是增加MWCNTs的量加大了它们在水溶液中的碰撞几率,造成吸附剂颗粒的拥挤,导致吸附位点重叠,从而降低了吸附质在 MWCNTs外表面的聚集程度.此外,高MWCNTs的量会增加固-液悬浮物的黏稠性,也可能抑制吸附质分子扩散到 WMCNTs表面.
2.3 pH对磁性MWCNTs吸附能力的影响
在硝基苯酚三种异构体的初始浓度为 30,mg/L、磁性MWCNTs投加量为0.16,g、反应时间为5,h条件下,考察了磁性 MWCNTs吸附三种药物的结果,如图4所示.
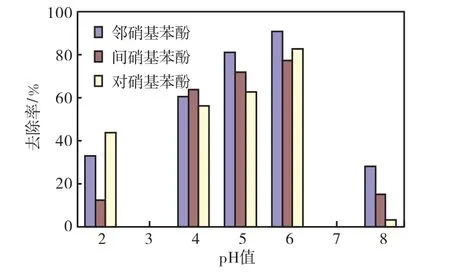
图4 磁性MWCNTs在不同pH下对硝基苯酚的去除率曲线
由图4可见:在酸性条件下,三种硝基苯酚的吸附量都很低,并且呈现随pH值的增加而增大的趋势;随着pH值的增加,去除率逐渐增大,在pH=6吸附达到平衡,邻、间、对硝基苯酚的去除率依次是 90.7%,77.3%和82.8%;但pH为碱性条件时,三种硝基苯酚的去除率都急剧下降.所以选择适宜的pH值为6.
硝基苯酚是一元弱酸,它在水溶液中的离子化可以用下式表示

其中:HA表示分子态的硝基苯酚;A–为硝基苯酚的离子态;H+是离解的氢离子.根据文献[10],设分子态的浓度 C0=[HA],总浓度 CT=[HA]+[A–],则分子态的硝基苯酚在不同pH中的摩尔分数可用式(3)计算,相应的硝基苯酚的阴离子在不同 pH中的摩尔分数(CA)可用式(4)计算

将某一硝基苯酚异构体的 pKa代入式(3)与式(4),就可得到不同pH下硝基苯酚各异构体的离子态和分子态的比例.由式(3)、(4)可以看出:pH<6时,硝基苯酚各异构体主要以分子态存在;随着 pH的逐渐增大,分子态的硝基苯酚逐渐减少;当 pH≥8时,则主要以离子态存在.
低pH溶液中有机弱酸去除率低下具有一定的共性[11].一方面,低 pH水溶液中存在着丰富的水合质子(H3O+),MWCNTs 表面富含电子的 π 键吸附缺电子的H3O+而发生质子化,形成表面正电荷;另一方面,由于有机弱酸在低pH下以分子状态存在,在H3O+作用下也会带有部分正电荷,而同种正电荷之间的斥力导致很低的吸附量.但随着 pH值的增加,溶液中同时存在着离子态与分子态的弱酸分子,而离子态有机弱酸具有很强的吸电子能力,容易与π-电子高度极化的MWCNTs表面形成电子授-受体,导致有机弱酸在MWCNTs 上的吸附量增加.但当 pH>6时,随 pH的增加,吸附量下降较快.原因是当溶液pH>6时,三种硝基苯酚的分子逐渐离子化成阴离子的形态,并且MWCNTs的表面带负电荷,此时MWCNTs的表面和硝基苯酚阴离子之间的静电排斥力起重要的作用,而且吸附在MWCNTs表面的硝基苯酚的阴离子之间也存在着静电排斥力.
从图4还可以发现,在pH=8时,MWCNTs对三种硝基苯酚的吸附量并没有降为零.其原因是硝基苯酚上的硝基具有较强的吸电子效应,使得 MWCNTs表面吸附的硝基苯酚阴离子上的负电荷得到一定程度的分散,减小了 MWCNTs上硝基苯酚阴离子与MWCNTs负电荷之间以及 MWCNTs上的硝基苯酚阴离子之间的静电斥力,导致 MWCNTs有能力吸附一定量的硝基苯酚阴离子.另外,在碱性条件下,提高pH 值势必增大溶液中的[Na+],而溶液中 Na+对于MWCNTs表面的负电荷与硝基苯酚的阴离子具有一定的屏蔽效应,造成带负电荷的 MWCNTs表面与硝基苯酚阴离子之间的静电斥力减小,从而保持一定的吸附量.
另一方面,在水溶液中,有机弱酸分子的电离状态(表现为分子态与离子态的比例)不但决定于溶液的pH,而且还与该分子的pKa相关.所以在pH不变的条件下,不同的硝基苯酚异构体(邻、间、对三种硝基苯酚的 pKa依次为 7.21,8.00,7.16)的分子态与离子态的比例有所不同,进而使得该 pH值下被吸附量也不尽相同.
2.4 三种硝基苯酚异构体的吸附动力学及吸附过程的评价
为了探讨磁性MWCNTs对异构体的吸附速率,称取0.16,g磁性MWCNTs分别加入到盛有200,mL浓度为30,mg/L的邻硝基苯酚、间硝基苯酚、对硝基苯酚溶液中,溶液的初始pH值为6,恒温 25,℃振荡,每隔一定时间用磁铁分离吸附剂后,取上清液测定吸附后溶液的吸光度,计算得出去除率和吸附量.磁性 MWCNTs对水中硝基苯酚的去除率曲线如图 5所示.
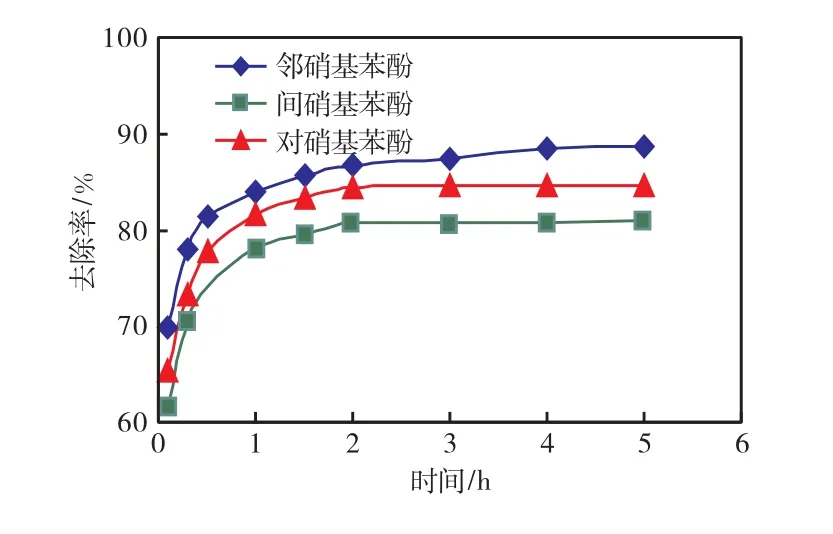
图5 磁性MWCNTs对水中三种硝基苯酚异构体的去除率曲线
由图5可见:在1,h内硝基苯酚各异构体的去除率就达到70%以上,原因或许是在初始阶段有大量未被占据的表面位点可用于吸附,而且还可能包括了吸附质与MWCNTs上含氧官能团的相互作用的贡献;在2,h时去除率缓慢达到80%以上,随后在3,h时达到平衡.由此可选择适宜的吸附时间在3,h左右.在吸附的中后期,去除率增加缓慢的原因可能是MWCNTs表面的吸附质达到饱和,MWCNTs上的吸附质分子与液相中的同种分子产生斥力,使得剩余的空表面位点很难被占据,迫使吸附质缓慢地向 MWCNTs的空腔内扩散而产生的结果[12].
3 结 论
(1)磁性 MWCNTs对于邻硝基苯酚、间硝基苯酚、对硝基苯酚的吸附主要发生在表面分布的活性位点上,三种异构体的去除率随 MWCNTs投加量的增加而增大;在投加量达到0.8,g/L时,基本达到最大去除率;虽然再增加投加量,其去除率还会增大,但增大不是很明显.所以根据实际应用以及从经济因素考虑,适宜的投加量选择0.8,g/L.
(2)硝基苯酚的三种异构体在酸性(pH<6)与碱性(pH>7)介质中的去除率都不是很好,说明反应不宜在酸性或碱性条件下进行.在pH为5~6间的去除率为 80%~90%左右,说明反应体系适宜在近中性条件下进行.考虑到酚类废水显弱酸性,所以选择适宜的pH值为6.
(3)三种药物的去除率均随时间的增加而增大;在3,h以后,去除率基本不再增大,说明吸附达到平衡.
[1]陈光才,沈秀娥. 碳纳米管对污染物的吸附及其在土水环境中的迁移行为[J].环境化学,2010,29(2):159-168.
[2]UPADHYAYULA V K K,DENG Shuguang,MITCHELL M C,et al. Application of carbon nanotube technology for removal of contaminants in drinking water:a review[J]. Science of the Total Environment,2009,408(1):1-13.
[3]熊振湖,王 璐,周建国,等. 磁性多壁碳纳米管吸附水中双氯芬酸的热力学与动力学[J].物理化学学报,2010,26(11):2,890-2,898.
[4]ZHANG Shujuan,SHAO Ting,KARANFIL Tanju. The effects of dissolved natural organic matter on the adsorption of synthetic organic chemicals by activated carbons and carbon nanotubes[J].Water Research,2011,45(3):1,378-1,386.
[5]EL-SHEIKH A H,AL-DEGS Y S,AL-AS'AD R M,et al. Effect of oxidation and geometrical dimensions of carbon nanotubes on Hg (II)sorption and preconcentration from real waters[J]. Desalination,2011,270(1/3):214-220.
[6]GONG Jilai,WANG Bin,ZENG Guangming,et al.Removal of cationic dyes from aqueous solution using magnetic multi-wall carbon nanotube nanocomposite as adsorbent[J]. Journal of Hazardous Materials,2009,164(2/3):1 517-1 522.
[7]朱仙弟,梁华定,赵松林,等. 碳纳米管对2-硝基苯酚和 2,4-二氯苯酚的吸附特性研究[J].安全与环境学报,2008,8(2):40-43.
[8]LU Chungsying,SU Fengsheng,HU Suhkai. Surface modif i cation of carbon nanotubes for enhancing BTEX adsorption from aqueous solutions[J].Applied Surface Science,2008,254(21):7 035-7 041.
[9]ZHANG Qi,ZHU Meifang,ZHANG Qinghong,et al.The formation of magnetite nanoparticles on the sidewalls of multi-walled carbon nanotubes[J].Composites Science and Technology,2009,69(5):633-638.
[10]唐登勇,杨 洋,郑 正,等. pH和盐对活性炭纤维吸附2,4-二硝基酚的影响[J].环境科学与技术,2009,32(6):41-44.
[11]KOYUNCU Hülya,Nuray Yıldız,Uğur Salgın,et al.Adsorption of o-,m- and p- nitrophenols onto organically modif i ed bentonites[J].Journal of Hazardous Materials,2011,185(2/3):1,332-1,339.
[12]PAN Bo,XING Baoshan. Adsorption mechanisms of organic chemicals on carbon nanotubes[J]. Environmental Science & Technology,2008,42(24):9,005-9,013.
Study on Magnetic Multi-walled Carbon Nanotubes Adsorbing Isomers of Nitrophenols in Aqueous Solutions
XIONG Zhen-hua,b,HU Pina,b,WANG Lua,b
(a. Tianjin Key Laboratory of Water Quality Science and Technology;b. Department of Environmental and Municipal Engineering,TIUC,Tianjin 300384,China)
This paper studies the three isomers of nitrophenols in aqueous solutions (o-nitrophenol, m-nitrophenol,p-nitrophenol) adsorbed by magnetic MWCNTs, and examines the impact of the factors such as dosage of magnetic MWCNTs, adsorption time, and pH values of the aqueous solutions on the adsorption process. The results show that the removal of the three isomers increases and then decreases as the pH value in aqueous solutions increases. When the initial concentration of three isomers of nitrophenols is 30 mg/L, respectively, the adsorption of o-nitrophenol, m-nitrophenol,p-nitrophenol by magnetic multi-walled carbon nanotubes has the optimum conditions: the best dosage of magnetic MWCNTs is 0.8 g/L, the pH value 6, the react time is 3 h. Under above conditions, the removal of the three isomers of ni-trophenols comes up to over 80%~90%.
magnetic MWCNTs;nitrophenols;isomers;characterization;adsorption
X703.1
A
1006-6853(2011)02-0109-05
2011-04-06;
2011-04-16
国家自然科学基金(50878138)
熊振湖(1956—),男,天津人,天津城市建设学院教授,博士.

