水热氧化法处理焦化废水的催化剂研究
贾雅楠,裴培
(1.河北联合大学 轻工学院,河北唐山 063000;2.首钢京唐钢铁联合有限责任公司,河北 唐山 063000)
0 引 言
水热氧化法是一种非常有效的化学氧化技术,特别适用于有毒有害的和高浓度的有机废水的处理,是有效的处理技术,但由于实验的温度、压力仍较高,热能及动力的消耗较大,其技术的经济性是需要考虑的。国内方振炜[1]等人进行了催化湿式氧化处理焦化高浓度废水的研究。陈瑞勇等[2]人对超临界水氧化处理焦化废水进行了初步研究。为进一步提高有机物的氧化去除率,并实现在更低的操作温度、压力下达到同样甚至更好的效果,以降低处理成本,因而对催化剂进行了进一步的研究。
1 实 验
1.1 实验材料
1.1.1 模拟废水
模拟废水:由苯酚(分析纯,产自北京化工厂)和去离子水配置而成。参考钢铁行业的焦化废水的含酚量通常在300 mg/L~4000m g/L,配制了以下浓度的溶液:苯酚溶液浓度依次为0.00532m ol/L(500 mg/L), 0.01064 mo l/L(1000 mg/L),0.01596 m ol/L(1500 mg/L),0.02128 mo l/L(2000 mg/L),0.0266 mo l/L (2500mg/L);其化学需氧量用COD0表示约为0.035mol/L(1120 mg/L),0.07 mol/L(2240 mg/L),0. 105 mol/L(3360mg/L),0.14mol/L(4480m g/L),0.175mol/L(5600mg/L)。
1.1.2 氧化剂
由市售双氧水(30%)配置而成,产自天津市东方化工厂。
1.1.3 焦化废水
实验中所用焦化废水取自某焦化厂,其废水中各项污染物含量见表1。焦化废水GC-MS分析结果,通过与NIST标准质谱图库对比检索,检出21种主要有机物,以酚类化合物为主要组分。另外有少量环烷烃和氮杂环化合物如喹啉、吲哚等。

表1 焦化废水中各项污染物含量
1.2 实验装置及实验步骤
本实验所用的装置为连续式超临界水氧化装置,如图3所示。试验条件为10~20 MPa,温度为433 K~573 K。实验中将模拟含酚废水与H2O2分别置于储液罐中,开动双柱塞泵,升温,调节流量以实现不同的停留时间,系统的压力由末端的背压阀控制。待反应温度,压力,停留时间达到实验条件后保持系统稳定15 min后,收集液相流出物并测定其COD。COD值采用多功能水质分析仪测量,型号为NOVA 60,产自德国。

图1 连续式超临界水氧化流程图
2 结果与讨论
2.1 催化剂的选择
催化反应在生产中有很重要的作用,催化剂的使用是提高反应速率和控制反应方向的一个最有效的方法。催化剂不改变平衡状态,但可以改变反应途径,使反应有可能选择比原来途径更为省力的新途径进行。报道的催化剂根据其主组分主要有金属,金属盐,氧化物,复合氧化物和光敏化半导体五大类。归纳如表2。研究表明对有机物水热氧化,多种金属具有催化活性。其中贵金属系催化剂的活性高,寿命长,适用广,但价格昂贵,应用受到限制。目前,多致力于非贵金属催化剂的研发。根据催化剂的使用状态,可分为均相催化剂(溶解金属盐)和非均相催化剂(固相)催化剂两大类。一般来说,均相催化剂比非均相催化剂活性高,反应速度快,反应设备简单,但金属离子流失引起二次污染并使处理成本增高。采用非均相催化法虽然催化剂与废水分离比较容易,处理流程短,但相间有传质阻力。废水悬浮物和反应中间产物可能引起催化剂颗粒被包覆或堵塞而使其失活。且从本实验的实验条件出发,反应器为连续式反应器,因而适宜采用均相催化剂。

表2 水热氧化催化剂
常用的均相催化剂为可溶性的过渡金属盐类,尤其是金属离子具有两种价态或更多价态,几种价态间可发生氧化还原反应,并能与过氧化物生成自由羟基,它们以溶解离子的形式混合在废水中,具有较好的催化效果。本文又考虑到作为催化剂的金属离子容易获得、便宜、且毒性较低,因而选用Cu(NO3)2、Fe(NO3)3、Ni(NO3)2、M n(NO3)2四种盐类进行研究。
2.2 催化湿式氧化实验
本实验在如下条件下进行:压力为15 MPa,温度为380~520 K,停留时间为222 s,K=2,苯酚初始浓度为0.00532 mol/L(500 mg/L),参考相关文献,催化剂用量定为0.08×10-3mol/L。由图2可以看出,Cu (NO3)2的苯酚氧化的催化效果较好,在413K的低温条件下,即可达到95%的转化率。催化效果较好的其次是Fe(NO3)3,再次是Ni(NO3)2,且从实验结果看M n(NO3)2对苯酚氧化没有催化作用,分析其原因一方面可能因为其结构所致,另一方面在反应过程中,高温下其溶解度很小,其沉积在反应器壁上,形成非均相催化剂,降低了催化作用。
如图3,可以看出,当采用Cu(NO3)2做催化剂,温度在413 K时,COD就可去除到56 mg/L。较之未加催化剂的氧化时温度为489 K,COD值为135mg/L。因此,加入催化剂可在更低的温度下达到与未加催化剂在较高的温度下的效果相同。

图2 催化剂的使用对COD转化率的影响

图3 温度对COD去除率的影响
2.3 动力学方程的建立
在未加催化剂情况下,对其活化能用最小二乘法进行回归,结果为18.47 k J/mol,其动力学方程为:

在Cu(NO3)2催化作用下,对其活化能用最小二乘法进行回归,结果为10.06 kJ/mo l,其动力学方程为:
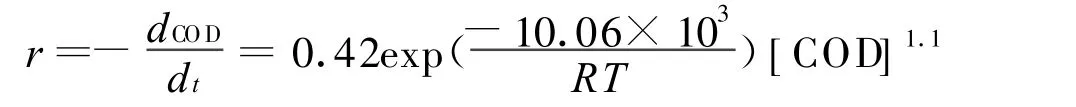
图4为实验值与计算值的比较,最大误差为5%,因此回归的动力学方程是适用的。

图4 COD去除率计算值与实际值对比
由所回归的动力学方程与未加催化剂的动力学方程相比较可以看出,催化剂的使用大大降低了反应活化能,对大量放热反应可以降低反应温度,使反应在更有利的热力学条件下进行。从而提高了生产率,减少了设备耗损和避免了催化剂因过热而烧结的情况。
2.4 实际焦化废水催化氧化实验
从以上实验结果可知,硝酸铜对苯酚含苯酚废水催化效果较为明显,其加入大大降低了反应活化能。因而在本实验中以硝酸铜为催化剂。
2.4.1 对COD的影响
图5为538 K、15 MPa、氧化剂过量倍数K=1.5的反应条件下,催化剂对焦化废水中COD去除率的影响。
总体上,随催化剂用量的增加,COD有所降低,但当铜离子浓度达到0.16×10-3mol/L(即铜离子的质量浓度达到40mg/L)后,催化作用则不明显,一味的增加催化剂用量对COD去除效果没有影响且反而会引入新的杂质铜离子,因而催化剂的用量不宜超过40 mg/L。

图5 催化剂对焦化废水中COD浓度的影响
2.4.2 对NH3-N的影响
图6为538 K、15 MPa、氧化剂过量倍数K=1.5的反应条件下,催化剂对焦化废水中NH 3-N去除率的影响。
且从以上实验看出经过处理后NH3-N的浓度相对原始废水中含量不但没有下降而且有所升高,分析原因,同样是上述原因:由于废水肿的喹啉、吲哚等含氮有机物在超临界水中热解形成了额外的氨,导致最终出水NH3-N含量增加,而实验中的停留时间不足以提供氧化NH 3-N的时间,而且硝酸铜在此反应中没有起到催化作用。因此,若想彻底去除NH 3-N,应增加停留时间。
根据秋常研二的报道,三井东压化学株式会社用CWAO法处理丙烯请废水实践,以铜离子为催化剂,以氨为铜离子的稳定剂,因而可得出结论,铜离子对氨没有催化作用。处理出水加碱蒸氨,并使铜沉淀出来,残留的铜以螯合树脂或离子交换树脂加以回收。由这个实验也可看出,铜系催化剂不分解氨。

图6 催化剂对焦化废水中NH 3-N浓度的影响
以硝酸铜为催化剂的真实焦化废水的催化湿式氧化与苯酚的湿式氧化对比中可以看出,同样的催化剂对不同性质的废水的催化效果不同。由于有机物氧化与其电荷特性和空间结构有很大关系,不同废水有不同的表观活化能,其催化氧化反应历程也不一样,催化氧化得难易程度也是不同的。
3 结 论
(1)通过模拟废水实验,在选择的四种催化剂Cu(NO3)2、Fe(NO3)3、Ni(NO3)2、M n(NO3)2中,Cu (NO3)2的催化效果最好。其加入可大大降低反应活化能,使反应更易进行。
(2)通过焦化废水的催化湿式氧化试验中,使用硝酸铜做催化剂,在铜离子浓度小于40 mg/L的范围内,对COD的去除率作用明显。但对NH3-N的去除没有催化作用。
[1] 方振炜,李光明,赵建夫.催化湿式氧化法处理焦化废水的分析[J].工业水处理,2003,23(1):12.
[2] 陈瑞勇,超临界水氧化处理焦化废水[D].太原:太原理工大学,2005.

