生淀粉糖化酶高产菌株诱变选育
孙子羽,迟乃玉,李 兵,王 宇,张庆芳
(1.大连大学生物工程学院,辽宁 大连 116622;
2.大连轻工业大学生物与食品工程学院,辽宁 大连 116034)
生淀粉糖化酶高产菌株诱变选育
孙子羽1,迟乃玉1,李 兵1,王 宇2,张庆芳1
(1.大连大学生物工程学院,辽宁 大连 116622;
2.大连轻工业大学生物与食品工程学院,辽宁 大连 116034)
以细菌 Aeromonas.sp.CNY01为出发菌株,通过紫外 (UV)和硫酸二乙酯 (DES)诱变,获得产酶较高的菌株 CNY01-27-13,酶活达到 98.42 U/mL,比原始菌株酶活提高了 110.52﹪,菌株经过 9次传代,酶活较稳定。
生淀粉糖化酶,紫外诱变,DES诱变,突变株
生淀粉酶一般来说是指可以直接作用、水解或糖化未经蒸煮淀粉颗粒的酶。它为哪一种酶,至今还没有一个严格的定义,因此生淀粉酶所涉及的酶有好几种,α-淀粉酶、β-淀粉酶、葡萄糖淀粉酶、脱枝酶中都有对生淀粉作用的成分[1-5],生淀粉糖化酶 (Raw Starch-digesting Glucoamylase,RSGA)是指那些能够将不经过蒸煮糊化的生淀粉颗粒直接水解成葡萄糖,进而将传统淀粉糖化 (糊化、液化、糖化)三步合一步完成的“葡萄糖淀粉酶”[6],具有良好的节能前景,如果将其应用于无蒸煮的酒精发酵 ,可节约总能耗的 30%~40%[7]。本文报道了用传统的诱变方法对一株生淀粉糖化酶产生菌的选育工作。
1 材料与方法
1.1 材料
1.1.1 菌种
细菌 Aeromonas.sp.CNY01为本实验室保藏菌种
1.1.2 试剂
玉米生淀粉 (北京联合华友商贸有限公司),3,5-二硝基水杨酸。
1.1.3 培养基
平板分离培养基:生淀粉 20 g,NaNO3 2 g,KCl 0.5 g,FeSO4·7H2O微量,K2HPO4 1.5 g,MgSO4·7H2O微量,琼脂 20 g,水 1000 ml,自然 pH,1×105 Pa灭菌 30 min。其中生玉米淀粉在 105℃下干热灭菌 2 h,然后在常温下无菌操作加入。种子培养基:蛋白胨 10 g,酵母膏 5 g,葡萄糖 1 g,K2HPO4 3 g,水 1000 ml,自然pH,1 ×105 Pa灭菌 30 min。
发酵培养基:玉米生淀粉 20 g,NaNO3 3 g,KCl 0.5 g,FeSO4·7H2O微量,K2HPO4 2 g,MgSO4·7H2O微量,水 1000 ml,自然 pH;1×105 Pa灭菌 30 min。其中生玉米淀粉在 105℃下干热灭菌 2 h,然后在常温下无菌操作加入。
1.2 方法
1.2.1 酶活测定方法
2%的生淀粉悬浮液 2.0 mL加入到 25 mL具塞比色管,添加 pH5.4柠檬酸 -柠檬酸钠缓冲液 2 mL,30℃预热 10 min,加入 1.0 mL酶液,于 30℃恒温振荡 (180 r/min)反应 10 min后,加入 DNS试剂 2 mL终止反应。摇匀,置沸水浴中煮沸 5 min。取出后流水冷去,加蒸馏水定容至 20 mL。以不加酶液管作为空白调零点,在 520 nm波长下比色测定吸光度值。酶活力单位的定义:在分析条件下 ,1 min释放 1μg的还原糖 (以葡萄糖计算)所需的酶量定义为 1个酶活力单位。
1.2.2 诱变方法
菌悬液制备:用接种环挑取活化后的菌体于无菌的盛有玻璃珠的三角瓶中,充分振荡15min,制成均匀的悬液,调整菌体浓度为 108个/mL。
紫外诱变:紫外灯 (30W)预热 1 h,取 5 mL菌悬液注入直径为 9 cm的培养皿中 (内含无菌搅棒),置于磁力搅拌器上,在距离为 30 cm处搅拌照射不同时间。暗室冰浴 2 h,做梯度稀释,选取适当稀释浓度涂选择性平板,20℃避光培养 5 d,计算致死率,在不同照射时间挑选其中D/d值大且生长快速的 10个诱变菌株,在发酵培养基中 20℃培养 36 h后,跟踪测定酶活,计算正突变率[8,9]。
DES诱变:在 100 mL的三角瓶中加入 15 mL pH7.0的磷酸缓冲液和 5 mL菌悬液,再加入 0.2 mL DES溶液混匀,36℃恒温震荡处理不同时间。取 1 mL处理液,加入 1 mL 25﹪的Na2S2O3终止反应,将处理液适当稀释,取 0.1 mL涂布于分离培养基平板,20℃避光培养 5 d,计算致死率,在不同处理时间挑选其中 D/d值大且生长快速的 10个诱变菌株,在发酵培养基中 20℃培养 36 h后,跟踪测定酶活,计算正突变率。
2 结果与分析
2.1 紫外诱变
将菌悬液用紫外线分别照射 10 s、20 s、30 s、40 s、50 s、60 s和 70 s后 ,通过平板计数计算致死率,结果见图 1,摇瓶发酵后计算正突变率,结果见图 2。从图 1和图 2可以看出CNY01最佳正突变率 (44.5﹪)所对应的致死率为 80.57﹪,即紫外灯照射时间为 30 s。
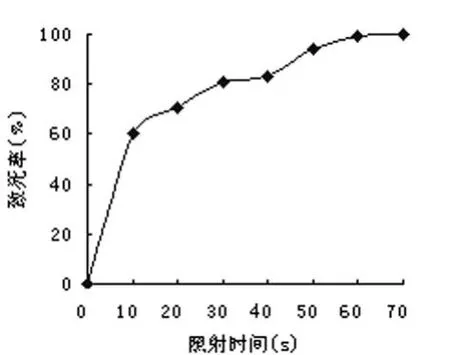
图 1 UV诱变致死率曲线
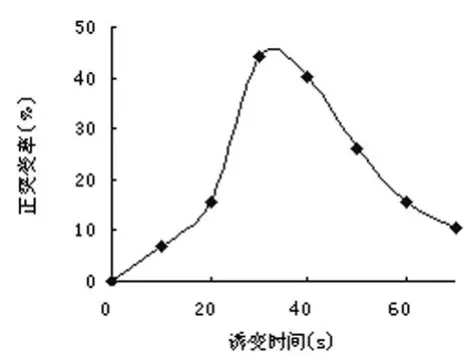
图 2 UV诱变正突变率曲线
经紫外诱变得到的 9株酶活较高的菌株,结果见图 3。有图 3可知,编号为 CNY01-10和 CNY01-27的两株菌酶活最高,其酶活力分别达到 65.3 U/mL和 63.27 U/mL。进一步菌株遗传稳定性检测 CNY01-27要优于 CNY01-10,所以选定 CNY01-27为再次诱变的出发菌株。
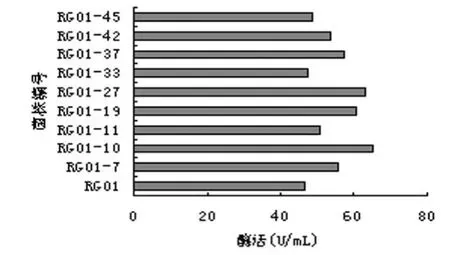
图 3 紫外诱变后突变菌株酶活力
2.2 DES诱变
将以 CNY01-27为出发菌株的菌悬液用DES分别处理 10 min、20 min、30 min、40 min、50 min、60 min和 70 min后,通过平板计数计算致死率,结果见图 4,摇瓶发酵后计算正突变率,结果见图 5。从图 4和图 5可以看出CNY01-27最佳正突变率 (30.24﹪)所对应的致死率为 87.67﹪,即 DES处理 20 min。
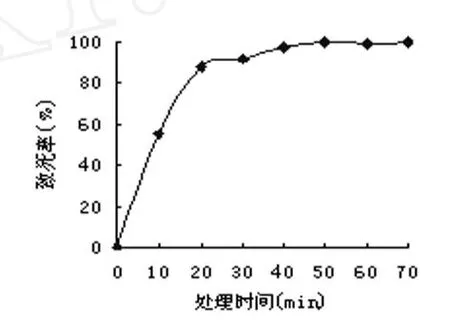
图 4 DES致死率曲线

图 5 DES诱变正突变率曲线
经 DES诱变处理得到 6株正突变菌株,结果见表 1。对这 6株菌株进行遗传稳定性检验,发现 CNY01-27-13连续传代产酶比较稳定,其结果见图 6。
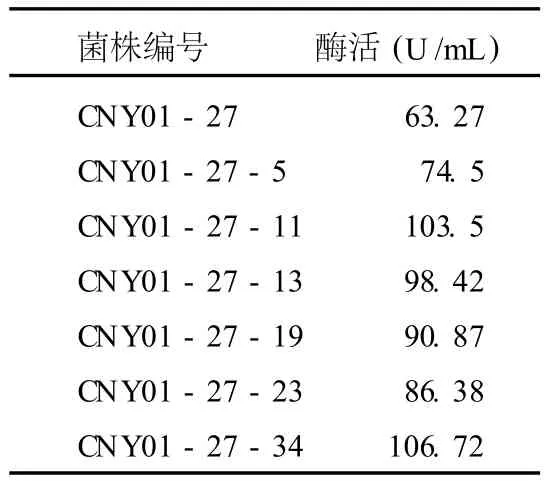
表 1 DES诱变后突变菌株酶活力
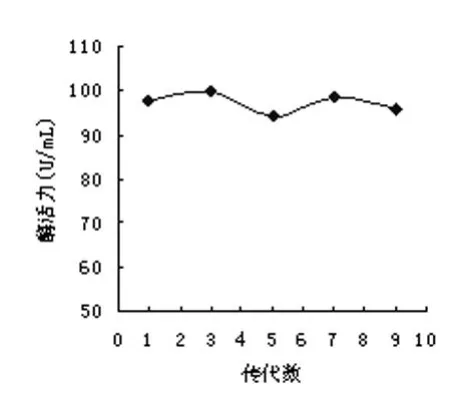
图 6 CNY01-27-13菌株产酶稳定性
由图 6知,CNY01-27-13菌株产酶比较稳定,测定的传代酶活分别为 97.69 U/mL、99.5 U/mL、94.3 U/mL、98.35 U/mL和 95.8 U/mL,而其他 5株菌随着传代数的增加,酶活力下降幅度都比较大。所以最终选定CNY01-27-13作为以后发酵产酶的出发菌株。
3 结论
以本实验室筛选得到的一株细菌Aeromonas.sp.CNY01为出发菌株,其初始酶活为 46.75U/mL,通过紫外诱变 (UV)得到菌株CNY01-27,其酶活达到 63.27 U/mL,比出发菌株提高了 35.34﹪;将菌株 CNY01-27再进行硫酸二乙酯 (DES)诱变,获得产酶较高的菌株 CNY01-27-13,酶活达到 98.42 U/mL,比出发菌株 CNY01-27酶活提高了 55.56%;相比而言,硫酸二乙酯 (DES)诱变要比紫外诱变(UV)效果显著。选育得到的菌株经遗传稳定性试验表明有较好的遗传稳定性。
[1]Favela-Torres E,Cordova-Lopez J,Garcia-Rivero M,et al.Kinetics of growth of Aspergillus niger during submerged[J],agar surface and solid state fer mentations. Process Biochem,1998,33:103-107
[2]Morita H,Fujio Y. High specific activity of raw starch digesting-glucoamylase producing Rhizopus sp.A-11 in liquid culture[J].Starch/starke,1997,49:293-296.
[3]WangWJ,PowellAD,OatesCG.Starch as a biomass source:raw sago starch hydrolysis by commercial enzymes[J].Bioresource Technology,1996,55:55-61.
[4]Volkin DB,Klibanov AM.Thermal destruction processes in proteins involving cysteine[J].Biol Chem,1989,262:2945-2947.
[5]Smith PK,Krohn R I,Hermanson GT,et al.Measurement of protein using bicinchoninic acid[J].Anal Biochem,1985,150:76-85.
[6]诸葛斌,姚惠源,诸葛健.生淀粉糖化酶高产菌的选育[J].微生物学通报,2001,(28):60-64
[7]Fang SK(方善康),Zhou FZ(周凤臻).Purification and some properties ofthree forms ofraw starch digesting glucoamylase from Aspergillus niger S4[J].Acta Microbiol Sin(微生物学报),1993,33(2):108-114.
[8]罗时,谭兴和,苏小军等.马铃薯生淀粉糖化酶高产菌株筛选与诱变研究[J].中国酿造,2009,2:19-22.
[9]郭宏文,江洁,田明等.酸性异淀粉酶产生菌的诱变选育[J].高师理科学刊,2007,27(2):54-56.
Mutating of raw starch-digesting glucoamylase stra in
SUN Zi-Yu1,CH INai-Yu1,L IBing1,WANG Yu2,ZHANGQing-Fang1
(1.Bioengineering College,Dalian University,Dalian,11622,China;2.School of Biological and Food Engineering,Dalian Polytechnic University,Dalian,116034,China)
A mutant strain CNY01-27-13 with high yied of raw starch-digesting glucoamylase was isolated from protoplast of Aeromonas.sp.CNY01 treated by UV and DES.The raw starch-digesting glucoamylase activity of the strain raised to 98.42 U/mL,which was 110.52%higher than the enzyme activity of protoplast strain.The enzyme activity of the mutant strain was very steady cultured by nine times.
raw starch-digesting glucoamylase,UV mutagenesis,DESmutagenesis,mutant
X172 < class="emphasis_bold">文献标识码:A文章编号:
1008-2395(2010)06-0075-03
2010-10-23
张庆芳 (1965-),性别,女,副教授,Email:zhangqingfang@dlu.edu.cn

