大孔树脂对海带多酚的吸附研究
刘晓丽,吴克刚,柴向华,于鸿鹏
(广东工业大学轻工化工学院食品与生物工程系,广东 广州 510006)
大孔树脂对海带多酚的吸附研究
刘晓丽,吴克刚,柴向华,于鸿鹏
(广东工业大学轻工化工学院食品与生物工程系,广东 广州 510006)
以海带总多酚的含量为指标,通过静态吸附与解吸试验对5种大孔树脂进行筛选,XDA-1大孔吸附树脂表现出较好的吸附性能与解吸效果。通过单因素试验,确定XDA-1树脂的较佳动态吸附条件为海带多酚液浓度5mg/mL,上样流速1.0 mL/min,较佳洗脱条件为乙醇浓度80%(体积分数),洗脱速度1.0 mL/min,洗脱体积10 BV,可得到纯度为80.5%的海带多酚。XDA-1型大孔吸附树脂对海带多酚具有良好的富集作用,适于海带多酚的分离纯化。
海带多酚;大孔吸附树脂;纯化
海带(Laminaria Japomica Aresch)是一种重要的经济海藻,在我国分布广泛,其海产量和养殖产量居亚洲之最[1]。海带多酚(kelp polyphenol,KP)作为一类重要的褐藻多酚化合物(phlorotannins),是海带次级代谢产生的以间苯三酚为结构单元的聚合物。褐藻多酚具有较好的抗氧化和抑菌作用,作为天然食品添加剂中的抗氧化剂、防腐剂等方面具有重要的意义[2-3]。此外,褐藻多酚还具有抗肿瘤、抗病毒、化学防御、除臭等活性。近年来,随着对褐藻多酚研究的深入,其独特的生物活性和医药价值日益受到人们的关注[4]。初步提取的海带多酚提取物中多酚物质含量较低,需要进一步纯化。在各种分离纯化方法中,大孔吸附树脂具有性质稳定、选择性强、处理量大、再生方便等优点,在天然产物工业化提取分离中有广泛的应用[5]。本试验以多酚吸附量和解吸率为指标,对5种常用的大孔吸附树脂进行筛选,并研究树脂对海带多酚的动态吸附特性。
1 材料与方法
1.1 材料与试剂
海带多酚提取液:采用料液比[海带匀浆∶乙醇,(g/mL)]1∶8,乙醇体积分数80%,浸提温度70℃,浸提时间4h,浸提次数2次,35℃下浓缩至无醇并进行冷冻干燥。经测定,其中海带多酚的干基含量(纯度)为36.4%。
XDA-1(极性)、LSA-10(中极性)大孔树脂:西安蓝晓交换吸附材料有限责任公司;H103(非极性)、S-8(极性)、AB-8(弱极性)大孔树脂:南开大学化工厂。
没食子酸丙酯:上海生化试剂二厂;其它试剂均为国产分析纯。
1.2 主要仪器
UV-2100紫外可见光分光光度计:上海尤尼柯仪器有限公司;HY-2恒温水浴摇床:江苏金坛市宏华仪器厂;RE-52A旋转蒸发器:上海亚荣生化仪器厂;ALPHA1-4冷冻干燥机:德国CHRIST公司。
1.3 方法
1.3.1 总多酚含量测定
采用Folin-Ciocalteu法测定[6],取样品溶液1 mL,加入5 mLFolin-ciocalteu试剂,摇匀后再加入15 mL 20%的NaCO3溶液,反应2 h。在700 nm波长处测定样品溶液吸光度。以没食子酸为标准品,测得标准曲线方程为:Y=0.0013X-0.0022,R2=0.9994。式中:X 为没食子酸浓度,(μg/mL);Y为吸光度。
1.3.2 大孔吸附树脂的预处理
将树脂用无水乙醇室温下密封浸泡24 h,水洗后用5%(体积分数)盐酸溶液浸泡8 h,水洗至中性,再用5%NaOH溶液浸泡8 h,用水洗至中性备用。
1.3.3 大孔吸附树脂静态吸附量及解吸率测定
将粗海带多酚浓缩液稀释至海带多酚含量为5 mg/mL的溶液。称取经过预处理的5种吸附树脂各1 g置于100 mL三角瓶中,各加50 mL海带多酚溶液,水浴摇床30℃下振摇吸附24 h后过滤,测定滤液中的海带多酚含量。再各用100 mL 80%(体积分数)乙醇,水浴摇床30℃下振摇解吸24 h后过滤,分别测定滤液及洗脱液中海带多酚总量和纯度,按下式计算各树脂吸附量及解吸率:
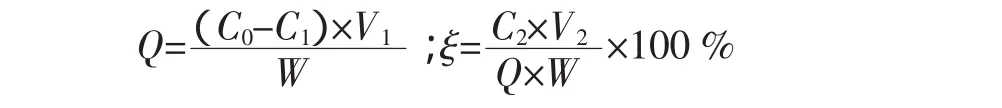
式中:Q 为树脂吸附量,(mg/g);C0为海带多酚初始浓度,(mg/mL);C1为滤液中海带多酚的浓度,(mg/mL);V1为滤液体积,mL;C2为洗脱液海带多酚浓度,(mg/mL);V2为洗脱液体积,mL;W 为大孔树脂湿重,g;ξ为解吸率,%。
1.3.4 大孔吸附树脂静态动力学特性测定
按照1.3.3的方法测定树脂在t时刻(t=1 h~12 h)时的吸附量Q(mg/g),以Q对t做图,得树脂对海带多酚的吸附动力学曲线。
1.3.5 大孔吸附树脂吸附等温曲线的测定
称取各型号树脂0.5 g,加入不同浓度的海带多酚水溶液20 mL,置水浴摇床,30℃振荡24 h后测定水溶液中海带多酚含量,计算吸附量,以吸附平衡后水溶液中海带多酚浓度为横坐标、此时树脂吸附量为纵坐标绘制各树脂对海带多酚的吸附等温线。
1.3.6 大孔树脂对海带多酚的动态吸附
取一定量预处理过的大孔树脂,湿法装入1.6 cm×60 cm玻璃柱,其中树脂装填高度50 cm,树脂体积100 mL。粗海带多酚提取物5 g,配制成浓度为50 mg/mL的水溶液,平衡后以l mL/min流速上样,待吸附饱和后以一定体积分数乙醇溶液洗脱,收集各流出液,测定其中海带多酚的含量、回收率和纯度。

2 结果与分析
2.1 大孔吸附树脂的筛选
2.1.1 不同树脂对海带多酚的吸附与解吸性能
5种不同树脂对海带多酚的静态吸附与解析结果见表1。
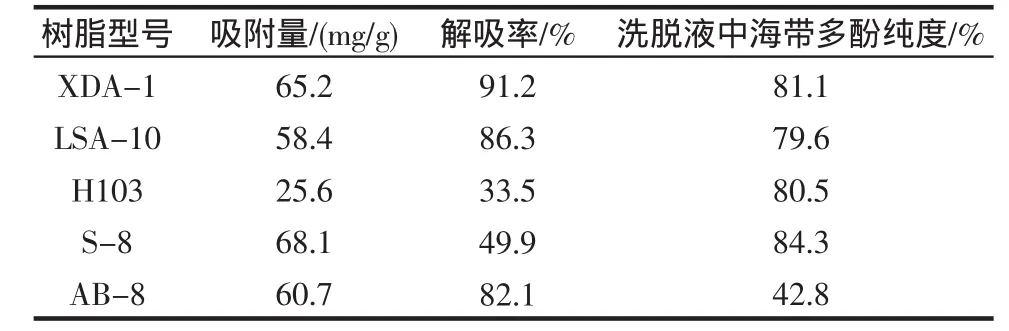
表1 不同大孔树脂对海带多酚的静态吸附性能Table1 Absorbend ability of 5 types of macroporous absorbent resin
由表 1 可见,XDA-1、LSA-10、S-8、AB-8 树脂对海带多酚有较强的吸附能力,H103的吸附能力相对较小。S-8树脂虽然比表面积较小,但由于其极性很强而且孔径较大,对海带多酚甚至杂质均具有很强的吸附能力。从解吸效果及产物纯度来看,S-8树脂的洗脱液中,海带多酚的纯度虽然很高,但海带多酚解吸率很低,说明海带多酚被S-8树脂吸附后很难洗脱,不适于海带多酚的分离。AB-8树脂的吸附量比较大,解吸率也能在80%以上,但其产物纯度不高。LSA-10、XDA-1树脂对海带多酚的选择性较强,而且解吸较容易,解吸率接近90%,海带多酚纯度也比较理想,因此进一步研究这2种树脂对海带多酚的吸附特性。
2.1.2 大孔吸附树脂吸附动力学研究
在有充分时间吸附的情况下,有些树脂可能有相近的饱和吸附量,但各树脂理化性质和结构不同,其吸附动力学过程各异。两种大孔树脂对海带多酚的静态吸附曲线见图1,由图1可以看出,XDA-1和LSA-10在0~2 h内的吸附速率较快,随着时间增加吸附速率急剧下降,然后缓慢趋向饱和,4 h后吸附已经进入相对平衡的状态。XDA-1树脂的吸附量也在4 h后发生吸附平衡,平衡时的吸附量高于LSA-10。
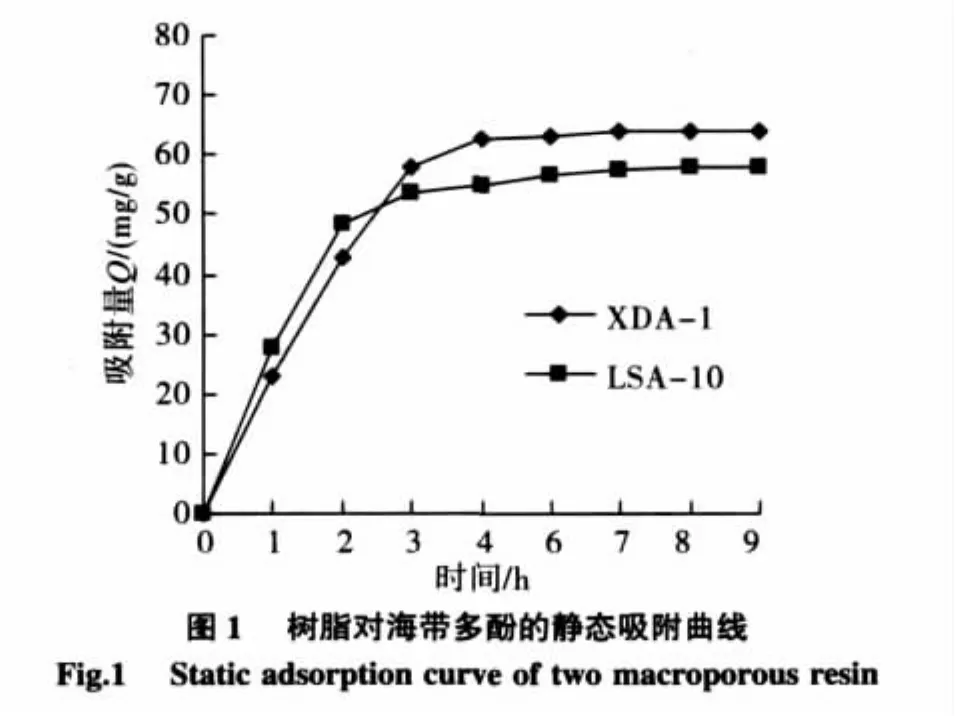
2.1.3 大孔吸附树脂吸附等温曲线
两种大孔树脂对海带多酚的吸附等温线见图2。
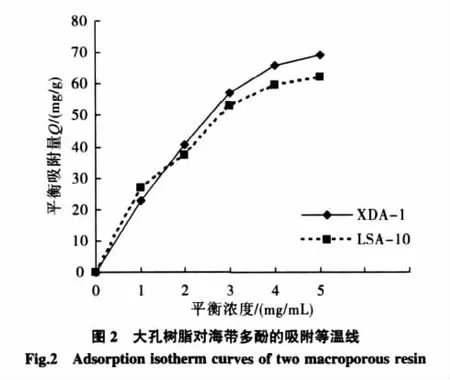
由图2可以看出,一定范围内树脂对海带多酚的平衡吸附量随着样液中海带多酚浓度的增加而增加,吸附等温线的初始阶段几乎呈线性的,表明低浓度海带多酚可以在树脂中高度扩散,溶液中的其他成分不会对树脂有效吸附位点产生强的竞争效应[7]。由于海带多酚在大孔树脂上可以进行吸附和洗脱是可逆行为,其发生的吸附是以范德华引力为基础的物理吸附,以树脂对海带多酚的吸附等温线拟合固体表面的吸附模型:Langmuir吸附等温式及Freundlich吸附经验公式[8]进行探索。
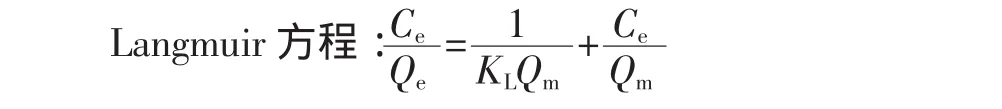
Freundlich吸附经验公式:Qe=KFCen即:lnQe=nlnCe+lnKF
式中:Qe为平衡吸附量,(mg/g);Ce为平衡浓度,(mg/mL);Qm为饱和吸附量,(mg/g);KL为结合常数,(mL/mg);KF,n 为等温吸附特征常数,KL可以评价吸附量的大小,n则可描述等温线的变化趋势[8]。将图2的相关数据用Langmuir方程和Freundlich线性方程拟合,分别得到相应各回归方程及其参数见表2。
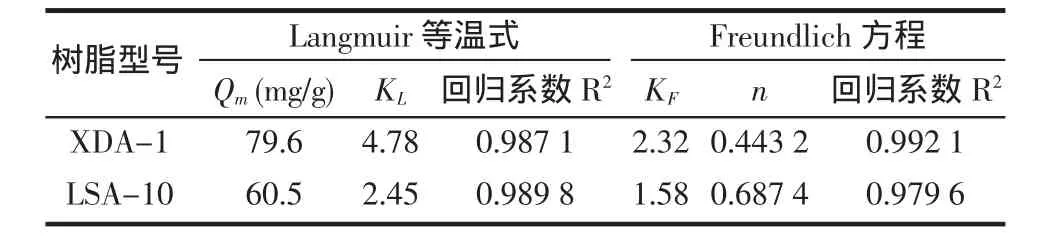
表2 等温线拟合Langmuir及Freundlich方程的参数Table2 Regression Equation and Model Parameters of Langmuir and Freundlich
从表2的线性回归结果可以看出海带多酚在XDA-1和LSA-10树脂上的吸附符合Langmuir方程和Freundlich方程(二者相关系数均达到0.95以上)。根据Langmuir等温吸附模型的假定,可以认为在所研究的浓度范围内各树脂对海带多酚的吸附为单层吸附。XDA-1树脂的Freundlich模型的等温吸附特征常数n值介于0.1~0.5之间,为“优惠吸附”[9],说明海带多酚在XDA-1树脂上的吸附更容易实现。同时,由Langmuir等温方程常数可以看出XDA-1树脂具有较高的最大吸附量,与静态吸附的结果相一致。因此选用XDA-1树脂进行下一步的试验。
2.2 XDA-1树脂的静态吸附解析研究
2.2.1 样品浓度对树脂吸附量的影响
样品浓度对海带多酚吸附量的影响见图3。
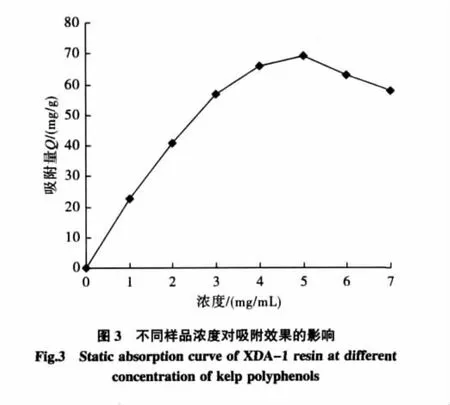
由图3可见,在多酚浓度较低的条件下,随着浓度的提高,多酚的吸附量也随着增加,但是随着料液浓度的提高,尤其是样液浓度超过5 mg/mL后,吸附量却随着样液浓度的增加而减少,这可能是因为在多酚溶液浓度较低时,增加试液浓度,可以增加多酚分子与树脂的接触,加速多酚进入树脂内部并迅速扩散,而当试液浓度增加至一定量后,继续升高浓度,树脂接触表面多酚分子过多,阻碍其他多酚分子进入树脂内部,影响多酚分子在树脂内部的扩散,导致树脂吸附量有所下降[9]。同时,浓度增加,试液中能与多酚竞争吸附的杂质也会增加,因此,样液浓度控制在5 mg/mL左右为宜。
2.2.2 解吸剂的选择
为尽可能提高海带多酚的回收率,通常选用解吸率较高的溶剂作为解吸剂,考虑到海带多酚一般要应用在食品及医药行业中,因此选用乙醇作为解吸剂,考察乙醇浓度对解吸率的影响,见图4。
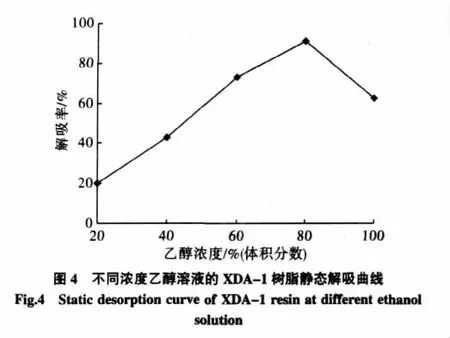
结果如图4所示,随着乙醇浓度增加,解析率先升高后下降。当乙醇浓度为80%(体积分数)时,解吸率达到最大,为90.8%。因此,选用80%乙醇溶液对海带多酚进行洗脱。
2.3 XDA-1大孔树脂对海带多酚的动态吸附研究
2.3.1 上样速度对树脂吸附量的影响
上样速度对海带多酚动态吸附量的影响见图5。
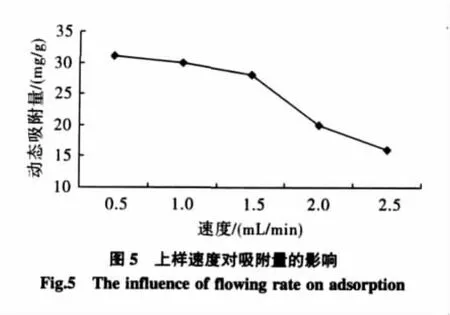
由图5可知,随着上料液流速的增加,多酚物质的吸附量降低,这是由于当上样液流速过大时,多酚物质还未扩散到树脂的内表面,就被冲出柱子,从而造成吸附量快速下降。虽然低流速对吸附有利,但流速过低又会影响到生产效率,使生产周期延长,提高生产的成本。综合考虑,上料液流速以1.0 mL/min较为适宜。
2.3.2 动态洗脱曲线
吸附饱和的XDA-1树脂,用少量水洗去吸附的可溶性糖类,再用10 BV(柱体积)的80%(体积分数)的乙醇洗脱,洗脱速度为1.0 mL/min,测定室温下乙醇溶液对树脂吸附的多酚物质的动态洗脱效果,洗脱曲线见图6。

由图6可以看出,动态条件下XDA-1树脂上吸附的多酚物质极易洗脱,只用很少量的洗脱剂即可使树脂柱上吸附的多酚物质洗脱下来。多酚物质的洗脱高峰也相对比较集中,当洗脱体积为25 mL~65 mL时,洗脱液中的海带多酚含量较高。合并多酚含量较高的试管测定回收率达到84.7%。合并的多酚洗脱液浓缩后,冷冻干燥,测得海带多酚的干基含量 (纯度)为80.5%。
3 结论
1)对5种大孔吸附树脂的静态吸附和解吸效果进行了比较和筛选,得出XDA-1树脂对海带多酚的吸附量较大、解吸率高、选择性好。
2)当多酚液浓度为5 mg/mL,上样流速1.0 mL/min时,XDA-1树脂对海带多酚的吸附量较大。
3)80%(体积分数)乙醇溶液作为解吸剂时,解吸率可达到90.8%。动态吸附时,洗脱速度为1.0 mL/min,海带多酚的动态吸附回收率达到84.7%,且洗脱峰集中,对称性好,无明显拖尾现象。
4)XDA-1型大孔吸附树脂对海带多酚具有良好的富集作用,适于海带多酚的分离纯化,纯化后可得到纯度为80.5%的海带多酚。
[1]王飞久,刘涛,段德麟,等.海带种质特征[J].海洋水产研究,2004,25(1):48-50
[2]Wang T,Jón sdóttir R, 譫lafsdóttir G.Total phenolic compounds,radical scavenging and metal chelation of extracts from Icelandic seaweeds[J].Food Chemistry,2009,116(1):240-248
[3]Yun B K,Young G M,Moon S H.Antioxidant and antimicrobial activities of seaweed,Ecklonia cava[J].Journal of Biotechnology,2008,136(1):S598
[4]Chew Y L,Lim Y Y,Omar M,et al.Antioxidant activity of three edible seaweeds from two areas in South East Asia[J].LWT-Food Science and Technology,2008,41(6):1067-1072
[5]周剑,丁玉峰.大孔吸附树脂分离中草药有效成分的应用[J].中国医院药学杂,2006,2(1):69-70
[6]Singleton V L,Rossi J A.Colorimetry of total phenolics with phosphomolybdicphosphotungstic acid reagents[J].American Journal of Enology and Viticulture,1965,16(3):144-158
[7]Silva E M,Pompeub D R,Larondelle Y,et al.Optimisation of the adsorption of polyphenols from Inga edulis leaves on macroporous resins using an experimental design methodology[J].Separation and Purification Technology,2007,53(3):274-280
[8]王正烈,周亚平,李松林,等.物理化学(下册)[M].4版.北京:高等教育出版社,2003:167-168
[9]艾志录,王育红,王海,等.大孔树脂对苹果渣中多酚物质的吸附研究[J].农业工程学报,2007,23(8):245-248
Adsorption of Polyphenols from Laminaria Japomica by Macropous Absorbent Resins
LIU Xiao-li,WU Ke-gang,CHAI Xiang-hua,YU Hong-peng
(Department of Food Science and Bioengineering,Faculty of Chemical Engineering and Light Industry,Guangdong University of Technology,Guangzhou 510006,Guangdong,China)
Taking the contents of total polyphenol as index,static adsorption and desorption experiments were carried out to screen the suitable resin from 5 types of macroporous absorbent resin for kelp polyphenol(KP).Results indicated that macroporous resin XDA-1 possessed the strongest absorbend ability and easier desorption property,which is a better candidate for KP purificating.Through single factor experiments,the optimum adsorption conditions of macroporous resin XDA-1 were concentration of feed 5 mg/mL,feeding rate 1.0 mL/min,and the optimum desorption conditions were elute-ethanol concentration 80%,elution rate 1.0 mL/min,elute volume 10 BV.Under the conditions,80.5%the purification of KP was obtained.The results showed,the purity of the KP was effectively improved by macroporous resins XDA-1.
kelp polyphenol;macroporous absorbent resin;purification
广东省科技计划农业攻关项目(2007A02030008-2);广东工业大学博士启动基金(083056)
刘晓丽(1977—),女(汉),讲师,博士,研究方向:食品添加剂与食品保鲜。
2009-08-26

