大肠癌肝转移机制及诊治进展
施东华 王小林
大肠癌发病率在欧洲国家跃居第1~2位,在中国居第4~6位[1]。大肠癌是国内常见的肿瘤之一,近年来发病率逐年上升。肝脏是大肠癌转移最常见的器官,约25%的大肠癌患者同时存在肝转移,另有30%~40%的大肠癌患者出现晚期肝转移。在晚期大肠癌病例中,近45%的患者死于原发病,83%的大肠癌复发病人出现肝转移,肝转移是原发灶切除后及晚期大肠癌患者最主要的死因。因此,对大肠癌肝转移发生机制的探索及如何早期诊治原发肿瘤和肝转移灶以延长患者生存期是目前的研究热点。
转移机制
大肠癌肝转移受多种基因调控,是多步骤而又连续的、十分复杂的生物学现象,其发生机制至今仍不甚明确。目前,对大肠癌肝转移机制的研究主要集中在原癌/抑癌基因测定、肿瘤转移相关分子的确定、肿瘤转移所涉及的信号转导过程等。
1.分子生物学过程
癌细胞恶性增殖是浸润转移的基础。肿瘤浸润包括黏附、基质降解与迁移三个步骤。由胶原、糖蛋白和蛋白多糖组成的基底膜是机体重要屏障。癌细胞的表面受体识别并黏附基底膜糖蛋白,2~8h后癌细胞分泌多种蛋白酶,以降解基底膜和细胞外基质(ECM)。通过基底膜被降解部位,癌细胞伸出伪足,向周围组织间质迁移。癌细胞识别与黏附血管内皮细胞需1h,4h可穿透血管内皮,24h完全移至血管外。
2.基因组测定
大肠癌的发生和发展包括了许多基因多种形式的先天及后天改变,如Ki-ras,p53,APC、β-catenin和AXIN2等常见的基因突变。但我们对肿瘤形成及转移的过程缺乏全面深入的理解,目前的许多研究也仅局限于有限的几个分子标志物。Ki等[2]利用cDNA基因芯片分别测定了正常大肠黏膜、癌变大肠黏膜及相应肝转移灶、无肝转移的大肠癌病灶及正常肝组织的基因序列,并最终通过RT-PCR半定量分析确定了伴和不伴肝转移的大肠癌中21个差异表达基因。这一研究可能为我们研究大肠癌肝转移相关基因提供线索,对于将来肿瘤治疗的靶位确定以启示。目前报道的参与大肠癌转移过程的癌基因还包括m yc、S100A4、c-erbB-2、c-met、M TA1、DPC4等 。m yc基因编码细胞核内蛋白质,c-myc的扩增与大肠癌淋巴结转移相关。有研究发现血清中c-erbB-2的水平与大肠癌演进晚期及肝转移相关。另外,越来越多的学者认为:大肠癌抑癌基因的失活也是其发生侵袭生长的主要原因,抑癌基因DCC、nm23、K AI1、p27、p21、Sm ad4,金属蛋白组织抑制剂T IMP-2与E-钙黏素基因等在大肠癌侵袭转移中起重要作用。
3.转移相关分子
3.1c-Met蛋白:c-Met蛋白是一种由c-met原癌基因编码的蛋白质产物,为肝细胞生长因子受体,具有酪氨酸激酶活性,与多种癌基因产物及调节蛋白相关,参与细胞信号转导、细胞骨架重排的调控,是细胞增殖、分化和运动的重要因素。与原发肿瘤相比,70%大肠癌肝转移灶中存在c-met基因的过度表达,c-met基因的过度表达能够预测肿瘤的侵袭性及可能存在的淋巴结转移。通过对高转移性大肠癌细胞系KM 20母细胞的研究,Gallick等[3]发现,c-met基因表达下调的肿瘤细胞种植于裸鼠盲肠后,新生的肿瘤血管密度显著减少,这与VEGF生成减少有关。而Src的选择性抑制因子PP2能显著降低KM 20母细胞VEGF生成的基线值,这种效应能够被HGF逆转。
3.2 E-钙黏素:E-钙黏附蛋白/连接蛋白复合体是维持上皮细胞的极性、形态和组织结构完整的主要黏附分子,有研究表明大肠癌进展过程中常有复合体功能的丧失,使癌细胞间黏附性降低,易于脱离,E-钙黏附蛋白/连接蛋白复合体的缺失与大肠癌的肝转移相关。可利用抗黏附素、E-钙黏蛋白及基质溶素(MMP-7)三者在大肠癌中的表达程度,对大肠癌潜在的肝转移可能进行预测[4]:3×抗黏附素积分[0=低表达(阳性表达肿瘤细胞≤50%)或1=高表达(>50%)]+4×E-钙黏蛋白积分[0=高表达(阳性表达肿瘤细胞>80%)或1=低表达(≤80%)]+2×基质溶素(MMP-7)积分[0=低表达(阳性表达肿瘤细胞≤30%)或1=高表达(>30%)],从而有望在大肠癌肝转移发生之前,对肿瘤发展过程进行有效干预,防止或延缓肿瘤转移的发生。
3.3整合素:整合素是一类位于细胞膜表面的糖蛋白受体家族分子,主要介导细胞与细胞外基质,细胞与细胞间的黏附,有实验显示整合素在大肠癌肝转移组织中较原发组织表达明显增高,提示其可能在大肠癌肝转移中起重要作用。整合素在肿瘤转移的三个阶段都起着重要的作用[5]:器官靶点、细胞黏附及肿瘤外侵,整合素的这一作用另见于除大肠癌以外的其他肿瘤的转移过程,使得整合素能够成为未来大肠癌肝转移的一个重要的治疗靶点。而目前针对肿瘤转移早期阶段的整合素治疗仍处于实验研究阶段,真正的临床应用尚需假以时日。
3.4选择素:选择素是一类调节钙依赖的白细胞、血小板及内皮细胞间黏附的分子,其中E-选择素与细胞中Lew is唾液酸糖类的结合所诱导的信号通路能够影响大肠癌的转移能力。Lew is唾液酸糖类作为肝血管内皮细胞表面E-选择素受体的配体,介导癌细胞与靶器官血管内皮细胞的黏附:促进癌细胞的趋化运动,从而导致转移高表达Lew is唾液酸糖类的癌细胞更易浸润基底膜,黏附于肝血管内皮上生长并形成肝转移癌。现已明确[6],选择素及其配体为循环中癌细胞-血小板-白细胞栓子的形成提供帮助,这些栓子能使癌细胞免受血流剪应力的作用,而白细胞则能易化肿瘤细胞与内皮的黏附。选择素-选择素配体及其下游分子事件潜在能够成为肿瘤治疗的靶点。
3.5基质金属蛋白酶(MMPs):大肠癌细胞能分泌或诱导分泌多种蛋白水解酶,用以降解基底膜与细胞外基质。已有充分证据表明,肿瘤的转移与其产生或诱导产生降解细胞外基质或基底膜的蛋白酶的能力密切相关,这些蛋白酶包括丝氨酸蛋白酶、金属蛋白酶、弹力蛋白酶、半胱氨酸蛋白酶、尿激酶纤溶酶原激活因子、组织蛋白酶B、组织蛋白酶D等。其中金属蛋白酶家族被认为是一组最重要的蛋白酶,在肿瘤浸润和转移中发挥重要作用,是抗肿瘤转移治疗的一个重要靶点。MMP-2(基质金属蛋白酶-2)的表达与肿瘤浸润的深度、血管受侵程度及肝脏转移有关,它能够用来预测大肠癌肝转移的发生;而MMP-9和RECK基因的表达与肿瘤血管浸润有关[7]。被转染RECK基因的大肠癌细胞,其浸润能力明显下降。金属蛋白组织抑制剂(TIMP)能抑制所有MMP活性形式,其中TIM P-2有显著转移抑制作用。
3.6运动因子:许多运动因子通过调节细胞的迁移参与大肠癌转移过程,它能多方面刺激细胞的运动如迁移、趋化、吞噬等,致癌细胞发生转移。其中最重要的是分裂素,据其功能,将其分为三种:①刺激癌细胞的运动和浸润的因子:如运动刺激因子、自分泌运动因子等。②刺激生长和运动的因子:其中以肝细胞生长因子(HGF)与转移的关系比较密切,HGF通过活化其受体c-met,参与运动信号的产生,可以作为结肠癌转移的标志物。此外,还有表皮生长因子EGF、IL-6和IL-8等。③促进运动而抑制生长的因子:如转化生长因子(TGF)等。
3.7血管生成因子:肿瘤转移与其诱导血管增生的能力关系密切。与血管增生相关的因子包括血小板衍生内皮细胞生长因子(PDGF)、血管内皮生长因子(VEGF)、α-TGF和β-TGF、EGF、纤维母细胞生长因子及肿瘤血管生成因子等。其中VEGF-C的表达水平与大肠癌淋巴结转移及淋巴侵袭相关。大肠癌与对应肝转移灶中的VEGF m RNA水平呈正相关(P=0.0083,r(s)=0.48),且VEGF m RNA水平与VEGFR-1存在相关性[P=0.0026,r(s)=0.39][8]。目前市场上出现的贝伐单抗(阿瓦斯汀)就是一种针对VEGF的靶向治疗药物。
3.8细胞因子:细胞因子(cytokines)是一类主要由免疫细胞和相关细胞产生的高活性、多功能小分子蛋白质。肿瘤坏死因子是一类能直接造成癌细胞死亡的细胞因子,在高转移大肠癌细胞株中高表达,可能通过“免疫逃逸”使大肠癌细胞在血液循环过程中逃脱免疫系统的监测,从而引起肿瘤转移。
3.9转录因子:近年来的研究表明一些核转录因子在癌转移中起重要作用。转录因子NFAT的拮抗剂具有显著的抗肿瘤演进的作用,提示NFAT可能在肿瘤转移中发挥作用。核转录因子NF-κB在很多癌中表达活跃,并调节几种抗凋亡基因的表达。NF-κB可溶性抑制物能显著地诱导黏附的大肠癌细胞发生凋亡,因此是预防大肠癌转移的候选因子。
3.10信号转导因子:已有很多证据支持信号转导可能在肿瘤的发展及转移表型的调控中发挥关键作用,有研究表明:采用特异的信号转导抑制剂对癌症进行试验性治疗是可行的。TGF-β在肿瘤发展早期是一种重要的抑制因子,因为它能抑制细胞周期演进和肿瘤生长,此外,细胞自分泌的TGF-β信号通路也是大肠癌进展晚期诱导和维持体外侵袭和转移所必需的。细胞死亡信号通路的失调与肿瘤的发展及临床进程相关,在伴有肝转移的大肠癌患者中,P53/BAX凋亡通路是一个明确的预后因素。
4.静脉侵袭
大肠癌极少侵袭动脉,而静脉侵袭却很常见。受累静脉包括肠壁内静脉(黏膜下或肌层内)、肠壁外薄壁静脉和厚壁静脉(肠周脂肪结缔组织内)三种。静脉侵袭方式有:①直接侵入静脉。②沿淋巴-静脉通路:淋巴结并非可靠过滤器,部分癌细胞不被淋巴结阻留,而沿淋巴-静脉通路侵入静脉。部分癌细胞能在淋巴管与静脉间自由出入。③渗入静脉:当肿瘤糜烂破溃、血管损伤或承受挤压时,癌细胞即可渗入静脉。如梗阻型大肠癌,由于肠壁肥厚肌层的强力蠕动,肠腔内压升高与长时间挤压肿瘤,驱使癌细胞渗入破裂的静脉。
5.血道转移
肝脏是大肠癌最常见的远处转移部位,其主要有两个原因:首先,肝脏接受大部分腹内脏器的门静脉引流,包括远端食管、胃、脾 、小肠 、结肠、直肠、肾上腺 、胰腺、胆囊和胆管及分支的静脉引流,约占肝血供的70%~80%。此外,肝脏约接受心输出量血液的30%动脉血供。由此,经肝脏滤过的血量仅次于经肺脏滤过的血量。其次,生理特征上,肝脏具有多种能够为肿瘤细胞生长提供优良环境的细胞。经宿主防御系统攻击后仍存留的肿瘤细胞最终到达肝脏,穿过肝窦壁,在肝窦周围间隙内落户,形成小的细胞集落,即所谓的微转移灶。后经恶性增殖与微血管化,成为临床意义上的肝转移癌。如果肿瘤细胞表达出在转移级联过程的任何阶段都容许其运动的合适表型,肿瘤转移随即发生。肝脏因其丰富的血流、高糖而低氧含量状态,以及狄氏间隙内富含营养的滤过液,使其拥有转移癌的最佳生长环境。加之肝脏与多个脏器毗邻,接纳丰富的淋巴引流,这些特点决定了肝脏是全身许多恶性肿瘤最易侵犯和转移的器官,其中尤以大肠癌多见。大量观察表明:①肿瘤转移遵循解剖特点,转移灶常发生在癌细胞迁徙转移过程中最先到达的器官部位;②循环中的癌细胞可以在各种器官内停留,但转移灶却只能发生在某一特定的器官。因此,大肠癌肝转移是癌细胞沿门静脉系统回流,经血道转移至肝脏的结果。
大肠癌肝转移是个复杂而又多样的过程,其机制尚未完全阐明,随着技术的发展和研究的深入,人们将会对大肠癌转移的机制不断有新的认识,从而为大肠癌转移的预防和治疗提供新的方向和思路。
诊断进展
由于肝脏是大肠癌最常见也是最易发生转移的器官,发生肝转移的患者其预后往往欠佳。因此,提高大肠癌肝转移的早期诊断率,对提高大肠癌患者的生存率及改善预后有极其重要的意义,也是目前大肠癌研究的热点。
1.影像学诊断方法
1.1B超检查:术前B超检查是目前应用最广泛的诊断之一,最常见的表现为肝内低回声灶或 “牛眼征”。大于 2.0cm的转移灶 B超检查敏感性可达100%。术中超声检查是诊断大肠癌肝转移的比较有价值的诊断方法之一,对于肝转移癌,不但可以精确地显示病灶,发现大于0.3cm的占位,而且能显示肝内解剖结构,确定肿瘤与肝内血管、胆管的关系,有利于进一步手术治疗。但不同患者之间,其转移灶超声表现也不尽相同,转移灶可表现为低回声(52%)、等回声(35.7%)和高回声(12.3%),少数呈“靶征”(20%)或伴有钙化(19%)[9]。因此,超声检查的准确性还有赖于对临床病史了解及医生的操作经验和诊断水平。
1.2CT检查:CT是大肠癌肝转移最常用的检查手段,但其检查目的除能够发现病灶外,还要判断病灶的性质及肝脏累及程度,对手术可切除性作出判断。另外,行CT动态增强三期扫描,可初步了解病灶的血供情况,有助于介入治疗方案的制定及评价介入治疗的效果。门静脉期的扫描有利于病灶的检出,但动脉期扫描更加有利于富血供病灶的检出。“牛眼征”是转移性肝癌的特征性表现,增强表现为病灶中心低密度,周围环状强化带,最外层呈强化不明显的低密度带,低于肝实质密度。但也可见转移性肝癌的囊性变,增强后CT表现为囊壁厚薄不一,壁内缘常不规则,增强后轻微强化,囊内容物密度不均。大肠癌肝转移的DSA表现可分为肿瘤边缘环状染色、较均匀染色和不染色3种,其中以边缘环状染色最常见[10]。
1.3MRI检查:转移性肝癌在 SET1WI和T2WI上的信号变化多样,T1WI多为中低信号,T2WI上为中高信号。转移性肝癌的典型表现为 “靶征”或“牛眼征”,即在T2WI上病灶中心可见到更高信号,为坏死或伴有出血。MRSE序列结合Gd-DTPA动态增强扫描可进一步提高肝转移癌的检出敏感性和定性准确性。而肝脏特异性造影剂M n-DPDP和SPIO MRI增强扫描更加有利于肝脏小转移灶的检出。
1.4PET检查:PET检查利用18F-FDG作为示踪剂来评价活体细胞的代谢及功能状态。经证实,通常情况下肿瘤细胞的葡萄糖代谢率明显高于周围正常肝组织,通过PET成像肿瘤放射性浓聚的特性来检出肿瘤病灶。18F-FDG探测的敏感性和特异性分别为94%和100%,能检出其他影像学方法未能发现的肝转移灶。
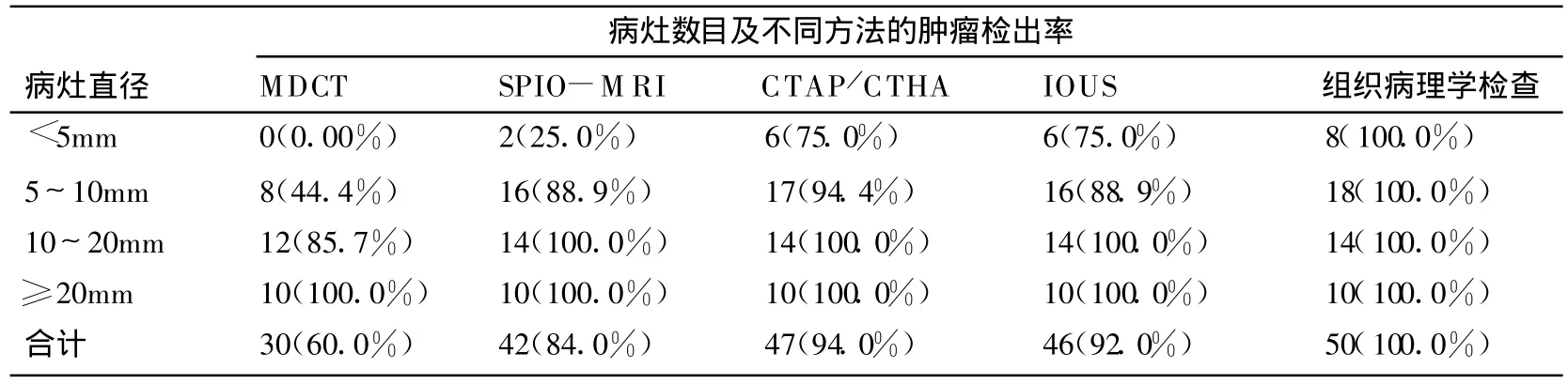
表1 不同大小病灶与不同检查方法肿瘤检出率的关系[11]
表1可以看出,通过对照组织病理学检查,CTAP/CTHA对病灶的检出敏感性最高(94.0%),接下来依次为IOUS(92.0%)、SPIO-MRI(84.0%)和MDCT(60.0%)[11]。
2.大肠癌肝转移生物标志物检测
癌症之所以成为致死率最高的疾病,一定程度上与缺少某种可进行早期诊断的肿瘤标志物有关,临床上确诊肿瘤时往往病情发展至晚期阶段而不能行根治治疗。而对能够早期预测肿瘤发生的敏感性和特异性都较高的肿瘤标志物的检测是临床所期待的。肿瘤标志物的理想来源是实验室检查常用的血清、血浆或尿液标本。这些标本中常包含有各种蛋白质成分有助于肿瘤的诊断。近年来,快速发展的蛋白质技术能够在患者体液标本中检出微量蛋白质,为肿瘤标志物的检测带来便利。在大肠癌,肿瘤的浸润和转移同样与一些蛋白质和调节因子的共同参与有关,这些分子相互协同或相互联系促进了大肠癌肝转移的发生,因此可作为肿瘤转移的生物标志物用于大肠癌肝转移的诊断和预后的判断。
2.1癌胚抗原(CEA):CEA作为免疫球蛋白超家族成员之一的一种癌细胞黏附分子,是大肠癌去分化过程中表达的重要标志和最有价值的肿瘤标志物之一,在大肠癌的复发转移中起重要作用,广泛应用在大肠癌肝转移的早期检测中。原发性大肠癌分泌CEA,导致细胞间连接松弛、排列紊乱和极性消失,从而促进癌细胞迁移、脱落和侵入循环管道;同时被CEA识别并黏附成集落的癌细胞到达肝脏定居,之后降解的CEA成为内源性免疫抑制剂,抑制机体特异性和非特异性免疫反应,协助癌细胞逃避免疫监视,为大肠癌肝转移灶的形成创造有利条件。最近发现CEA mRNA的检测对早期发现肿瘤转移具有较高的敏感性(100%),高于CEA蛋白的敏感性(71.4%)。
2.2细胞间黏附分子-1(ICAM-1):在免疫球蛋白超家族中,ICAM-1在宿主免疫监督体系下可能起抑制肿瘤演进的作用,ICAM-1的表达与大肠癌的转移密切相关,可以作为估计患者预后的因子。
2.3 IL-8:IL-8在正常大肠黏膜组织、大肠癌组织和大肠癌肝转移组织中的表达依次升高,且具有显著性差异,大肠癌组织中IL-8高表达是肝转移的高危因素,检测大肠癌组织中IL-8的表达可以帮助确定肿瘤的分期及预测其肝转移的发生。IL-8在大肠癌的演进及肝转移过程中相当于一种自分泌生长因子调控着细胞的增殖、迁移和肿瘤组织内血管生成。
其他与大肠癌肝转移的发生密切相关的肿瘤标志物包括 E-钙黏素、整合素、选择素和MM Ps等,有关这些生物标志物的介绍见第一部分,恕不赘述。某一生物标志物能够成为肿瘤标志物,就必须对肿瘤预测具有较高的敏感性和特异性,现今临床使用的肿瘤标志物都具有一定的假阴性和假阳性率,其预测价值还有待于进一步评估。相信随蛋白质检测技术的发展及对肿瘤研究的深入,人们能够找到理想的大肠癌肝转移相关标志物。
治疗进展
肝转移是晚期大肠癌患者的主要死因,又由于大肠癌肝转移患者往往处于原发肿瘤的晚期阶段,故临床治疗的效果还与原发肿瘤的临床分期,肝转移灶的数量、部位、与肝内管道的关系,肝门淋巴结是否转移,是否存在肝静脉/门静脉癌栓,是否存在肝外转移等多种因素有关。针对不同的病情采取不同的个体化治疗方案及多学科综合治疗可望延长大肠癌肝转移患者的生存期。
1.外科手术治疗
目前,对孤立性肝转移病例,手术切除是唯一可能根治的方法,能潜在提高5年生存率。但这一治疗方法并不适用于所有患者,对于左右半肝多发转移、瘤体占据1/2肝脏体积以上、肿瘤侵及大血管、有明显肝功能障碍的患者,手术切除又显得无能为力。此时就需要进行肿瘤的多学科综合治疗。最近,国内一项随机对照研究称[12],无明确肝转移的大肠癌患者术前予以肝动脉及肿瘤局部供养血管灌注FUDR及奥沙利铂,能有效降低肝转移的发生率,并延长大肠癌Ⅲ期病人根治术后肝转移的中位时间,但对生存期的影响有待于进一步评估。Quénet等[13]认为,对肝转移癌不能切除的患者,FOLFIRINOX方案(奥沙利铂、伊立替康、亚叶酸钙、氟尿嘧啶)具有较高的治疗反应率(70.6%),在减瘤后有82.4%的病人成功实施了肝转移灶切除术,且26.5%的病人达到R0切除,但此项研究为小样本非随机对照研究。
2.全身化疗
2.1新辅助化疗:新辅助化疗是指以提高手术切除率和根治性,并改善整体治疗效果为目的而于手术前给予的化疗。对于肝转移病灶可切除的病人,新辅助化疗可提高R0切除的机会,增加术后残肝体积,改善术后肝功能状况;对于肝转移病灶不可切除的病人,规范的新辅助化疗可使30%左右病人转为可手术切除,而并不影响术后5年生存率;另外,新辅助化疗可评价肿瘤对化疗药物的敏感性,指导术后化疗,改善病人预后。化疗方案须包含奥沙利铂和(或)伊立替康和5-FU或卡培他滨。
2.2辅助化疗:辅助化疗的目的是降低术后肿瘤复发率。同新辅助化疗一样,辅助化疗的有效性也缺少强有力的前瞻性随机对照的实验资料支持。
2.3姑息化疗:姑息化疗是针对初始和经过规范治疗后都无法手术切除的大肠癌肝转移病人,目的是改善病人的生存质量和延长生存期。
3.介入治疗
大肠癌肝转移是影响疗效及预后的重要因素,约50%的大肠癌患者最终死于肝转移。自从1976年Goidstein首创用肝动脉栓塞治疗肝癌获得成功后,肝动脉栓塞术被公认为是不能手术切除的中、晚期肝癌的重要治疗方法。1984年,我院林贵率先开展了这项工作。有研究表明[14]经动脉途径应用聚N-异丙基丙烯酰胺磁性阿霉素纳米微球 (ADM-PN IPAMFe3O4)联合外加磁场治疗对兔VX 2肝肿瘤生长有较明显的抑制作用,初步肯定ADM-PNIPAM-Fe3O 4是一种有效的介入化疗栓塞剂,但其临床应用还有待进一步探讨。有研究称介入治疗61例消化道肿瘤肝转移患者的有效率(CR+PR)为86.7%,平均生存期为19.2个月,1年、3年、5年生存率分别为91.8%、32.8%、13.1%[10]。目前国内、外对大肠癌肝转移的介入治疗有不少报道,也取得一定成绩。
基因介入放射学是在影像监控或引导下,在基因水平对单基因疾病进行诊断和治疗的技术。大量用于大肠癌肝转移临床前动物模型和早期临床试验的新型分子疗法给临床治疗带来新希望。由于具有亲瘤内选择性复制能力并能够通过溶瘤作用和继发肿瘤感染来杀灭周围癌细胞,溶瘤病毒已成为实体癌治疗中备受关注的新治疗工具[15]。
临床上根据肿瘤的血供情况,肿块的大小、数量,有无动静脉瘘,有无门静脉、下腔静脉癌栓等制定治疗方案,主要有经皮肝动脉栓塞化疗(TACE)、门静脉栓塞术(PVE)、经皮无水酒精瘤内注射(PEI)、经皮射频消融术(PRFA)、冷冻消融术(cryosurgery ablation)、激光消融术(laser ablation)、植入放疗(im plantation radiotherapy)、靶向药物治疗(targeted therapy)等。未来,随着基因治疗药物、更多强有效的分子靶向药物的问世,肿瘤的介入治疗必然会成为最有发展前景的治疗方法之一。
前景展望
近年来,人们对大肠癌肝转移的研究热点主要集中在基础实验研究领域,包括分子及蛋白质水平和信号转导通路变化的研究,大肠原发癌及肝转移灶内基因测定及致癌基因的检测、肿瘤生物标志物的测定、肿瘤转移相关蛋白的确定等。但基础研究最终必将服务临床,为临床提供新的诊断和治疗方法,分子影像诊断及微创靶向治疗技术将成为未来肿瘤的主要诊治手段,同时也为临床更加客观地判断疾病预后提供可靠的评估标准。

