东北地区人参药材最佳产地与生态环境的聚类分析研究△
周海鸥,李秀昌,陈祥涛,李春楠,孙佳明,张辉*
(1.吉林省中医药科学院,吉林 长春 130012;2.长春中医药大学中医药与生物工程研发中心,吉林 长春 130117)
东北地区人参药材最佳产地与生态环境的聚类分析研究△
周海鸥1,李秀昌2,陈祥涛2,李春楠2,孙佳明2,张辉2*
(1.吉林省中医药科学院,吉林 长春 130012;2.长春中医药大学中医药与生物工程研发中心,吉林 长春 130117)
目的:通过测定东北地区22个不同产地的38个人参样品的总皂苷含量,以分析东北地区人参药材的最佳产地与生态环境。方法采用比色法测定人参总皂苷含量,并用SPSS统计分析系统进行聚类分析。结果:长白山南部,为东北地区人参药材的最佳产地;北纬40~42°,东经125~127°区域内,海拔500~1 000m,年平均气温4℃以上的森林地带为东北地区人参药材的最佳生态环境。结论:本方法简便,准确,可行,为人参药材的质量评价及道地药材的科学开发提供了依据。
人参;人参总皂苷;比色法;聚类分析
国家科技支撑计划项目(2006BAI09B05-10)
人参为五加科(Araliaceae)植物人参 Panax ginseng C.A.Mey.的干燥根及根茎,具有大补元气,复脉固脱,补脾益肺,生津,安神的功能[1]。中医认为本品性平,微苦而不燥,补益脾肺之效甚佳,尤善益气救脱,为治元气虚脱之要药。现代临床用其治疗各种原因引起的休克、心力衰竭、急性脑血管病等疾病效果显著。
在中医药长期医疗实践中,道地药材一直是评价药材品质的独特的综合性标准。中药材的道地产地的优选,可以为中药材的质量评价及道地药材的科学开发提供理论依据。据相关论著报道[2-5],中国人参主要产区分布在长白山地(包括张广才岭、老爷岭、木棱窝集岭、完达山)、小兴安岭的东南部,南起辽宁宽甸,北至黑龙江伊春,即北纬40~48°,东经117~137°的区域内森林地带,海拔 500~1 000m;年积温1 900~2 800℃,年平均气温4℃以上,1月平均气温-28~-24℃,7~8月平均气温20~24℃,年降雨量800~1 000mm(7~8月降水量400mm),无霜期为120~140d,年平均湿度70%~80%;年日照2 387h;森林覆盖率为76.4%,植被为针叶混交林;土壤类型为暗棕壤,pH值为5.5~6.5左右,山地选择坡度为15°以内,坡向以东、南、北3个坡向为宜[6]。而在上述产地及生态环境中生长的人参药材品质也存在着一定的差异。
本文对采自东北地区22个不同产地的38个人参样品进行总皂苷的含量测定,同时应用系统聚类分析法对所有样品的人参总皂苷含量进行数理统计分析,以研究东北地区人参的最佳产地及生态环境。
1 仪器和试药
Varian Cary 50型紫外可见分光光度计,大孔吸附树脂柱(内径1.5cm,长25cm),Satorius BP211D 1/10万电子分析天平。
人参皂苷Re对照品(中国药品生物制品检定所),D101型大孔吸附树脂,香荚兰醛(香草醛)、冰醋酸、高氯酸、三氯甲烷、正丁醇和甲醇等其他试剂均为分析纯。
2 方法与结果
2.1 供试品溶液的制备
取药材粉末(过三号筛)约1g,精密称定,置具塞锥形瓶中,精密加入水饱和的正丁醇50mL,称定重量,置水浴中加热回流提取1.5h,放冷,再称定重量,用水饱和正丁醇补足减失的重量,摇匀,滤过[1]。精密量取续滤液25mL,置蒸发皿中,蒸干,残渣加水10mL,微热使溶解,放冷,上已处理好的D101大孔吸附树脂柱(树脂高度为12cm),以水50mL洗脱,弃去水液,再用70%乙醇50mL洗脱,收集洗脱液,蒸干,用甲醇溶解并转移至5mL量瓶中,加甲醇至刻度,摇匀,即得。
2.2 对照品溶液的制备
精密称取经五氧化二磷干燥至恒重的人参皂苷Re对照品10.425mg,加甲醇溶解定容至5mL,制成1mL含人参皂苷Re2.085mg的溶液。
2.3 测定波长的选择
精密吸取对照品溶液20μL和样品编号4的供试品溶液30μL,分别加入干燥的具塞试管中,水浴挥干溶剂,加入新鲜配制的5%香草醛-冰醋酸溶液0.2mL,高氯酸0.8mL,于60℃恒温水浴中加热15min,取出,流水冷却2min,加冰醋酸5mL,摇匀,随行试剂为空白,于Varian Cary 50型紫外可见分光光度计上,在400~700nm波长范围内进行扫描[7]。结果供试品溶液与对照品溶液均在553nm波长处有最大吸收,故确定测定波长为553nm。
2.4 标准曲线的制备及线性关系考察
精密吸取对照品溶液20,40,60,80,100μL,分别加入5支干燥具塞试管中,水浴挥干溶剂,各加入新鲜配制的5%香草醛-冰醋酸溶液0.2mL、高氯酸0.8mL,于60℃恒温水浴中加热15min,取出,流水冷却2min,加冰醋酸5mL,摇匀,随行试剂空白,按照分光光度法试验,在553nm波长处测定吸收度。以吸收度为纵坐标,人参皂苷Re含量为横坐标,绘制标准曲线。得线性方程为Y=37.715X-0.027,r=0.999 1。人参皂苷 Re在 41.70~208.50μg线性关系良好。
2.5 精密度试验
精密吸取对照品溶液25μL,5份,按 “2.4”项方法操作并测定吸光度,结果吸光度的RSD=0.23%(n=5),仪器精密度良好。
2.6 样品溶液稳定性试验
取样品编号4药材粉末(过三号筛)约1g,按“2.1”项方法制备样品溶液。取编号4样品溶液,放置,分别在 0,1,2,3,4h取样 25μL,按“2.4”项方法操作并测定吸光度,计算样品含量。结果吸光度的RSD=2.05%(n=5),样品溶液4h内显色稳定。
2.7 样品溶液显色后溶液稳定性试验
取样品编号4药材粉末(过三号筛)约1g,按“2.1”项方法制备样品溶液。取编号4样品溶液25μL,按 “2.4”项方法操作,放置,分别在0,1,2,3h后测定吸光度,计算样品含量。结果吸光度的RSD=1.78%(n=4),样品溶液显色3h内稳定。
2.8 重现性试验
取样品编号4药材粉末(过三号筛)6份,每份约1g,按 “2.1”、 “2.4”项方法制备并测定吸光度,计算样品含量,结果RSD=1.24%(n=6),样品重现性良好。
2.9 加样回收率试验
精密称取已知含量的样品编号4人参粉末(过三号筛)1g,5份,加入人参皂苷Re对照品适量,按“2.1”、“2.4”项方法制备并测定吸光度,计算样品含量及回收率,结果见表1。
2.10 样品含量测定
取药材粉末(过三号筛)约 1g,按 “2.1”、“2.4”项方法制备并测定吸光度,计算样品含量,结果见表2。
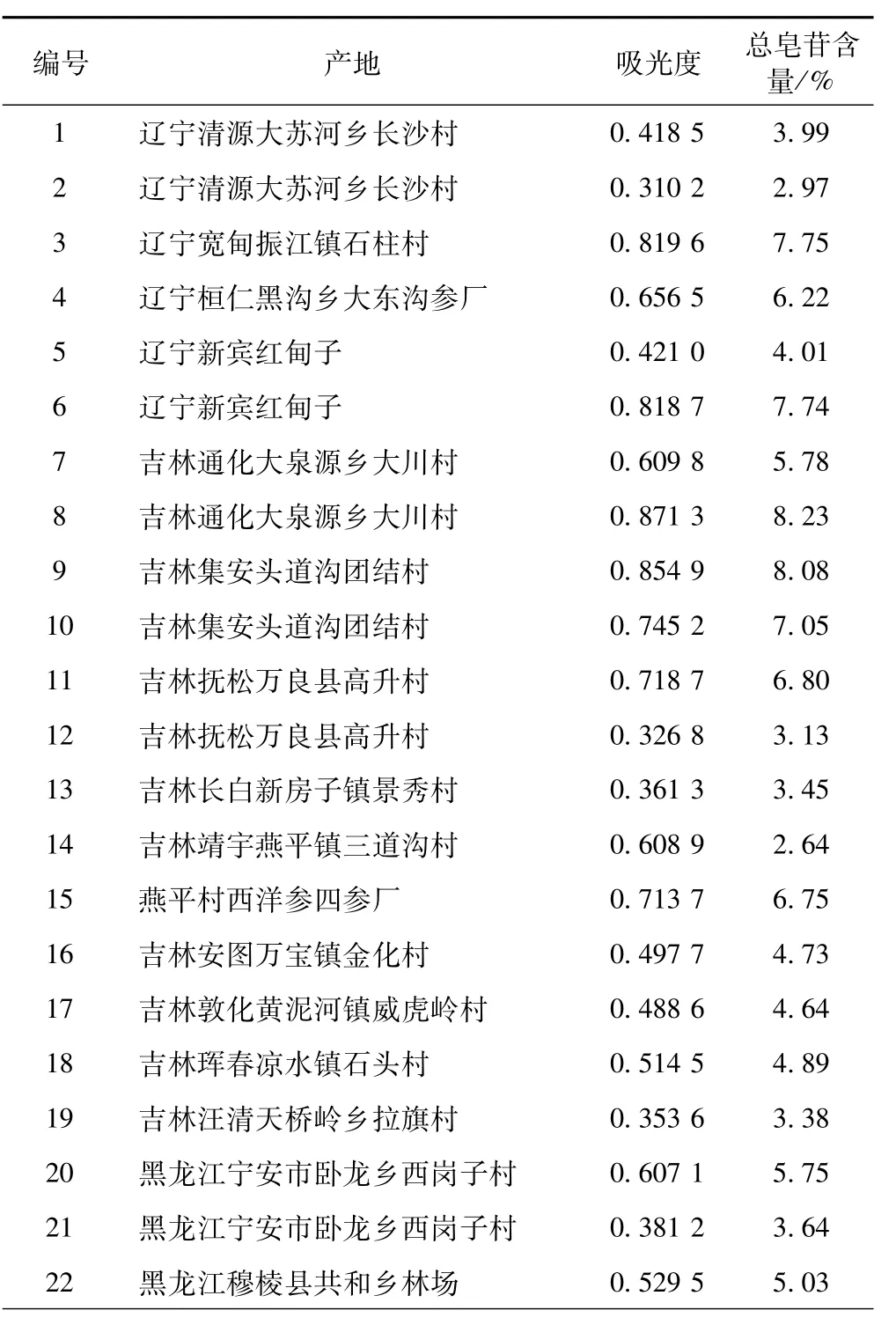
表2 样品中人参总皂苷的含量测定
2.11 人参总皂苷聚类分析
应用 SPSS(Statistical Package for the Social Science)统计分析软件中的系统聚类法(Hirearchical Cluster),以38个不同产地的人参样品的总皂苷含量数据为特征变量进行聚类分析。结果表明长白山脉南部、中部、北部各自聚为一大类,长白山北部和南部山脉附近聚为一类,聚类分析树形图见图1。
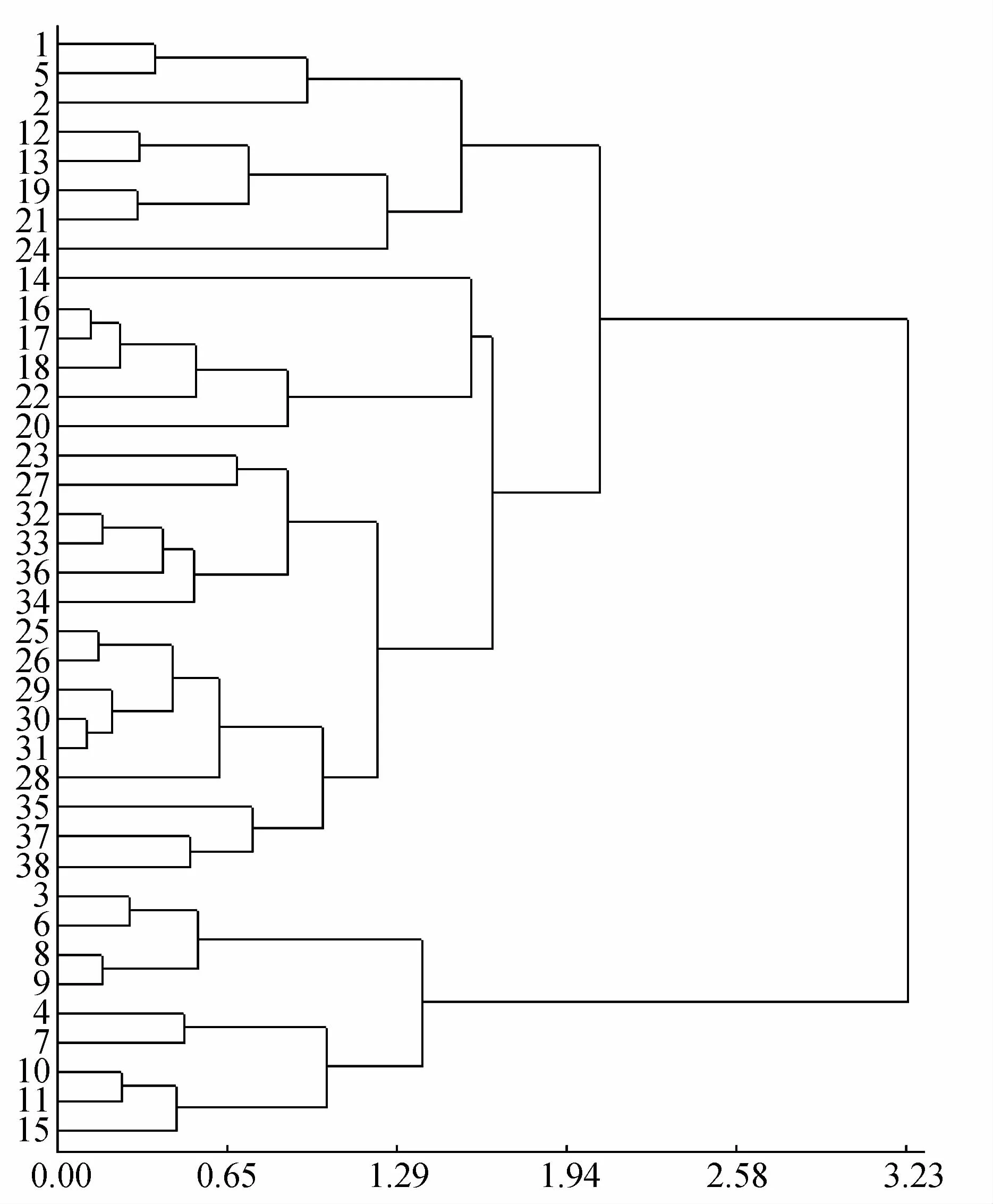
图1 不同产地人参样品系统聚类分析图
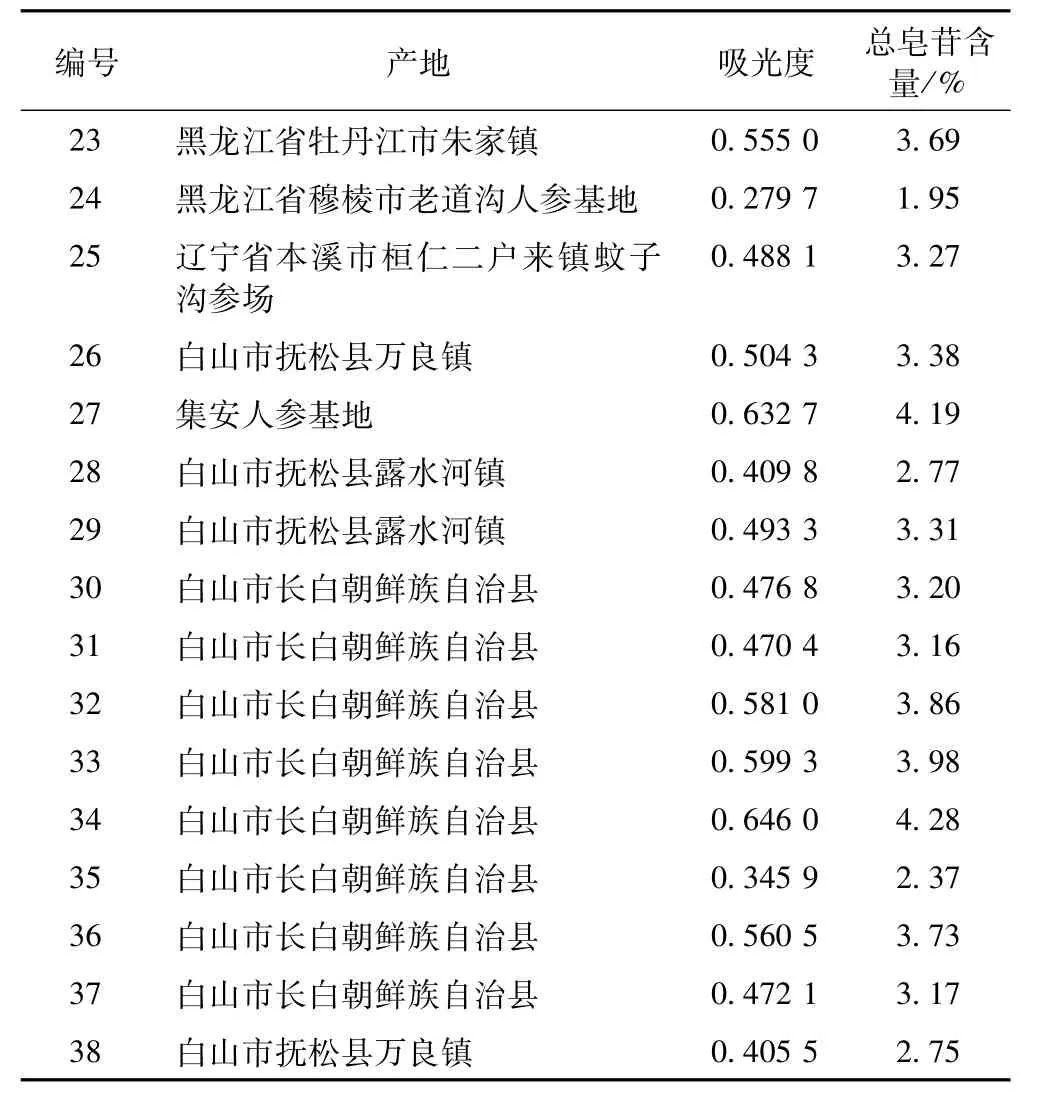
续表2
3 讨论
采用大孔吸附树脂分离纯化人参有效部位——人参总皂苷[8],然后用比色法测定人参总皂苷,可以消除杂质干扰。该方法精密度高,重现性、稳定性均较好,平均回收率为100.96%,可以用于人参药材质量控制。
该项目研究过程中,2010年版 《中国药典》尚未出版,2005年版 《中国药典》未收载人参总皂苷的含量测定方法,故采用 《卫生部药品标准》——中药成方制剂(第18册)中人参总皂苷的含量测定方法进行测定。
中药的质量评价一直是中药基础研究与应用的重点和难点问题,只有对中药材进行科学的质量控制,才能更好地保证中药饮片及其相关制剂的质量,实现中药的安全、有效、稳定、可控,为中药走向世界奠定良好的基础。
在人参有效物质基础明确的前提下,我们科学地以人参总皂苷的含量为考察指标,对38个产地的人参样品进行了化学模式识别研究,系统聚类分析了人参药材的产地,明确了人参道地药材的最佳产地,所得结论更为客观、科学、合理。
利用SPSS软件分析不同产地人参样品的总皂苷含量差异可见,在长白山南部,即南起辽宁宽甸,北至吉林靖宇,包括辽宁宽甸、恒仁、新宾,吉林集安、通化、抚松、靖宇等地的人参总皂苷含量明显高于中北部,应该作为东北地区人参药材的最佳产地,见图2。

图2 东北地区人参药材聚类分析产地总皂苷含量差异分布图
依据肖培根绘制的东北野生人参分布图,该地区的最佳生态环境约为:北纬40~42°,东经125~127°的区域内森林地带(见图3),海拔 500~1 000m;≥10℃年积温2 500℃,年平均气温4℃以上,1月平均气温 -18℃,7~8月平均气温20~21℃,年降雨量800~1 000mm(7~8月降水量400mm),无霜期为100d,土壤类型为暗棕壤,pH值为5.5左右[6],余基本与论著报道相同。
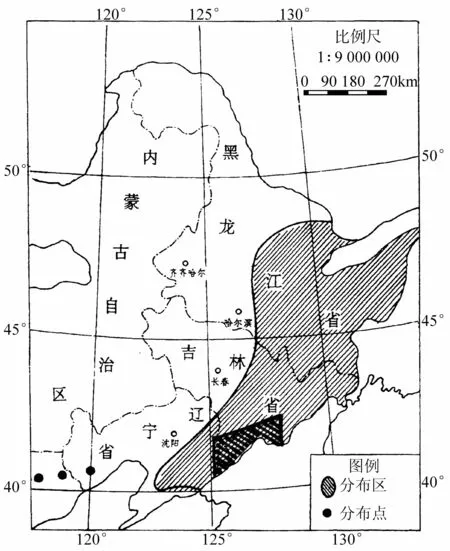
图3 东北野生人参分布图
人参质量的优劣主要受产地及生态环境的影响,但相同产地的人参质量也存在较大差异,这与人参的采收季节、采集年限、加工方法、保存方法等影响因素密切相关,至于人参总皂苷含量与这些条件之间的关系还有待进一步研究确定,若今后能够结合其主要药理活性指标,则其质量模式识别研究将更加科学而全面。
[1]国家药典委员会.中国药典(一部)[S].北京:化学工业出版社,2005:7-8.
[2]宋炳海.中国气候[M].北京:科学出版社,1962.
[3]杨美华.长白山地理系统论文集[M].1981.
[4]竺可桢.中国自然地理(气候)[M].北京:科学出版社,1984.
[5]盛承禹.中国气候总论[M].北京:北京出版社,1986.
[6]王铁生.中国人参[M].沈阳:辽宁科学技术出版社,2001:12.
[7]卫生部.药品标准·中药成方制剂(第18册)[S].1998:167-168.
[8]蔡雄,刘中秋,王培训,等.大孔吸附树脂富集纯化人参皂苷工艺[J].中成药,2001,23(9):631-634.
Research on Optimal Producing Areas and Ecological Environment of Panax Ginseng by Cluster Analysis
Zhou Haiou1,Li Xiuchang2,Chen Xiangtao2,Li Chunnan2,Sun Jiaming2,Zhang Hui2
(1.Jilin Academy of Sciences of Traditional Chinesemedicine,Changchun Jilin 130012,China;2.Development Center of Traditional Chinese Medicine and Bioengineering,Changchun University of Chinese Medicine,Changchun Jilin 130117,China)
Objective:To investigate the optimal producing areas and ecological environment of panax ginseng by determining the contents of total ginsenosides of thirty-eight samples collected from twenty-two different regions in northeastof China.M ethods:Colorimetry was used to determine the contents of total ginsenosides and SPSS software system was used to perform data and cluster analyses.ResultsThe south of Changbai Mountains is the optimal producing areas.The forest area in northeast of China is the best ecological environment,which have characteristics:latitude 40~42℃,longitude 125~127℃ area,elevation 500~1 000m,annual average temperature of 4℃ above,etc.ConclusionThe method is simple,accurate,feasible and can provide a basis for the quality evaluation of panax ginseng and the scientific developing of Geo-authentic crude drug.
Panax ginseng;Ginsenosides;Colorimetry;Cluster analysis
*张辉,Tel:(0431)86172080,E-mail:zhanghui_8080@163.com
2010-01-14)

