香果健消片质控方法研究I:蜘蛛香主要成分的鉴别和含量测定
肖雨婷,赵明芬,彭 芳,肖培云
(大理学院药学院,云南大理 671000)
香果健消片质控方法研究I:蜘蛛香主要成分的鉴别和含量测定
肖雨婷,赵明芬,彭 芳,肖培云*
(大理学院药学院,云南大理 671000)
目的:建立香果健消片中橙皮苷的鉴别和含量测定方法。方法:采用薄层色谱法对橙皮苷进行鉴别;采用高效液相色谱法(HPLC)测定橙皮苷的含量,以Agilent XBP-C18(4.6mm×250mm,5μm)为分析柱,流动相为甲醇-5%冰醋酸(35∶65),检测波长283nm。结果:薄层鉴别结果显示,橙皮苷在相应的色谱条件下分离效果良好;HPLC结果显示,橙皮苷在0.202~4.040μg之间线性关系良好(r=0.999 9),平均回收率为100.3%(n=6),RSD为1.28%。结论:此方法简便、稳定,重现性好,可用于本品中橙皮苷的鉴别和含量测定。
香果健消片;蜘蛛香;橙皮苷
香果健消片是由蜘蛛香、木香、草果等药材经提取制成的中药制剂,具有健胃消食之功效,用于消化不良、气胀饱闷、食积腹痛、胸满腹胀。现行质量标准收载于《卫生部药品标准》中药成方制剂〔1〕,该质量标准中,只用香草醛进行显色鉴别,无专属性较强的薄层色谱鉴别和含量测定方法。为了保证本品的用药安全,更好地控制药品质量,本实验对方中主药蜘蛛香进行薄层色谱法(TLC)鉴别,并采用高效液相色谱法(HPLC)测定其主要化学成分橙皮苷的含量〔2〕。
1 仪器与材料
1.1 仪器 Agilent1200高效液相色谱仪(包括G1311A四元泵、G1314B可变波长、G1316A柱温箱、G1329A自动控温进样器、G1322A真空脱气机);AgilentXBP-C18(4.6×250mm,5μm)分析柱;电子分析天平(瑞士梅特勒AL204-IC);薄层色谱成像仪(武汉药科新技术开发有限公司YOKO-ZS);超纯水机(台湾艾柯纯水设备厂KL-UP-UV-20);超声波清洗器(宁波新芝生物科技股份有限公司SB5200DT)。
1.2 材料 香果健消片(云南云河药业有限公司生产,批号:090603,090706,090802,081201);橙皮苷对照品(批号:110721-200613,中国药品生物制品鉴定所提供);硅胶G(青岛海洋化工有限公司生产);甲醇为色谱纯(美国Fisher公司);水为超纯水;其它试剂均为分析纯。
2 鉴别
2.1 橙皮苷对照品溶液的制备 精密称取橙皮苷对照品5.050mg,置10mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成0.505mg/mL的对照品贮备液〔3〕。精密移出上述溶液400μL,用甲醇稀释至1.0mL,即得对照品溶液(含橙皮苷0.202mg/mL)。
2.2 供试品溶液的制备 称取不同批号(090603、090706、081201)各10片,去糖衣,精密称定,研细,各取约1.0g,精密称定,加入20mL甲醇,称定重量,25℃超声提取30min,放冷,滤过,滤液置水浴上挥干,残渣各加入2.0mL甲醇,溶解,即得供试品溶液〔3〕1,2,3(批号分别为090603、090706、081201)。
2.3 蜘蛛香对照药材溶液的制备 按处方制备蜘蛛香对照药材,再按“2.2”项制备,即得蜘蛛香对照药材溶液。
2.4 阴性对照品溶液的制备 按处方制备缺蜘蛛香的阴性对照品,再按“2.2”项制备,即得阴性对照品溶液。
2.5 薄层色谱条件及结果 参照TLC试验〔4〕,用毛细吸管吸取上述供试品、对照品、对照药材、阴性对照溶液,分别点于同一硅胶G薄层板上,以乙酸乙酯-甲醇-水(100∶17∶15)的上层溶液为展开剂,进行一次展开,展至约6cm,取出,晾干。再以甲苯-乙酸乙酯-甲酸-水(20∶10∶1∶3)为展开剂,进行二次展开,展开至16cm,取出,晾干,喷以3%AlCl3溶液,在110℃下加热至斑点显色清晰,置紫外光灯(365nm)下检视〔5〕。供试品色谱中,在与对照品、对照药材色谱相应的位置上,分别显相同颜色的荧光斑点,阴性对照无相应的荧光斑点。见图1。
3 含量测定
3.1 系统适用性试验 色谱柱:Agilent XBP-C18分析柱(4.6×250mm,5μm);流动相:甲醇-5%冰醋酸溶液(35∶65);检测波长283nm;柱温35℃;流速1.0mL/min。理论塔板数按橙皮苷峰计算应不低于2 500〔5〕。
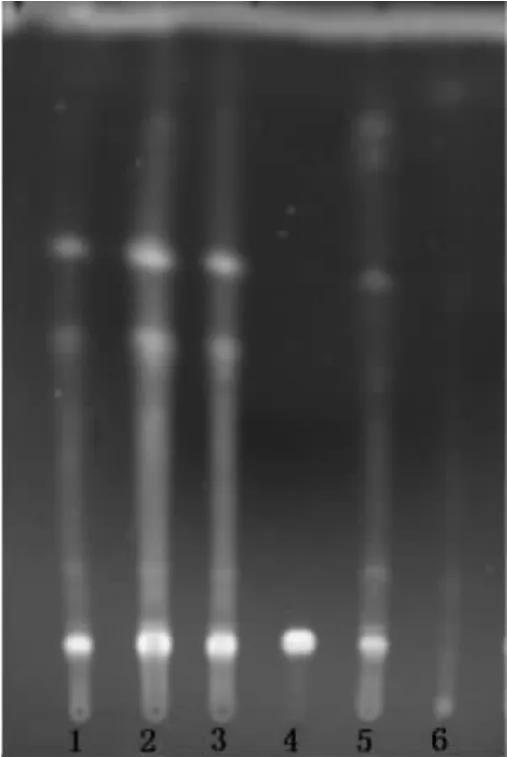
图1 蜘蛛香的TLC图谱
3.2 供试品溶液的制备 取本品20片,去糖衣,精密称定,研细,取约0.5g粉末,精密称定,加入20mL甲醇,称定重量,25℃下超声提取30min,放冷后,补重,摇匀,用微孔滤膜滤过,取续滤液,即得。
3.3 阴性对照品溶液的制备 取缺蜘蛛香的阴性对照样品0.5g,按“3.2”项供试品溶液的制备方法制备,即得。
3.4 专属性试验 精密吸取对照品溶液、供试品溶液和阴性对照溶液各5μL,分别注入液相色谱仪,结果供试品色谱中呈现与对照品保留时间相同的色谱峰,阴性对照品在橙皮苷对照品相同保留时间处未显色谱峰,故认为无干扰。见图2。
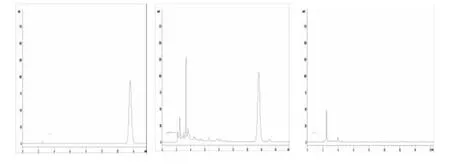
图2 HPLC色谱图
3.5 标准曲线的制作 按“3.1”项色谱条件,取0.202mg/mL的对照品溶液,分别以1,2,5,8,15,20μL进样测定,以橙皮苷的峰面积峰值为纵坐标,进样量为横坐标,绘制标准曲线,得回归方程为:y=2 036.6X+10.554(r=0.999 9)。结果表明,橙皮苷在0.202~4.040μg范围内与峰面积呈良好的线性关系。
3.6 精密度试验 按“3.1”项色谱条件,取0.202mg/mL的对照品溶液连续6次进样,峰面积的RSD为0.83%。结果表明,仪器精密度良好。
3.7 稳定性试验 按“3.1”项色谱条件,按“3.2”项制备供试品溶液,在0,2,4,6,8,10,12h各进样1次,测定供试品溶液中橙皮苷峰面积值,所得橙皮苷的峰面积RSD为2.75%。结果表明:供试品溶液中橙皮苷12h内稳定。
3.8 重现性试验 取同一批号(090603)样品6份,按“3.2”项制备各供试品溶液,并按“3.1”项色谱条件进行测定,橙皮苷的含量为0.85mg/片,RSD为2.43%。
3.9 加样回收率试验 取已知含量的同一批号(090603)样品6份,每份约0.45g,精密称定,各加入橙皮苷贮备溶液(0.505mg/mL)1mL,按“3.2”项供试品溶液制备方法制备,按“3.1”项色谱条件测定,计算回收率。见表1。
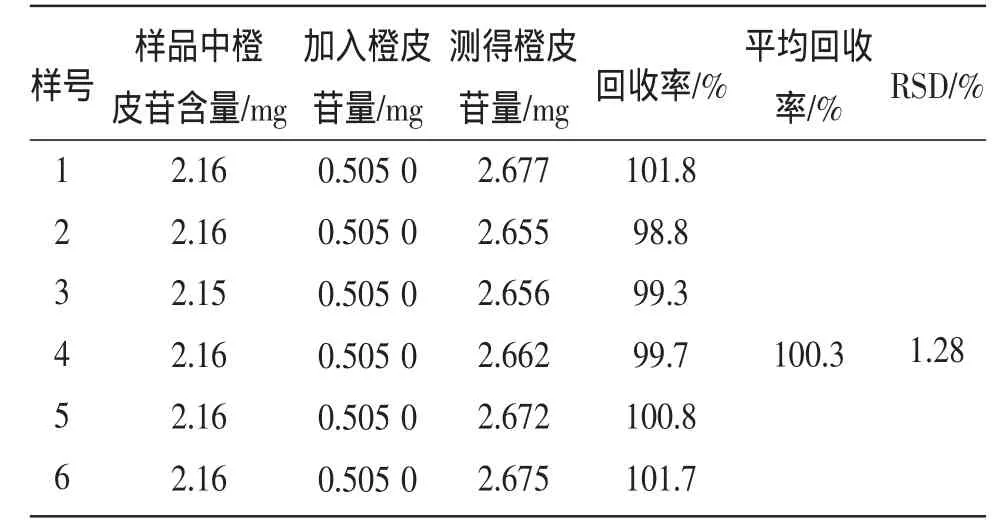
表1 回收率测定结果
3.10 样品含量测定 取4个不同批号的药品,按“3.2”项供试品溶液制备方法制备,按“3.1”项色谱条件测定,计算。结果见表2。
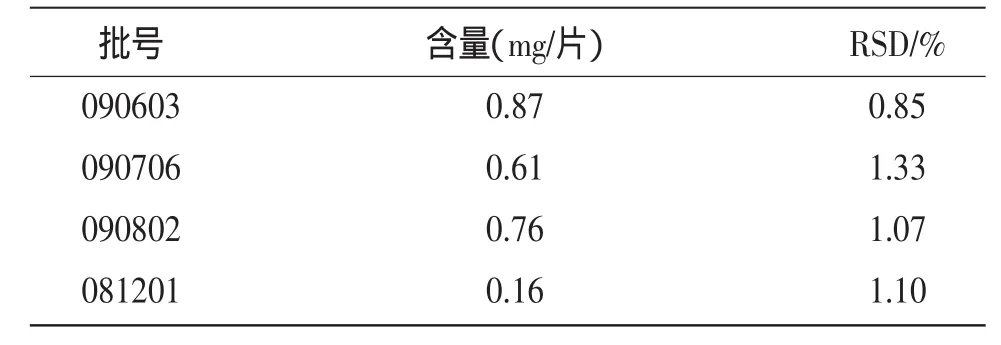
表2 含量测定结果
4 讨论
橙皮苷在甲醇中易溶解,故在薄层色谱鉴别、HPLC测定橙皮苷时选用甲醇作溶剂〔6〕。
原质量标准中“鉴别”属化学鉴别,由于其专属性不强,故本实验采用TLC对香果健消片中蜘蛛香主要化学成分橙皮苷进行了薄层鉴别。对薄层条件进行优化:考察了不同比例的展开剂(乙酸乙酯-甲醇-水、甲苯-乙酸乙酯-甲酸-水)系统,结果采用乙酸乙酯-甲醇-水(100∶17∶15)、甲苯-乙酸乙酯-甲酸-水(20∶10∶1∶3)为展开剂。供试品色谱中,在与对照品相应的位置上显相同颜色的荧光斑点,有5个斑点与对照药材相对应,阴性对照无相应的荧光斑点。试验结果表明阴性对照溶液对供试品均无干扰,专属性强、斑点清晰,特征斑点分离效果良好,斑点无拖尾现象,故此方法可用作香果健消片中橙皮苷的鉴别。
对制剂中橙皮苷进行含量测定研究,为了在短时间内获得好的分离效果,对色谱条件进行了优化:首先,考察了不同组成和比例的流动相〔5,7-8〕(乙腈-水、甲醇-水)系统,酸主要比较了冰醋酸和磷酸。结果乙腈-水系统分离效果不如甲醇-水系统,且在甲醇-水系统中加入5%的冰醋酸可提高分离效果。综合考虑各因素后确定采用甲醇-5%冰醋酸溶液(35∶65)为流动相进行洗脱。其次,考察了不同的波长〔5,9〕(280、283nm)、不同的柱温(25、30、35℃),最后确定波长为283nm、柱温为35℃。在上述条件下,能够在15min之内测定橙皮苷峰,且橙皮苷峰达到基线分离。此方法简便、快速、可靠,适用于香果健消片中橙皮苷的含量测定。
〔1〕国家药典委员会.中华人民共和国卫生部药品标准〔M〕.北京:人民卫生出版社,1990:120.
〔2〕陈发奎.常用中草药有效成分含量测定〔M〕.北京:人民卫生出版社,1999:188-198.
〔3〕吴子富,李晶,文萍,等.龙甘胃舒分散片的质量控制〔J〕.中国医院药学杂志,2009,29(11):878-881.
〔4〕国家药典委员会.中华人民共和国药典〔M〕.北京:化学工业出版社,2005:附录31.
〔5〕池浩波,张雪原,林晓辉,等.宝儿康散质量标准修订研究〔J〕.中国药品标准,2008,9(5):334-338.
〔6〕何继祥,许庆,朱正华,等.蜘蛛香野生变家种可行性研究〔J〕.云南中医中药杂志,2008,29(10):29-30.
〔7〕石晋丽,刘勇,肖培根.HPLC法测定不同产地蜘蛛香中橙皮苷的含量〔J〕.中草药,2005,36(3):449-450.
〔8〕狄宏晔,石晋丽,闫兴丽,等.蜘蛛香药材质量标准研究〔J〕.中国中药杂志,2007,32(22):2357-2359.
〔9〕程静,解翠珠,何继祥.野生蜘蛛香与家种蜘蛛香中橙皮苷含量对比〔J〕.中国现代药物应用,2008,2(22):62.
(责任编辑 蒋 康)
Research of the Quality ControlMethod of the Xiangguojianxiao TabletsⅠ:Indentification and Determ ination of the Major Components of Valeriana Jatamansi Jones
XIAO Yuting,ZHAOMingfen,PENG Fang,XIAO Peiyun*
(C ollege of Pharmacy,DaliUniversity,Dali,Yunnan 671000,China)
Objective:To establish a method for the identification and determination of hesperidin in Xiangguojianxiao tablets.MethodsHesperidin in Xiangguojianxiao tablets was identified by TLC,and the contentswas determined by HPLC.Agilent XBPC18(4.6mm×250mm,5μm)was used as analytical column.The ana-lyticalmobile phase was composed ofmethanol-5%and glacial acetic acid(35:65 V/V).The determination wave-length was 283 nm.Results:Hesperidin in Xiangguojianxiao tabletswas separated very well under the corresponding chromatographic condition.The calibration curve of hesperidin was linear in the range of 0.202~4.040μg (r=0.999 9);recovery rate was 100.3% (n=6),and RSD was 1.28%.ConclusionThis method is simple,stable and reproducible,and can be used for identification and determination of hesperidin in Xiangguojianxiao tablets.
Xiangguojianxiao tablets;valeriana jatamansi jones;hesperidin
R975+.1
A
1672-2345(2010)08-0009-03
大理学院大学生科研基金资助项目(2009DXSY01)
2010-06-12
肖雨婷,主要从事药学研究.
*通信作者:肖培云,副教授,电话:15808729786
