锆-氚反应热力学特性
黄 刚龙兴贵 彭述明 梁建华 杨本福
(中国工程物理研究院核物理与化学研究所,绵阳 621900)
锆-氚反应热力学特性
黄 刚*龙兴贵 彭述明 梁建华 杨本福
(中国工程物理研究院核物理与化学研究所,绵阳 621900)
锆;氚;p-c-T曲线;热力学参数
利用金属氢化物可以方便地对氢同位素氕、氘、氚进行泵输、转移、固态吸附贮存、功能薄膜制造等。目前应用较成熟的有铀[1]、钛[2]、锆钴合金[3]等材料。锆与钛是属于同一族的金属元素,也是一种吸氢密度很高的功能材料,目前国内外已有较多关于氢在锆中固溶[4]、扩散[5-6]等方面的报道,但有关锆吸氚性能方面的报道较少。为了将锆应用于贮存氘和氚,有必要研究锆与氘和氚作用的各种物理化学特性。在锆-氘反应性能研究[7]的基础上,本工作进行了锆吸、放氚的实验,对其热力学特性进行了研究。
1 实验部分
1.1 实验装置
实验装置为无油高真空金属测试系统[7]。该系统由真空系统 (系统的极限真空为10-6Pa)、加热系统(电阻丝电炉和控温装置(控温精度为±1℃))、气体引入系统 (1只贮氘铀床、1只贮氚铀床和1只回收废氚用铀床)和测量系统(电离真空计(量程为10-8~10-1Pa)、薄膜压力测量仪(量程为 0~133 kPa))等组成。
1.2 实验方法
1.2.1 试样准备
(1)将纯度为99.99%的锆经机加工成 Φ 10 mm×1 mm的小圆片,质量约为400 mg。未经处理的锆样品表面呈现暗灰色。实验用氚纯度为98%,贮存于金属铀床中。
(2)将样品放入氢氧化钠溶液中煮沸约15 min,边煮边搅拌以防止暴沸。该流程重复2次以保证表面油污清洗完全,清洗完毕后用自来水冲洗,再放入氢氟酸稀溶液中反应,以除去表面的氧化层,可以看到,样品表面很快变成黑色,这时需要往溶液中滴入少量的硝酸和硫酸溶液,样品表面的黑色覆层才能被反应溶解,样品表面逐渐变成明亮的银白色。反应完全的样品用蒸馏水清洗干净,晾干后放入真空室贮存待用。
(3)将锆样品装入系统的样品室中,进行系统抽真空。分步启动机械泵、分子泵抽真空,当真空度达到5 mPa后加热升温,电炉加热电压为30 V,升温温度设定为700℃。当样品温度升至700℃后,将温度保持在在此温度约1 h,待系统的真空度达到1 mPa后停止加热,将样品冷却至室温。
(4)样品除气后,加热氚化铀床放出一定量氚气,加热样品使之升温吸气;吸收一定量氚气后,将样品加热到700℃以上,使氚解吸,用铀床回收解吸的气体。如此反复数次,使锆样品在室温即能快速吸气即可。
1.2.2 吸氚压力-组成等温线(p-c-T 曲线)测定
将样品恒温在某个预定温度,采用分步吸气平衡法[7]放出一定量氚气让锆吸收,记录相应的压力数据,由公式(1)计算每次氚的增量:

式中:ΔnT/nZr为吸气增量与锆金属的原子比;M为锆的相对原子质量;m为样品的质量,g;R为气体常数,8.314 J·mol-1·K-1;p1,p,p3为管道初始压力、样品室初始压力和反应平衡压力,Pa;V1为管道体积,554 mL;V2为样品室体积,219 mL;T1为管道温度,为室温,K;T2为样品室温度,K。
将第i次计算所得值ΔnT/nZri与前几次计算值累加,并与对应的平衡压力p3在p-c-T曲线上可作得第i个点,将所有的点连接起来,即可得锆在某一温度的p-c-T曲线。
1.2.3 锆解吸氚p-c-T曲线测定
将接近饱和的样品温度恒定,记录吸氚平衡压力。关闭样品室阀门,用铀床回收管道里的气体后抽真空,然后再打开样品室阀门,让锆解吸氚,记录平衡压力,计算锆氚原子比。如此循环,即可测得锆解吸氚p-c-T曲线。
2 结果与讨论
2.1 活化性能
从图1的曲线可以看出,锆在第1次吸气活化时,直到540℃才开始缓慢吸气,到650℃时才出现明显的吸气过程;第2次活化时,虽然在460℃时就出现缓慢吸气过程,但也是在600℃左右才出现明显吸气;第3次活化时,吸气温度明显降低,350℃开始吸气,速度也明显比前两次加快;到第4次活化时,270℃已能快速吸气。可见,锆金属较易活化,吸气时速度也很快。

2.2 锆吸氚的p-c-T曲线
锆吸氚的p-c-T曲线结果示于图2。由图2可知:锆在低于500℃的温度范围内,其吸氚p-c-T曲线只存在一个平台,且平衡压较低。由氢锆体系相图[8]可知,在450~500℃的温度区间,氢化锆在氢浓度较低范围内时为六方密堆积(hcp结构)的α金属相区,随着氢浓度增加,α相逐渐转变为δ相,当氢锆原子比达到1.5左右以后完全形成面心立方的单一δ相,图2中450~500℃的p-c-T曲线仅有的一个平台就对应于锆氚化物的α+δ双相区。
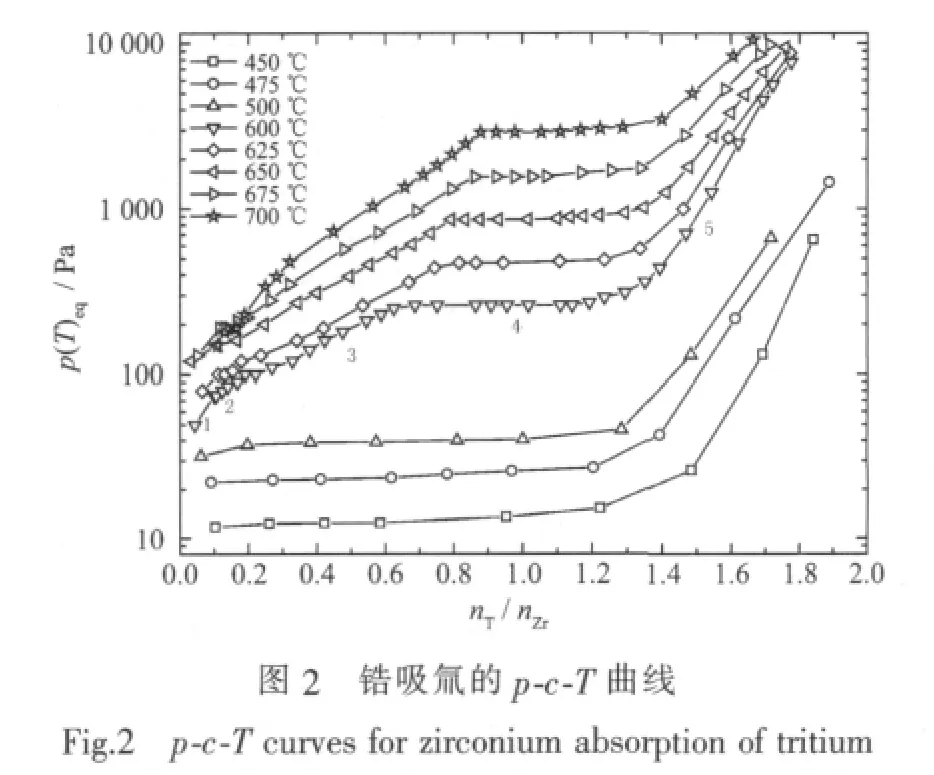
在图2中600~700℃的高温区域,锆的吸氚曲线出现了2个平台,把曲线粗略分成了5个区域,如图2中数字所示,表明在此温度范围内,锆氢相平衡变得较复杂,随着氢浓度的增加,锆由最初的α相转变为β相,β相又逐渐转变为δ相,在这个相变过程中,锆氢化物物相共存在五种不同的组合形式,分别是α 相、α+β 相、β相、β+δ相和 δ相,图 2 中的5个区域,分别对应于上述5个相区,其中平台区是相转变过程中的双相共存区。从图可以看出,600~700℃时锆吸氚p-c-T曲线的第一平台的坪区很窄,从氚锆原子比约0.1开始,仅有约0.1原子比的宽度,且平台有一定的斜率,表明锆在吸收少量的氚达到临界值之后,锆晶格原子发生重排,从hcp结构的α相快速转变为bcc结构的β相。曲线的第二平台较为平坦,且随着温度的升高向高原子比方向移动,但其坪区宽度基本不变。
2.3 锆吸氚容量
由图2中锆在475℃吸氚的p-c-T曲线可知,氚化锆在原子比接近1.3的时候其平台区基本结束,相结构转化为单一的δ相,锆吸氚平衡压开始快速上升,锆的吸氚容量达到了1.89,加上用氚活化时锆本身对氚的滞留量,其吸氚总量非常接近于锆吸氢的理论值2.0,所以,锆对氚的容留能力与钛相似,且在相同温度下其平衡压力比钛更低,很适合用作贮氚材料。
2.4 吸氚平衡压与温度的关系
在平台区,锆吸氚的吸气平衡压与温度的关系示于图3。图3所示结果表明:在平台区,lnp与1/T呈良好的线性关系,对图中实验点进行线性拟合就可根据范德荷夫方程计算锆吸氚在不同物相时的热力学参数ΔH⊖、ΔS⊖,结果列于表1。由表1可知,锆吸氚在形成不同的相组成时有不同的标准焓变和标准熵变。


表1 锆吸氚氚化反应的热力学参数Table 1 Thermodynamic parameters of zirconium tritide
锆氢平衡相图显示,在温度低于500℃的区域范围内,氚化锆基本上都处于α+δ双相区,升降温过程不会引起物相结构和热力学性能的变化,所以,由范德荷夫方程和表1中低温平台的热力学参数计算得到锆在20℃的吸氚平衡压力约为1.0×10-10Pa,由此可见,锆在吸收氚气冷却至室温以后,其平衡压非常低,很适合用作特种真空器件的氚贮存材料。
2.5 锆解吸氚p-c-T曲线与滞后效应
锆在675和700℃解吸氚的p-c-T曲线示于图4。为了便于比较,将其吸气曲线也一并放在其中。由图4可以看出:锆解吸氚的p-c-T曲线与吸气pc-T曲线的趋势基本一致,也有相应的平台,但在相同的T/Zr原子比时,解吸平衡压力比吸气平衡压力低,吸、放氚这一逆过程中存在明显的滞后效应,说明锆吸氚以后很稳定,不易释放出氚气来。

[1]Li R,Sun Y,Wei Y J,et al.Fusion Eng.Des.,2006,81:859-862
[2]Daigo S,Junji M,Hiroaki M,et al.J.Alloy Compd.,2004,381:215-220
[3]Masanori H,Toshio O,Katsunori M,et al.Fusion Eng.Des.,2000,49-50:831-838
[4]Shinsuke Y,Daigo S,Hiroaki M,et al.J.Alloys Compd.,2004,372:129-135
[5]Wipf H,Kappesser B,Werner R.J.Alloys Compd.,2000,310:190-195
[6]Pletnev R N,Kupryazhkin A Y,Dmitriev A V,et al.J.Struct.Chem.,2002,43(3):445-448
[7]HUANG Gang(黄 刚),LONG Xing-Gui(龙兴贵),YANG Ben-Fu(杨本福),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2008,24(12):2056-2059
[8]Thaddeus B,Hiroaki O,Subramanian P R,et al.Binary Alloy Phase Diagrams.2nd Ed.Ohio:ASM International,1992.
Thermodynamic Characteristics of Zirconium-Tritium Reaction
HUANG Gang*LONG Xing-GuiPENG Shu-Ming LIANG Jian-HuaYANG Ben-Fu
(Institute of Nuclear Physics and Chemistry,China Academy of Engineering Physics,Mianyang,Sichuan 621900)
The p-c-T curves and the relation between equilibrium pressure and temperature of tritium absorption and desorption from zirconium were measured in the temperature range of 450~700 ℃.There are different changes of enthalpy and entropy when zirconium changes to different phases.The change of enthalpy in the phase of α plus δ is-106.5 kJ·mol-1in the temperature range of 450~500 ℃,the changes of enthalpy in the first and second plateau are-85.9 and-170.2 kJ·mol-1,respectively,in the temperature range of 600~700 ℃.The corresponding changes of entropy are-72.6,-38.3 and-144.9 J·K-1·mol-1,respectively.There are obvious lagging effects when zirconium desorbs tritium.
zirconium;tritium;p-c-T curve;thermodynamic parameters
O614.41+2;O613.1;O642.1
A
1001-4861(2010)09-1707-04
2010-04-26。收修改稿日期:2010-06-23。
国家自然科学基金(No.50871106)资助项目。
*通讯联系人。E-mail:yunerfei80@yahoo.com.cn
黄 刚,男,30岁,硕士,助研;研究方向:氚化学与氚工艺。

