呋苄西林钠的有关物质测定及抗菌活性考察
张 菁,姜建国,高燕霞
(河北省药品检验所,河北 石家庄 050011)
呋苄西林钠为氨基青霉素的脲基衍生物,是广谱半合成青霉素,主要用于绿脓杆菌感染。目前,其原料药及制剂质量标准中含量测定方法为剩余酸碱滴定法[1],但操作烦琐,专属性差,影响因素多,而且一些无生物活性物质也参与反应,不能真实反映其抑菌活性。笔者采用高效液相色谱(HPLC)法[2]测定呋苄西林钠的有关物质,并对其抗菌活性进行研究,旨在为改进生产工艺和提高产品质量提供依据。
1 仪器与材料
Agilent 1100型色谱系统;CZB-1抗生素比浊法测定仪;玻璃培养杯(厚度 1 cm)。金黄色葡萄球菌[CMCC(B)26 003]由中国药品生物制品检定所提供;呋苄西林钠标准品(批号为070301,含量902 U/mg,本所标定);呋苄西林钠原料(批号分别为 060104,20060105,20070106,国内药厂提供);抗生素检定用培养基Ⅲ号(pH=7.9±0.1,中国药品生物制品检定所提供);灭菌生理盐水和磷酸盐缓冲液(pH=6.0)均按2005年版《中国药典(二部)》附录[3]配制;磷酸二氢钾、磷酸氢二钾、磷酸为国产分析纯;乙腈为色谱纯。
2 方法与结果
2.1 浊度法的建立与评价
菌液配制:取金黄色葡萄球菌新鲜斜面培养物,接种于营养琼脂斜面上,置35~37℃培养18~23 h,用灭菌生理盐水洗下菌苔,加生理盐水稀释,使之在580 nm波长处的吸光度约为1.0。取菌液2~3.3mL,加至培养基100 mL中,摇匀。
溶液配制:取呋苄西林钠标准品适量,精密称定,用适量水溶解并稀释成1 000 μg/mL的溶液,作为标准品贮备液;精密量取贮备液适量,用磷酸盐缓冲液(pH=6.0)稀释至试验质量浓度,作为标准品溶液。取呋苄西林钠,精密称取适量,用适量水溶解并稀释成1 000 μg/mL的溶液,作为供试品贮备液;精密量取贮备液适量,用磷酸盐缓冲液(pH=6.0)稀释至试验质量浓度,作为供试品溶液。
培养与测定:取标准品溶液1.0 mL,置灭菌培养管中,再加试验菌液9.0 mL,置抗生素比浊法测定仪内,于(37±1)℃下培养;另取稀释溶剂1.0 mL,加至9.0 mL空白培养基中,混匀,作为空白对照。于530 nm波长处测定各管金黄色葡萄球菌对数生长期内不同培养时间的吸光度值(A)。根据量反应平行线原理计算供试品的效价值。
试验菌、培养基选择:呋苄西林钠为广谱半合成青霉素,对大多数革兰阳性菌与部分革兰阴性菌有杀灭作用,因此选择金黄色葡萄球菌和大肠杆菌作为试验菌;在Ⅲ号液体培养基中培养,加菌量分别为1%,2%,3%;抗生素质量浓度为0.1~1.0 μg/mL。绘制菌株在不同加菌量及不同抗生素浓度的生长曲线。根据菌生长曲线及在不同抗生素浓度下菌液吸光度值的变化,发现金黄色葡萄球菌和大肠杆菌在Ⅲ号液体培养基中生长对不同质量浓度的抗生素敏感,抗生素的线性质量浓度范围宽。以大肠杆菌为试验菌时,各抗生素质量浓度不呈线性,故选择金黄色葡萄球菌作为试验菌。
测定时间选择:对不同加菌量(2% ~3%)及菌的不同传代次数进行比较,以不同抗生素质量浓度下的吸光度 A为纵坐标、培养时间 t为横坐标绘制菌生长曲线(图1)。可见,不同抗生素质量浓度下的金黄色葡萄球菌培养约2 h进入对数生长期;比较不同抗生素质量浓度下的菌液 A-t生长曲线发现,传代次数不同及加菌量不同的菌平稳生长时间均在4~6 h,因此选择测定时间4~6 h。比较4~6 h不同时间点的 A-lgC曲线(图2),发现菌液的吸光度值A在0.4~0.8时便于测定,据此可确定抗生素质量浓度的测定范围。
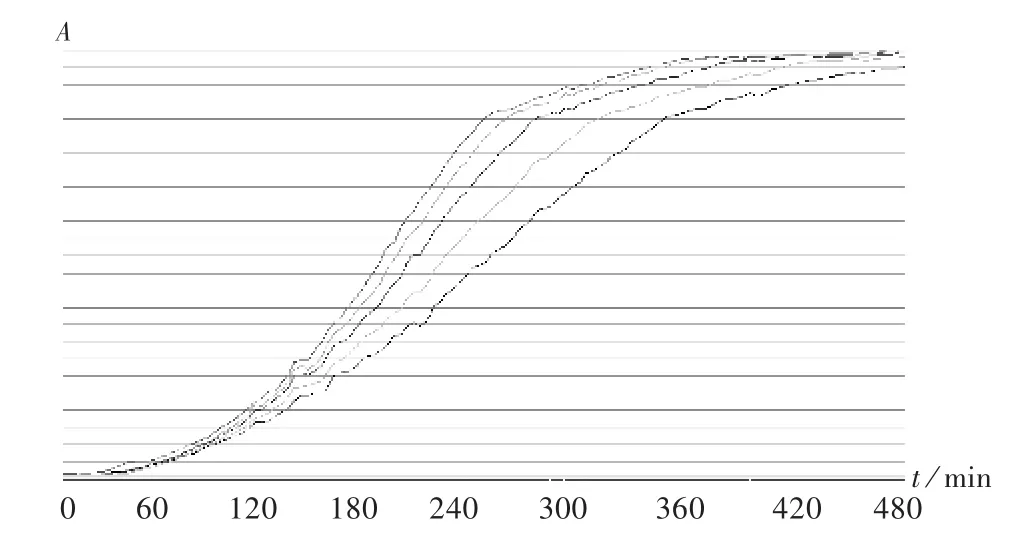
图1 不同抗生素质量浓度下1.5%的金黄色葡萄球菌在新制培养基中的 A-t生长曲线
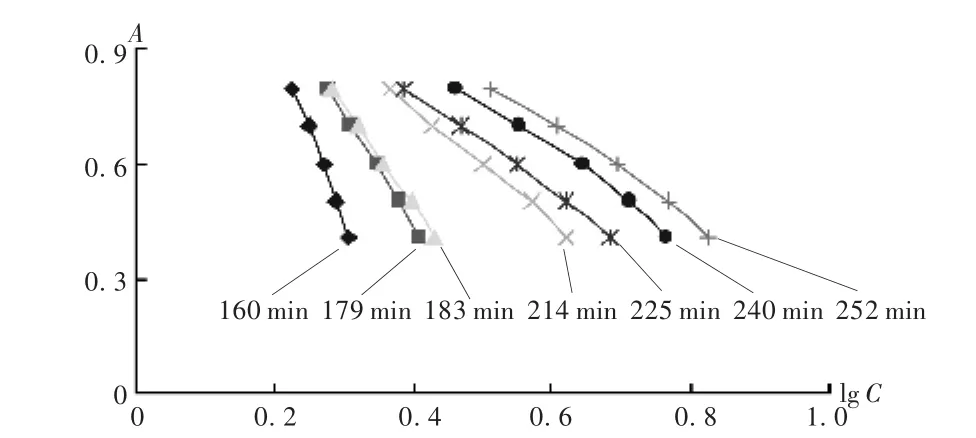
图2 2%金黄色葡萄球菌在培养基中不同培养时间的 A-lg C曲线
一剂量法(标准曲线法):精密量取质量浓度为1 000 μg/mL的标准品溶液,用磷酸盐缓冲液(pH=6.0)稀释成 0.1,0.2,0.4,0.8,1.0 μg/mL 的标准曲线溶液;用磷酸盐缓冲液(pH=6.0)将供试品溶液稀释至约4.0 μg/mL,按上述测定方法测定。计算标准曲线,并计算供试品的效价,当连续5点供试品的效价值误差(RSD)小于2%时终止试验。抗生素质量浓度在0.1~1.0 μg/mL范围内与吸光度值A线性关系良好,线性回归方程为 A=384.448 C+588.816,r=0.999 8(n=5)。
二剂量法:根据一剂量法试验结果,选择0.4μg/mL和0.8μg/mL为二剂量法测定质量浓度;用磷酸盐缓冲液(pH=6.0)分别稀释标准品与供试品溶液;按2005年版《中国药典(二部)》附录ⅩⅣ中的2.2法计算供试品的效价;当连续5点供试品的效价值误差(RSD)小于2%时终止试验。
回收率试验:精密称取已知含量的样品与呋苄西林钠标准品适量,配制成含呋苄西林80%,100%,120%的溶液,分别按一剂量法、二剂量法试验,计算回收率。结果见表1。
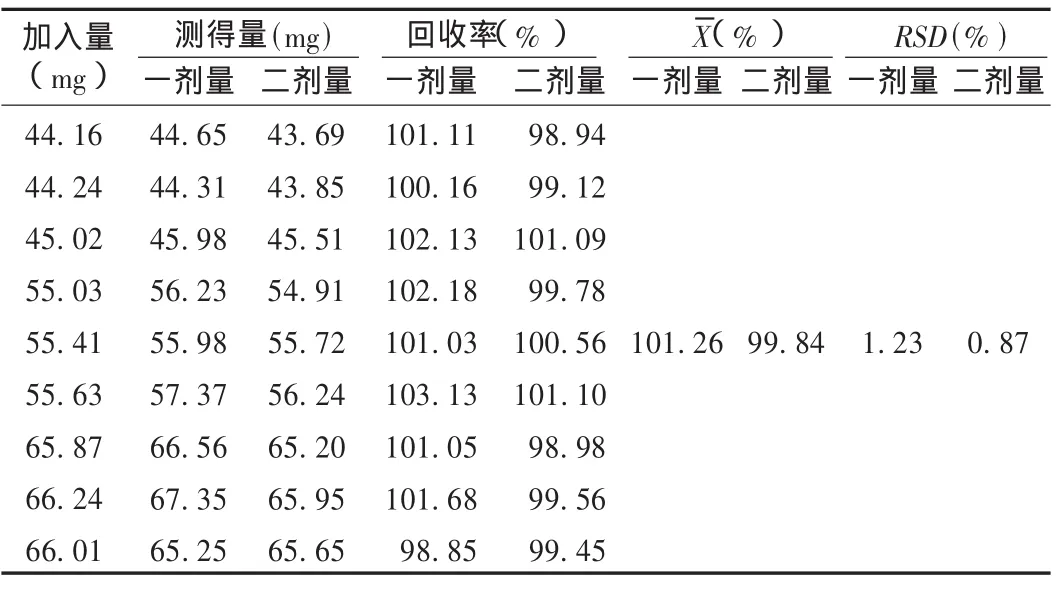
表1 回收率试验结果(n=9)
精密度及重现性试验:取同一供试品溶液在1d内连续测定2次,日内精密度 RSD为0.72%(n=2);取同一供试品溶液连续测定5 d,每日1次,日间精密度 RSD为1.13%(n=5)。
2.2 HPLC法
色谱条件:以C18柱为试验用柱。参考本类物质的HPLC法,在确保所有杂质峰与主峰完全分离的情况下,采用线性梯度洗脱(见表2)。流动相A为磷酸盐缓冲液(0.1 mol/L磷酸二氢钾溶液,用磷酸调pH至3.5)-乙腈(80∶20),流动相 B 为磷酸盐缓冲液 -乙腈(75∶25),流速为1.0 mL/min。
测定法:取本品适量,用水溶解并稀释成4.0 mg/mL的溶液,作为供试品溶液;精密量取1.0 mL,置100 mL量瓶中,加水至刻度,作为对照品溶液。取供试品溶液和对照品溶液各20μL,分别注入色谱仪,记录色谱图(图3)。结果见表3。
2.3 样品测定
分别采用HPLC法、容量法和浊度法对3批呋苄西林钠原料的含量和有关物质进行测定。结果见表3。
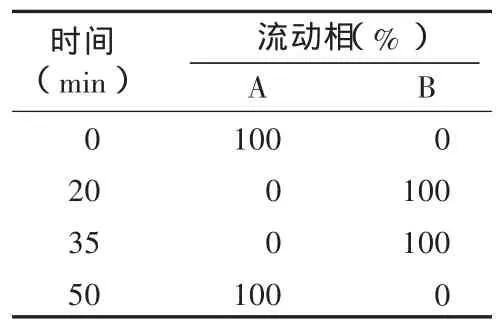
表2 流动相梯度洗脱表
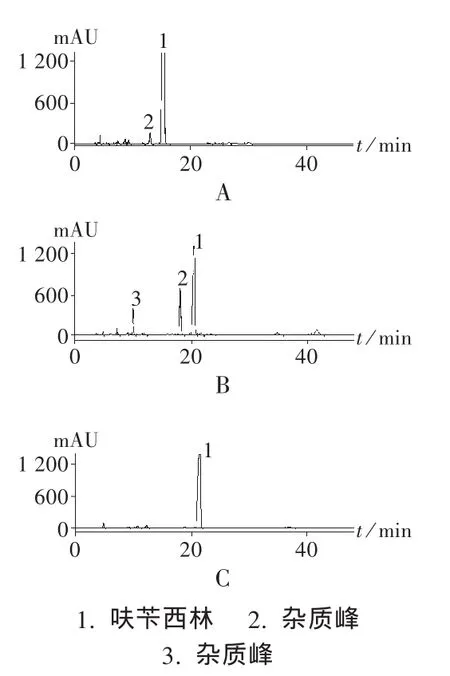
图3 呋苄西林钠有关物质色谱图
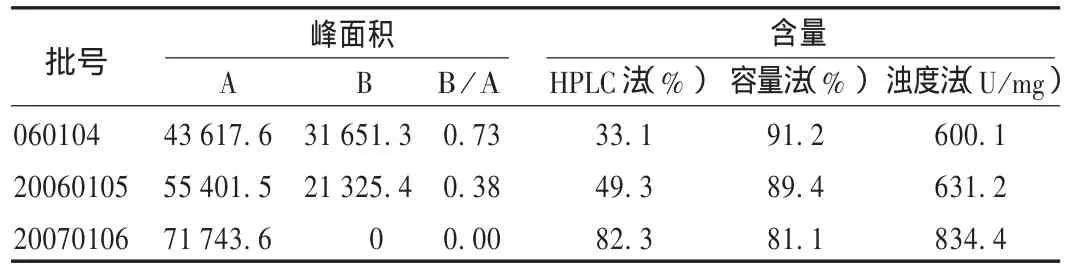
表3 呋苄西林钠有关物质、含量测定结果
3 讨论
从图3可见,不同批号原料的有关物质存在很大差异。其中批号为060104的样品呈单个主色谱峰;而批号为20060105和20070106的样品呈2个较大色谱峰,最大杂质峰(B)与主峰面积的比值高达0.73,说明不同批次间质量存在较大差异。从表3可知,3种方法测定结果存在很大差异。浊度法测定结果显示呈单个主色谱峰的生物活性较高,呈2个较大色谱峰的生物活性较低。
呋苄西林分子中有β-内酰胺结构,不稳定,在偏酸或偏碱条件下会发生水解。剩余酸碱滴定法就是利用这一原理,但不能真实反映抑菌活性。采用浊度法测定效价可克服此不足,能正确反映样品的生物活性。
[1]WS1-C2-0021-89,卫生部药品标准抗生素药品(第一册)[S].
[2]张 菁,王金龙,姜建国.高效液相色谱法测定呋布西林钠的含量及有关物质[J]. 中国药业,2008,17(16):29-30.
[3]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2005:附录Ⅺ A.

