丹红注射液联合甲钴胺治疗糖尿病周围神经病变的Meta分析
马爱霞 金雪晶
一、研究目的及背景
糖尿病周围神经病变(Diabetic PeriPheral Neuropathy,DPN)是糖尿病最常见的微血管并发症和主要致残原因之一,发病率极高。临床上对于已发生的神经病变尚缺乏特效的治疗药物。
关于中医治疗糖尿病周围神经病变的文献报道多为临床疗效的观察,提供的研究方案种类繁杂,不成体系。笔者查阅近7年资料发现,自2005年起,陆续有关于丹红注射液治疗DPN的临床研究开展。相关成果报道自2007年起出现在杂志文章和学术报告中,其中以丹红注射液联合甲钴胺治疗DPN的临床研究居多,可以说这是中医方法治疗DPN的一个新课题。鉴于该研究时间尚短,临床使用并不十分广泛,笔者将对丹红注射液临床治疗糖尿病周围神经病变的常用方案进行有效性、安全性及疗效指标的Meta分析,希望可以使更多的研究者关注这一课题,以期进一步认识丹红注射液在治疗DPN方面的临床效果。
二、文献资料的纳入
(一)文献纳入和剔除的标准
在CNKI中跨库检索中国期刊全文数据库、中国博士学位论文全文数据库、中国优秀硕士学位论文全文数据库以及中国重要会议论文全文数据库,选时间跨度为2004年1月至2010年5月的文献,以“丹红”和“糖尿病周围神经病变”以及“对照组”为检索词进行检索,结果共得到107篇文献。
1.文献纳入标准
(1)将糖尿病周围神经病变患者分为丹红、甲钴胺联合治疗组和甲钴胺组,选择比较腓神经、胫神经以及正中神经的感觉和运动神经传导速度变化、不良反应和疗效为主要评价目的的试验文献。
(2)糖尿病的诊断按照WHO1999年有关糖尿病的诊断与分类标准和国内DPN诊断标准进行判断;排除妊娠患者,严重心、肝、肾功能不全者,患有其他严重糖尿病并发症的患者,以及其他疾病所致的周围神经病变患者。
(3)疗效评定标准:显效为自觉症状消失,膝、腱反射基本恢复正常,肌电图显示神经传导速度(NCV)增加,即NCV>5m/s或恢复正常;有效为自觉症状明显减轻,膝、腱反射未完全恢复正常,NCV<5m/s;无效为治疗前后无明显变化。
2.文献剔除标准
(1)未以研究丹红联合甲钴胺治疗DPN为研究目的的文献。
(2)临床对照试验期间除控制血糖的基本治疗外无法排除其它神经疏导和修复治疗的研究文献。
(3)对照组为维生素B族或其他活血化瘀类中药注射剂的研究文献。
(4)每组例数过少(n<20)的研究文献。
(5)重复发表或有数据抄袭嫌疑的研究文献。
(二)文献纳入情况
以上文所述的文献纳入标准和剔除标准对107篇文献进行初步筛选,共纳入有效文献9篇;治疗组为丹红注射液联合甲钴胺,对照组为甲钴胺。现将纳入研究的原始文献数据列表(见表1)。
三、分析结果
(一)丹红和甲钴胺联合用药与甲钴胺单独用药有效性比较的结果
纳入有效性分析的9篇文献中,采用丹红注射液联合甲钴胺治疗的病人共361例,其中达到显效标准的151例;采用甲钴胺单独治疗的病人共349例,其中达到显效标准的81例。在合并分析前,3个研究的权重调整后OR值的95%CI不包含1,即其他各研究中治疗组相对对照组病人有显著增加显效性的机会。异质性检验结果显示,各试验间的效应值差异不存在异质性[(P=0.54)>0.05]。合并资料分析,采用固定效应模型,合并的OR值为2.64(P<0.00001),合并分析结果表明,菱形完全在垂直线的右侧(图1)。说明丹红注射液联合甲钴胺治疗糖尿病周围神经病变的显效率显著高于甲钴胺。
在纳入文献中,治疗组达到有效标准(显效和有效之和)的319例;对照组达到有效标准的202例。在合并分析前,仅有1项研究的权重调整后OR值的95%CI包含1,即除此之外其他研究中治疗组相对对照组病人有显著增加有效性的机会。异质性检验结果显示,各试验间的效应值差异不存在异质性[(P=0.23)>0.05]。合并资料分析,采用固定效应模型,合并的OR值为5.61(P<0.00001),合并分析结果表明,菱形完全在垂直线的右侧(图2)。说明丹红注射液联合甲钴胺治疗糖尿病周围神经病变的有效率显著高于甲钴胺。

表1 纳入丹红注射液联合甲钴胺研究的原始文献数据
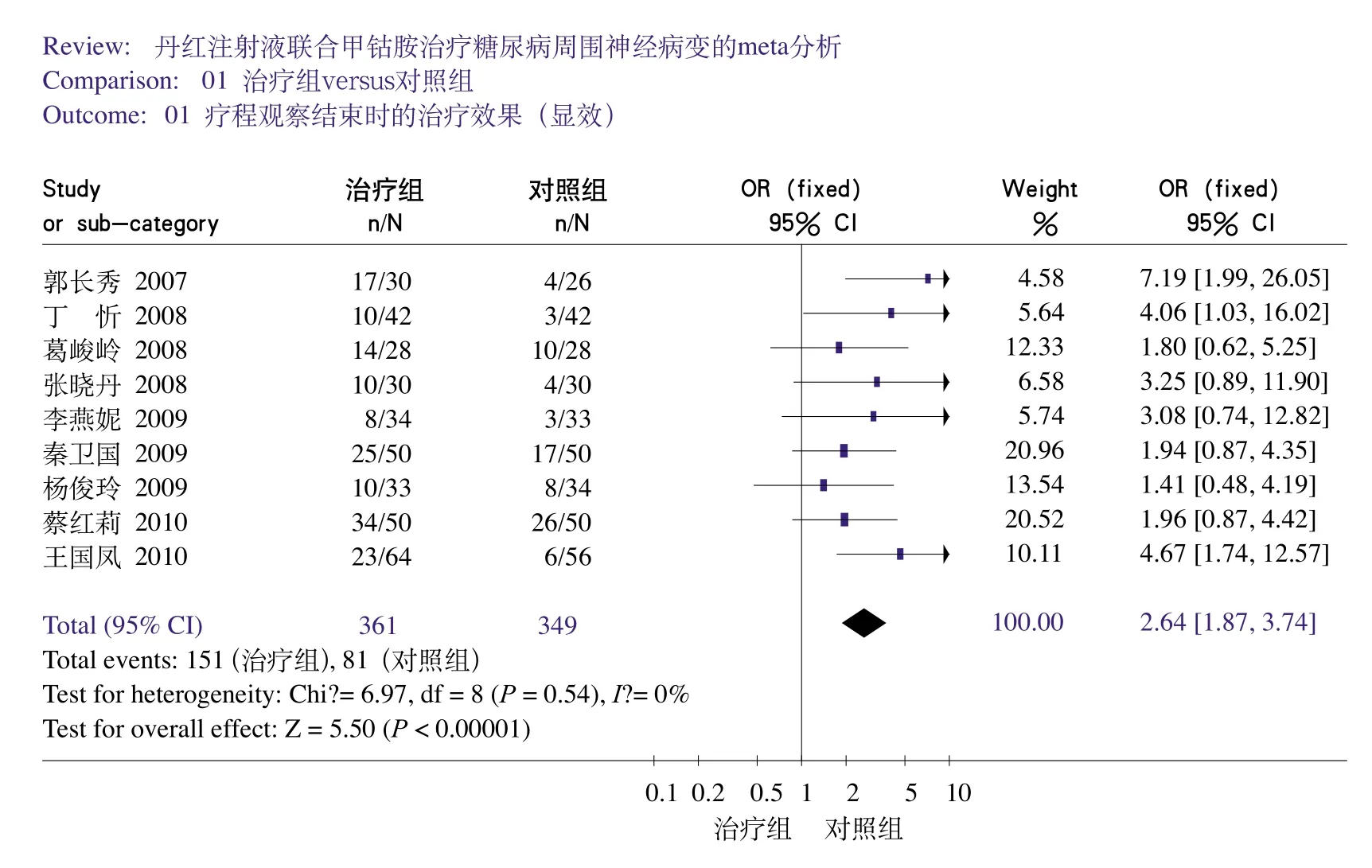
图1 丹红和甲钴胺联合用药显效性Meta分析的森林图(N:样本量;n:显效例数)

图2 丹红和甲钴胺联合用药有效性Meta分析的森林图(N:样本量;n:有效例数)
笔者还就丹红注射液用量和临床治疗显效率之间进行了相关性分析(取甲钴胺用量均为500μg的研究文献,共8篇),得出二者间相关系数r=0.32275,α=0.05时,临界值取值为0.7067>|r|,故就所纳入分析之研究所提供的数据来看,丹红注射液用量与临床治疗显效率之间不存在显著相关性。
基于上述情况,笔者就显效性进行了不同丹红用量的亚组分析。但森林图显示,丹红注射液小剂量(20ml/d)使用时菱形位置比另外两种剂量时更加偏右(图3)。

图3 丹红和甲钴胺联合用药显效性亚组分析的森林图(N:样本量;n:显效例数)
导致这种结论产生的原因可能有:纳入相关性分析文献仅有8篇,涉及数据较少;多数试验数据集中在丹红注射液用量为20ml的试验,不利于相关性分析结果;纳入分析的所有研究之间存在的临床差异和研究者进行数据处理的统计学差异。但由于丹红注射液成分复杂,DPN亦不是其主要适应证,因而在药理和药代动力学方面还应进行更深一步研究,同时也需要更多一线医疗工作者提供量大质优的随机对照试验和临床对照试验报告,以探究丹红注射液联合甲钴胺临床治疗糖尿病周围神经病变时的最佳用药量。
(二)丹红和甲钴胺联合用药与甲钴胺单独用药在改善神经传导速度方面的比较
各个研究在神经传导速度改变方面的研究对象并不统一,测量神经包括正中神经、胫神经、腓神经、尺神经等,测量值包括感觉神经传导速度(SNCV)和运动神经传导速度(MNCV)。纳入研究文献中涉及最多的是腓神经和正中神经的感觉神经传导速度变化的比较,各有5篇。在记录腓神经感觉神经传导速度变化的研究中,接受丹红注射液联合甲钴胺治疗的患者为228例,接受甲钴胺单独治疗的患者215例。在记录正中神经感觉神经传导速度变化的研究中,接受丹红注射液联合甲钴胺治疗的患者为197例,接受甲钴胺单独治疗的患者193例。各研究均采用治疗组和对照组在治疗前和治疗后神经传导速度的均数和标准差(x±s)进行记录。笔者根据在方差已知情况下两个正态总体均值差的区间估计公式,计算出每组治疗前后变化的神经传导速度作为临床指标进行分析。
异质性检验结果显示,两组比较各试验间的效应值差异均存在异质性(P<0.00001),故采用随机效应模型进行合并资料分析。两组分析结果均表明治疗组和对照组治疗前后感觉神经传导速度变化存在显著差异(腓神经P<0.00001,正中神经P=0.004),菱形均完全在垂直线的右侧(图4、图5)。说明丹红注射液联合甲钴胺治疗组治疗前后神经传导速度变化显著优于甲钴胺组。
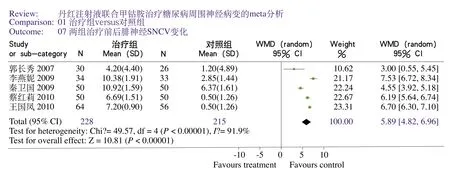
图4 腓神经的感觉神经传导速度(SNCV)变化Meta分析的森林图(N:样本量)
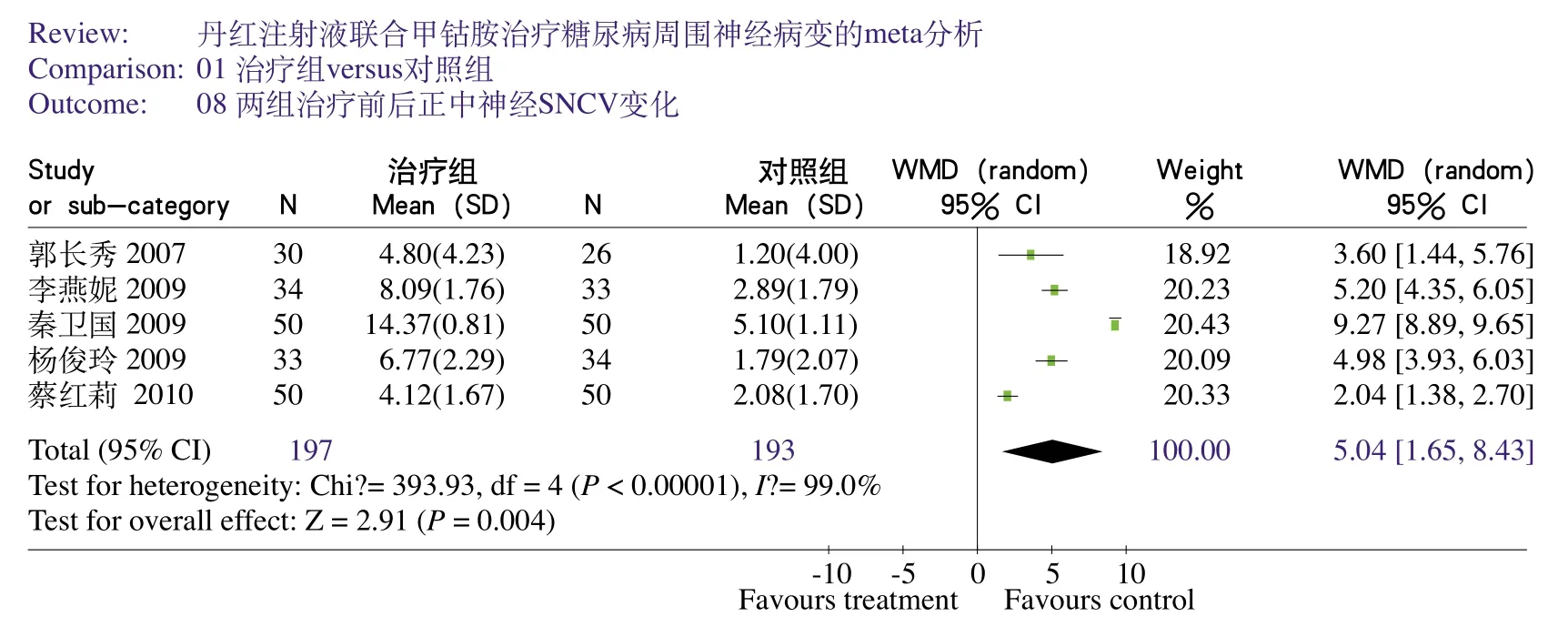
图5 正中神经的感觉神经传导速度(SNCV)变化Meta分析的森林图(N:样本量)
分析导致各项研究结果存在异质性的原因可能包括:采用了不同厂家生产的不同型号的肌电图机进行测量以及测量误差等。
(三)丹红和甲钴胺联合用药与甲钴胺单独用药安全性比较的结果
在纳入分析的9篇文献中,有6篇提到了不良反应情况。但除2篇报道有不良反应发生外,其余均为无不良反应发生,因此无法进行Meta分析。本文将在讨论部分综合其他文献对安全性进行讨论,在此不作赘述。
(四)纳入临床试验的发表性偏倚
绘制漏斗图至少应在5个点以上[10],故本文只绘制了丹红注射液联合甲钴胺治疗糖尿病周围神经病变显效性和有效性的数据漏斗图。图6为显效性分析的漏斗图,图中各点分布较为对称,故可认为发表性偏倚较小。而图7为有效性分析的漏斗图,各点分布对称性不是很强,较大样本集中在左边,因而认为存在一定的发表性偏倚。

图6 丹红和甲钴胺联合用药显效性分析数据漏斗图
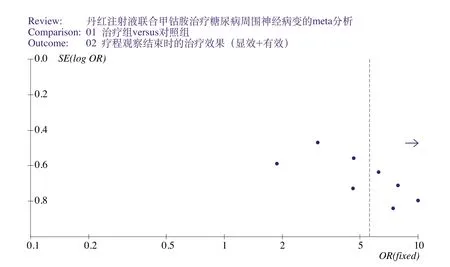
图7 丹红和甲钴胺联合用药有效性分析数据漏斗图
四、敏感性分析
为了考察研究中所含的各种不确定性因素对分析结果的影响,笔者从以下几个角度进行敏感性分析:(1)只包括采用相同剂量(治疗组丹红20ml+甲钴胺500μg;对照组甲钴胺500μg)的文献;(2)只包括每组样本量N≥30的文献;(3)对于连续性变量的结局指标类研究,剔除包含异常结果的文献;(4)选择不同衡量效应尺度,即相对危险度(relative risk,RR)和风险差异(risk difference,RD)。分析结果见表2、表3。
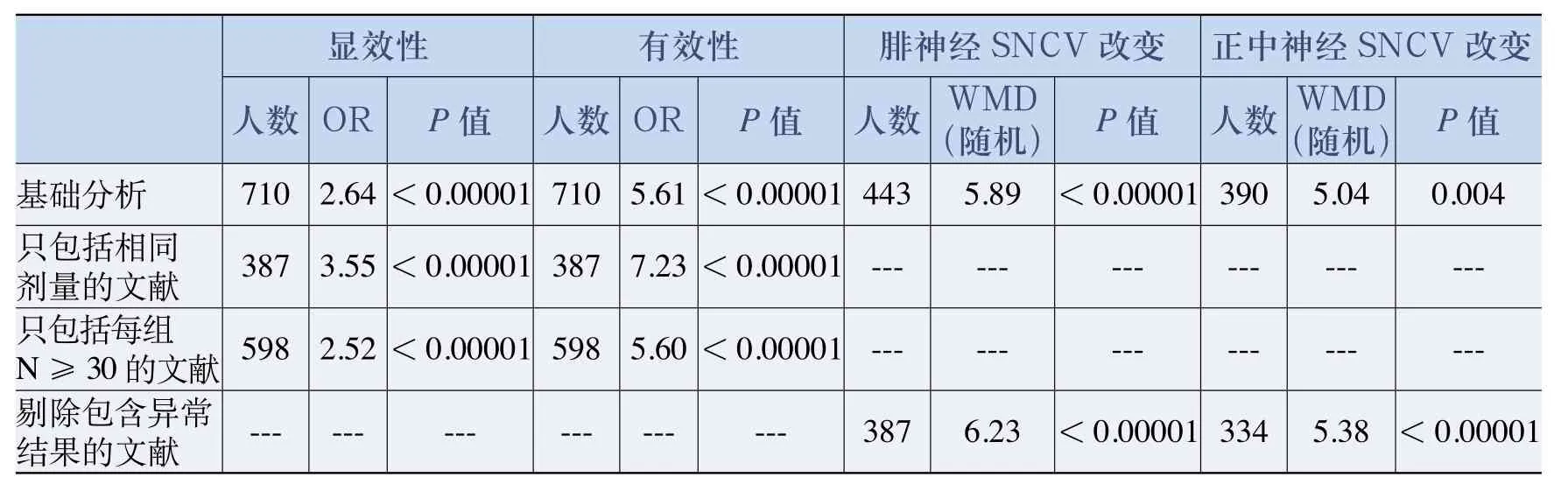
表2 敏感性分析结果(1)
(一)只包括相同剂量的文献
本研究所纳入的临床试验中,甲钴胺用量除1篇为2000μg外,其余均为500μg;丹红注射液所用剂量不统一,分别为20ml(5篇)、30ml(2篇)、40ml(2篇)。由于后两类(30ml和40ml)文献数量过少,只对第一类文献(20ml)的研究进行显效性和有效性的Meta分析。由于涉及腓神经和正中神经的感觉神经传导速度改变的研究数量太少,因此未进行这两项的Meta分析。
纳入显效性研究的5篇文献中,采用丹红联合甲钴胺治疗的病人共199例,其中达到显效标准的70例;单独采用甲钴胺治疗的病人共188例,其中达到显效标准的25例。在合并分析前,各研究之间没有显著性差异(P=0.37)。采用固定效应模型,合并的OR值为3.55(P<0.00001)。同样的5篇文献在进行有效性研究时,各研究之间不存在异质性(P=0.10)。采用固定效应模型,合并的OR值为7.23(P<0.00001)。结果表明当丹红注射液用量为20ml/d、甲钴胺用量为500μg/d时,丹红联合甲钴胺比甲钴胺单独治疗在治疗DPN的显效率上有明显优势。
(二)只包括每组样本量≥30的文献
纳入研究的样本量大小会影响研究结果的产出,样本量大的研究所占权重也大。因此本文将按样本量分层进行敏感性分析,以每组研究例数N≥30为分类标准,对N≥30例的研究进行显效性和有效性的Meta分析。而由于改变条件后纳入的腓神经和正中神经的感觉神经传导速度改变的研究数量太少,因此不再进行Meta分析。
纳入显效性分析的7篇大样本研究中,采用丹红联合甲钴胺治疗的病人共303例,其中达到显效标准的266例;采用甲钴胺单独治疗的病人共295例,其中达到显效标准的167例。在合并分析前,各研究间没有显著性差异(P=0.67)。采用固定效应模型,合并的OR值为2.52(P<0.00001)。同样的7篇文献在进行有效性研究时,各研究间不存在异质性(P=0.11),采用固定效应模型,合并的OR值为5.60(P<0.00001)。对N≥30的大样本研究进行Meta分析获得的结果与本文上述结论相一致,即表明丹红联合甲钴胺比甲钴胺单独治疗在治疗DPN上的显效率和有效率更为突出。
(三)剔除包含异常结果的文献
在纳入腓神经和正中神经感觉神经传导速度改变的5篇文献中,郭长秀的研究[5]结论中标准差过大,因此我们剔除了这一研究质量不佳的文献,对其余文献进行腓神经和正中神经感觉神经传导速度的Meta分析。在腓神经的感觉神经传导速度(SNCV)改变量的研究中,采用丹红联合甲钴胺治疗的病人共198例,采用甲钴胺单独治疗的病人共189例,采用随机效应模型,加权均数差(WMD)为6.23(P<0.00001)。在正中神经SNCV改变量的研究中,采用丹红联合甲钴胺治疗的病人共167例,采用甲钴胺单独治疗的病人共167例,采用随机效应模型,WMD为5.38(P<0.00001)。两组研究纳入数据间仍存在异质性,与上文结果相一致。
(四)选择不同衡量效应尺度
在本次研究中,计量资料研究均采用了优势比(OR),而对于前瞻性随机对照试验,相对危险度(RR)和风险差异(RD)则更加适用。RR为相对比值,是治疗组与对照组的结局发生率之比,一般来说当OR<RR时,用OR来估计风险会更敏感一些。RD为绝对差值,是治疗组与对照组的结局发生率之差,如果两率较大,检验两率的差值用RD值较好;由于是两组之差,RD的变异性最大[11]。本文选择RR和RD作为衡量效应尺度,对所纳入研究的9篇文献(共710人,丹红联合甲钴胺治疗组361人,甲钴胺单独治疗组349人)进行Meta分析的结果如表3所示。

表3 敏感性分析结果(2)
从表3来看,在改变衡量效应尺度后,显效性的合并分析结果与上文结论一致。但有效性则显出纳入研究各结果间的异质性,故该用随机效应模型进行分析,合并分析结果仍为丹红联合甲钴胺比甲钴胺单独治疗在临床治疗DPN中更有效。
五、讨论
本文以药物经济学和统计学原理作为指导,主要采用Meta分析对丹红注射液联合甲钴胺在临床上治疗糖尿病周围神经病变的有效性、安全性及临床效应指标进行评价。本文纳入了9个研究丹红注射液联合甲钴胺在治疗DPN方面有效性的中文随机对照试验。通过Meta分析发现,与单独使用甲钴胺相比,丹红联合甲钴胺在显效性、有效性、神经传导速度改善方面均有优势。本文从用药剂量、样本量、剔除显著差异的文献、选择不同衡量效应尺度等方面开展了敏感性研究,大多数敏感性分析的结果与结论相同;但当改变有效性研究的衡量效应尺度时,纳入研究结果出现异质性。
在安全性方面,由于涉及随机对照试验中不良反应例数的文献过于少,无法进行定量分析。在联合用药分析纳入的9篇文献中仅有2篇在丹红和甲钴胺联合治疗组出现不良反应,2例轻微[6],1例因皮疹退出[7];在丹红对比维生素B族的研究以及丹红注射液联合其他药物使用治疗DPN的研究中,均无不良反应报道。仅根据上述报道,可以认为使用丹红注射液治疗DPN是安全的。但偶见的联合用药发生不良反应的原因较为复杂,无法确定是否由丹红注射液引起,说明书注明的丹红注射液常见不良反应为头晕,头痛,心悸,发热,皮疹,偶见过敏性休克,医疗工作者在临床使用中应当注意。
此外,由于文献资料数量偏少和质量差异等原因,本研究还存在有待进一步完善之处:
(1)作为一类用来综合比较对同一科学问题所取得研究成果的统计方法,Meta分析的优势在于对同类小样本研究结果的统计合成,可增大样本量,提高研究的精确度。但出于各种原因,研究人员在发表研究结果时往往会带有主观性偏倚,当得出阴性结果时一般不愿发表;杂志社也可能会因发表性偏倚的存在而拒绝发表阴性结果的文章。这种现象导致了许多带有阴性结果的文章无法发表,因而本文也存在偏倚的可能[12]。
(2)丹红注射液为国家食品药品监督管理局在2002年批准的处方药,临床使用时间尚短。其说明书写明的功能主治为:活血化瘀,通脉舒络;主要用于瘀血闭阻所致的胸痹及中风,以及心脑血管疾病。糖尿病周围神经病变并不是其主要适应证。由于报道使用丹红注射液进行DPN治疗的文献均出现在2007年以后,笔者跨4个数据库进行检索,但得到的可纳入Meta分析的文献仍然很少,尤其是在不良反应方面可纳入的文献数量无法达到Meta分析的要求,故在进行安全性分析时无法给出详实的数据依据,只能进行定性分析。若能在以后的研究中获得更多关于丹红注射液治疗DPN方面的安全性数据,则能使整个研究更加完整,使结论更具说服力。
(3)对于丹红注射液治疗糖尿病周围神经病变的研究还处于摸索阶段,试验研究相关报道较少,且尚未建立病证相结合的DPN动物模型及相关论证,还需研究者进一步研究。
[1]葛峻岭(Ge JL)等.丹红联合甲钴胺治疗糖尿病周围神经病变的疗效观察[J].实用心脑肺血管病杂志,2008,16(4):51-52
[2]王国凤(Wang GF)等.丹红联合甲钴胺治疗糖尿病周围神经病变疗效观察[J].现代中西医结合杂志,2010,19(2):188-189
[3]秦卫国(Qin WG)等.丹红注射液联合甲钴铵治疗糖尿病周围神经病变50例临床观察[J].广东医学院学报,2009,27(5):533-534
[4]张晓丹(Zhang XD)等.丹红注射液联合弥可保治疗糖尿病周围神经病变[N].中国医药导报,2008,5(24):107
[5]郭长秀(Guo CX)等.丹红注射液联合弥可保治疗糖尿病周围神经病变的疗效观察[J].中国实用医药,2007,2(17):71-72
[6]蔡红莉(Cai HL)等.甲钴胺联合丹红注射液治疗老年糖尿病周围神经病变的疗效观察[J].中国实用神经疾病杂志,2010,13(3):77-78
[7]杨俊玲(Yangt JL).丹红注射液联合甲钴胺治疗糖尿病周围神经病变33例疗效观察[J].云南中医中药杂志,2009,30(10):10-11
[8]李燕妮(Li YN).丹红注射液联合甲钴胺治疗糖尿病周围神经病变疗效观察[J].人民军医,2009,52(1):34-35
[9]丁忻(Ding X),刘玉坤(Liu YK).丹红注射液治疗糖尿病性周围神经病变疗效观察[J].辽宁中医杂志,2008,35(4):572
[10]康德英(Kang DY)等.Meta-分析中发表性偏倚的识别与处理[J].中国循证医学杂志,2003,3(1):45-49
[11]钟文昭(Zhong WS)等.Review Manager(RevMan)--临床医生通向Meta分析的桥梁[J].循证医学,2003,3(4):234-246
[12]张银花(Zhang YH),李洪超(Li HC),马爱霞(Ma AX).唑来嶙酸治疗恶性肿瘤骨转移疼痛的Meta分析[J].中国药物经济学,2009(5):25-36

