毛囊干细胞合成β-NGF及其受体p75NTR对皮肤创伤的早期修复作用
林森,周红利,聂政
(1.成都医学院人体解剖与组胚教研室,成都 610083;2.成都医学院“发育与再生”四川省重点实验室,成都 610083)
皮肤创伤愈合过程不仅仅依赖于表皮干细胞的增生和分化,当表皮严重受损时HFSC可向创伤部位迁移,可能形成新的表皮细胞促使伤口愈合[1-6]。多种细胞参与皮肤创伤修复过程。在创伤后几小时,表皮细胞开始增生并迁移以覆盖暴露的伤口进行再上皮化修复,大量的细胞因子参与愈合过程。有研究发现,β神经生长因子由成纤维细胞、角质形成细胞和肥大细胞等驻留细胞产生,起重要的生理作用,此因子在隆突区的增强可能对毛囊肝细胞的分化和组织修复有重要意义[7]。
1 材料和方法
1.1 实验材料
光学显微镜(Olym pus),磁力搅拌器(江苏海门仪器),电子天平(Sartorius),-20℃低温冰箱(Siemens),-80℃低温冰箱(Sanyo),纯水系统(Millipore),冰冻切片机(Leica,德国)。DAB(北京中山生物技术),β-NGF ELISA试剂盒(武汉博士德),OCT包埋剂(Leica,德国),PBS粉末,抗体稀释液SP-9001抗兔免疫组织化学试剂盒,SP-9002抗鼠免疫组织化学试剂盒都购自(北京中杉金桥生物技术公司),小鼠抗K 15多克隆抗体(Novocastra),兔抗β1-integrin多克隆抗体(武汉博士德),兔抗CD34多克隆抗体(武汉博士德),兔抗β-NGF多克隆抗体(武汉博士德),兔抗p75NTR多克隆抗体(北京博奥森)。
1.2 实验方法
1.2.1 制作在体创伤模型 选取7 d龄SD乳鼠,同一时间用外科手术刀切除新生鼠双侧唇部表皮全层组织,深达真皮,可见裸露毛囊头部。
1.2.2 取材 分别在创伤后2、4、6、8、10、12 h取双侧唇部组织进行相应指标检测。并在每个时间点使用苏木精-伊红(HE)染色观察表皮愈合情况。同时在同窝新生鼠中按照上述时间点取相应的正常唇部组织作为对照,进行相同指标检测。所有切片进行冰冻切片,厚度6μm,丙酮后固定。
1.2.3 创伤组织和正常组织的HFSC定位以及β-NGF及p75NTR的检测 采用免疫组织化学方法,所有切片进行冰冻切片,4℃下丙酮后固定。取冰冻切片,常温下晾干,待湿气消散后用PBS洗4 min×3,37℃下3%H 2O2封闭20m in,PBS洗4 min×3,封闭液(2%羊血清)室温孵育30 min,吸去封闭血清,勿洗,添加β神经生长因子抗体(1∶200),一抗(设PBS空白对照)。所有切片37℃孵育1 h后再进行4℃湿盒内过夜孵育,次日PBS漂洗4 min×4,加生物素化二抗,37℃孵育40min,PBS洗4min×3,加三抗,37℃孵育40 min,PBS洗4min×3,滴加DAB显色液,显微镜下观察显色结果。充分冲洗,干燥脱水,二甲苯透明,中性树脂封固。其他一抗为K 15(1:70)、β1-integrin(1∶100)及CD34(1∶100)和p75NTR(1∶100),方法类同。
1.3 图象分析
使用Olympus全自动数码镜头采集图像,以目标染色区域阳性强度双盲法即阴(0)、弱(1)、中(2)、强(3)和很强(4)来分析所有切片阳性平均值。
1.4 统计学分析
采用Spss11.0对数据进行one-way and twoway ANOVA分析检验。以P<0.05为差异有统计学意义,P<0.01为差异具有显著性统计学意义。
2 结果
2.1 HE染色观察表皮全层切除已经愈合情况
早期愈合过程中(图1),全层表皮切除后,可见创伤愈合短时期,即2~12 h的情况。2 h时表皮全层已经切除,而12 h时期表皮正在愈合,有肉芽组织出现,上层表皮与真皮组织结合不紧密,结缔组织出现。毛囊隆突区变化较小,隆突区各层细胞无明显的形态学变化。
2.2 检测表皮全层损伤后毛囊隆突区的β-NGF、p75NTR、K 15、CD34和β1-integrin表达
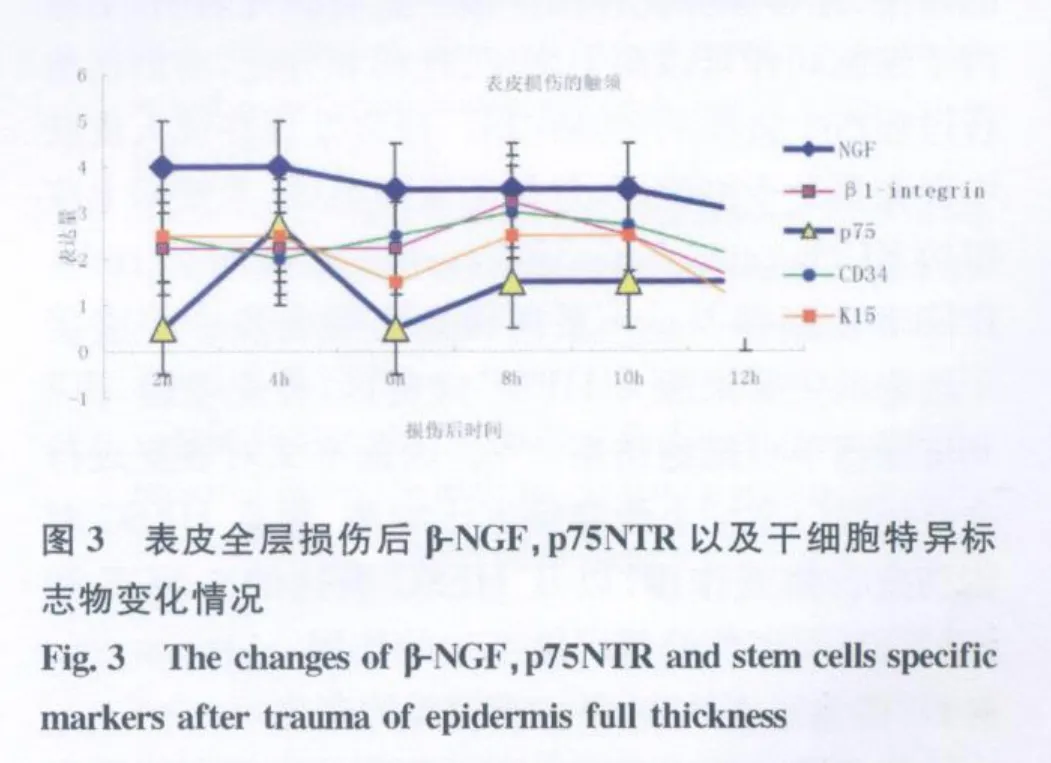
β-NGF在2~10 h表达平稳,但是到创伤后12 h呈下降趋势(图2,3)。而p75NTR在创伤初始阶段4 h表达升高,随即平稳至12 h。对于β1-integrin,CD34和K 15呈先抑后扬式表达,即在6 h时略有降低,随后8 h时增高,但都在10 h和12 h时间点呈降低多趋势(图2,3)。
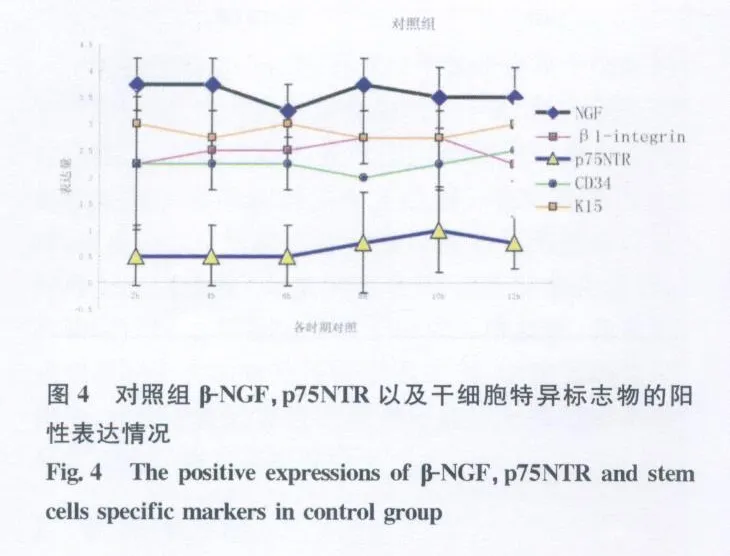
正常对照组呈现β-NGF平稳表达,无明显变化;p75NTR表达逐渐升高,在10 h达到最高,随即下降;干细胞标志物CD34,K 15和β1-integrin则在2~12 h期间平稳表达,其波动差别无显著统计学意义图3。
3 Spss 11.0 two-way ANOVA统计分析结果
3.1 组内分析结果
全层表皮创伤后β-NGF的变化在2~12 h时间点与其他时间点无显著差异。在8 h时毛囊外根鞘均匀表达β-NGF,隆突区表达强度与其他部分基本一致;12 h时β-NGF表达在外根鞘最外层,隆突区表达强度比其他部分大(图3)。
β-NGF的变化在2~12 h时间点无明显差异(P>0.05)(图3)。β1-integrin的变化在12 h与其他时间点有显著差异(P<0.05)(图3)。
p75NTR的变化在2、4、6 h与其他时间点有显著差异(P<0.05)(图3)。
CD 34的变化在4 h、与其他时间点有显著差异(P<0.05)(图3)。
K 15的变化则在6、12 h与其他时间点有显著差异(P<0.05)(图3)。
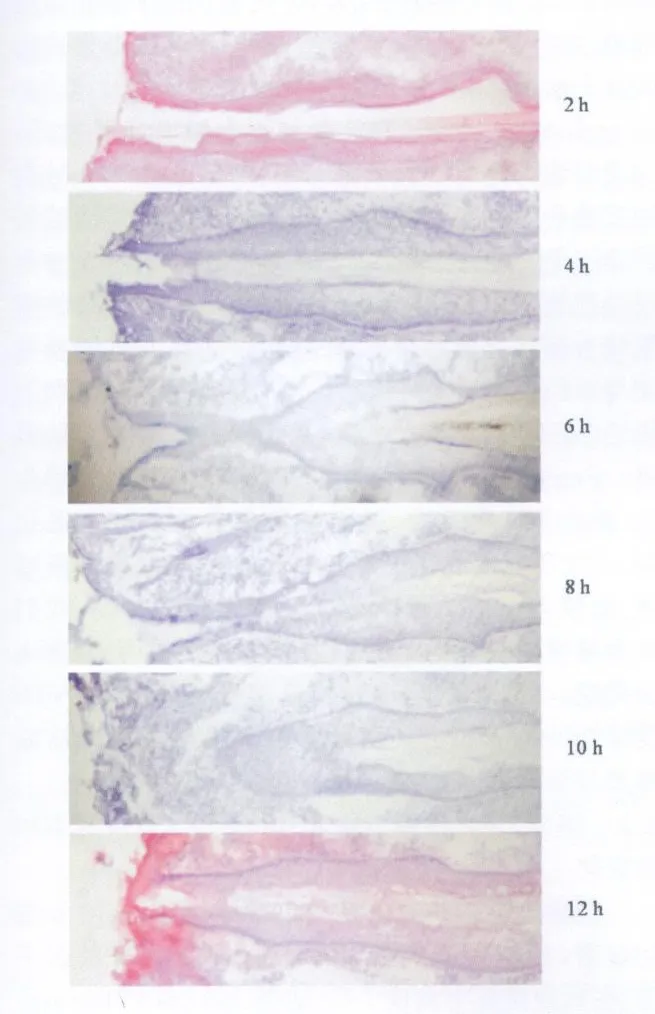
图1 表皮全层创伤后2~12 h愈合过程(HE染色×200)Fig.1 Haling process ofepiderm is full thickness after trauma 2-12 hous

3.2 组间分析结果
全层表皮创伤后β-NGF与对照组相比无显著变化;β1-integrin与对照组相比在2~12 h无显著变化;p75NTR与对照组相比在4 h变化显著;CD34与对照组相比在2~12 h无显著变化;K 15与对照组相比在6、12 h变化显著。
4 讨论
当创伤发生后,创面临近的KC自我更新过程被打断。KC被激活,这意味着KC分泌各种细胞因子和生长因子,同时自身对这些因子产生应答。最终,对这些因子的应答改变了KC表型,使KC成为激活状态KC[8]。在创伤愈合过程中,许多细胞以及因子发挥重要的生理作用,参与创伤修复。以往研究认为表皮的创伤修复主要依赖于表皮干细胞的增生、迁移和分化作用。但一直有研究表明,毛囊内干细胞同样可以向上增生、迁移和分化,对创伤愈合过程产生重要的生理作用。研究发现在成人皮肤中存在多个干细胞库,包括毛囊隆突区、毛囊间上皮组织KC(keratinocytes of interfollicular epiderm is,IFE)和皮脂腺[9]。一系列研究证明表皮中多潜能干细胞的主要来源为HFSC隆突区,补充毛囊、IFE和皮脂腺单位细胞谱系[4,10]。因此本文对表皮进行全层切除以激活毛囊隆突区干细胞,观察HFSC对创伤愈合修复作用,以及HFSC表达的β-NGF和p75NTR对创伤修复可能产生的作用。
4.1 隆突区β-NGF和p75NTR的变化
本文挑选四个显著差异的创伤时期来展示隆突区β-NGF和p75NTR的变化。其中β-NGF在创伤后2~12 h的毛囊隆突区无显著降低,其他时间点基本保持一致。这说明2~10 h时期HFSC表达的β-NGF无显著变化。但是在12 h时间点下,β-NGF的表达与对照组相比有显著的降低。与此同时,HFSC特异性标志物β1-integrin、CD34和K 15的表达在临近12 h时期不同程度地降低,这提示β-NGF的12 h时期表达变化与HFSC的干细胞性质转变有关。以往研究发现,表皮受损时,HFSC会被激活,向创伤部位迁移、增生和分化为表皮细胞,修复创伤部位[1-6]。根据本研究所得结果,我们判断HFSC可能已经发生迁移,因此所表达的β-NGF降低,同时β1-integrin的降低同样说明HFSC的黏附分子减少,黏附力下降,可能发生迁移趋势。如果进行细胞标记追踪来验证此结果,效果会更佳。结合以往认为β-NGF在创伤修复中的作用[11-13],我们认为HFSC合成的β-NGF间接分泌到胞外,对创伤愈合起作用。Hasan等[14]研究发现在新生鼠表皮中β-NGF在创伤后2 d表达较高,这与本研究结果β-NGF在毛囊隆突区表达降低正相反,提示HFSC对于创伤愈合的修复方式可能不同于单纯表皮细胞参与创伤愈合方式。按照迁移理论,隆突区HFSC受到刺激后离巢,向表皮迁移,分化为TA细胞和表皮细胞,填补创伤区域。正常的β-NGF表达则为持续同一个水平,48 h无下降趋势。
p75NTR的表达在4 h与正常组有显著差异,这说明该受体的变化比β-NGF频繁。在4 h时期的突然升高可能说明此时对β-NGF以及其他神经营养因子的应答增强,结合隆突区含有至少25种不同类型的密集表皮神经末梢[15-17]以及短时期的恢复(8 h恢复正常水平),我们推测这种突然增强可能与神经末梢的瞬时信息传递有关。这种短时期间隔的HFSC对创伤修复作用目前尚无相关文献报道。Peters等[18]发现p75NTR能够抑制毛囊的生长,促进其退化发生,诱导毛囊由生长期进入退化期,本文研究发现在正常组中,p75NTR表达逐渐增强,参照Generini等[13]定义毛囊发生的时期,我们认为隆突区表达的p75NTR同样促进了毛囊进入退化期。p75NTR在4 h的显著升高,说明β-NGF受体之一的p75NTR可能参与了早期炎症激活或者是其他效应,但还需要进一步的验证和实验。
4.2 HFSC特异性标志物β1-integrin、CD34和K15的变化
实验组中β1-integrin与正常组比较在12 h变化显著,创伤后隆突区β1-integrin在12h表达下降,在后期研究中发现18 h增强(data not shown)。由于β1-integrin为细胞黏附分子,因此我们推测HFSC的迁移从创伤后12 h前就已经开始。相关文献证明在表皮全层切除后第3天创伤边缘的棘层和颗粒层有散在的表达β1-integrin的细胞出现,并且该种类细胞的数量在不断增加[19]。结合HFSC在外根鞘70~100μm/d迁移距离以及表皮与毛囊隆突区的距离,我们推测表皮创缘逐渐增加的β1-integrin可能来自于隆突区HFSC。
CD34是细胞表面标志分子之一,一直以来是胚胎干细胞,血管细胞和其他多种细胞的标志物,同样也可作为外根鞘细胞的特异标志物。在正常组中表达基本稳定,而在实验组中却呈现中间弱,两端高的趋势。我们推测这种原因与HFSC部分迁移后造成的短期干细胞分裂不平衡,干细胞巢逐渐补充干细胞数量有关。
K 15为隆突区干细胞的特异性标志物,在创伤后6、12 h与正常组有显著差异。以往干细胞相关研究结果表明,创伤因素会造成基底层中K 15(K 15为成熟基底层细胞KC表型)的降低,提示创伤为促使细胞分化的因素[20]。一个干细胞分裂为一个TA细胞和一个干细胞子代。TA细胞不断迁移,而干细胞则驻留在干细胞巢。结合β1-integrin和CD34在部分时间点的表达趋势,我们从另一种方向推测表皮全层的创伤同样能够刺激隆突区的干细胞分化迁移。标志物的变化可能同样与干细胞的数量以及分裂速度有关。因此,本文中3种特异性标志物的协同变化一定程度上能够说明干细胞在应对创伤愈合修复时的应激性反应。免疫组织化学方法研究可从形态学角度描述组织的变化,但结论较单一,下一步的研究应采用BrdU标记毛囊干细胞的方法,展示迁移和分化过程,追踪其受到创伤激活后的变化。另外,可采用流式细胞仪对干细胞进行定量定性研究,使研究更加缜密和详尽。
[1] Taylor G,Lehrer MS,Jensen PJ,et al.Involvement of follicular stem cells in forming not only the follicle bu t also the epidermis[J].Cell,2000,102:541-561.
[2] Jahoda CA,Reynolds AJ.Hair follicle dermal sheath cells:unsung participants in wound healing[J].Lancet,2001,358(P2P1):1445-1448.
[3] Chase HB.Grow th of hair[J].Phy siol Rev,1954,34:112-126.
[4] Cotsarelis G,Sun TT,Lavker RM.Label-retaining cells reside in the bulgearea of pilosebaceousunit:implication for follicular stem cell,hair cycle,and skin carcinogenesis[J].Cell,1990,61(7):1329-1337.
[5] Cotsarelis G,Cheng SZ,Dong G,et al.Existence of slow-cycling limbal basal cells that can be preferentially stimulated to proliferate:implications on epithelial stem cells[J].Cell,1989,57:201-209.
[6] Ronfard V,Rives JM,Neveux Y,et al.Long-term regeneration of human epiderm is on third degree burns transplanted with autologous cultured epithelium grow n on a fibrin matrix[J].Transplantation,2000,70:1588-1598.
[7] 曾俊,陈登榜,代吕霞,等.毛囊隆突区β神经生长因子水平对乳鼠烫伤创面愈合的影响[J].中国组织工程研究与临床康复,2010,14(11):1987-1991.
[8] Tom ic-Canic M,Kom ine M,Freedberg IM,et al.Epidermal signal transduction and transcription factor activation in activated keratinocytes[J].J Dermatol Sci,1998,17:167-181.
[9] Ghazizadeh S,Taichman LB.Multiple classes of stem cells in cutaneous epithelium:a lineage analy sis of adult mouse skin[J].EM BO J,2001,20:1215-1222.
[10] Oshima H,Rochat A,Kedzia C,et al.Morphogenesis and renewal of hair follicles from adultmultipotent stem cells.Cell,2001,104:233-245.
[11] Kawamoto K,Matsuda H.Nerve growth factor and wound healing[J].Prog Brain Res,2004,146:369-384.
[12] Muangman P,Muffley LA,Anthony JP,et al.Nerve grow th factor accelerates wound healing in diabeticmice[J].Wound Repair Regen,2004,12(1):44-52.
[13] Generini S,Tuveri MA,Matucci Cerinic M,et al.Topical application of nerve grow th factor in human diabetic foot ulcers:a study of three cases[J].Exp Clin Endocrinol Diabetes,2004,112(9):542-544.
[14] Hasan W,Zhang RJ,Liu M X,et al.Coordinate expression of NGF andα-smoothactinm RNA and protein in cutaneous wound tissue of developing and adult rats[J].Cell Tissue Res,2000,300:97-109.
[15] Bergm an E,Ulfhake B,Fundin BT.Regulation of NGF-family ligands and receptors in adulthood and senescence:correlation to degenerative and regenerative changes in cutaneous innervation[J].Er J Neurosci,2000,12:2694-2706.
[16] Fundin B,Rice FL,Pfaller K,et al.The innervation of the mystacial pad in the adult rat studied by anterograde transport of HRP-conjugates[J].J Com p Neurol,1994,99:223-246.
[17] Rice FL,Fundin BT,A rvidsson J,et al.Comp rehensive immunofluorescen ce and lectin binding analysis of vibrissal follicle sinus complex innervation in the mystacialpad of the rat[J].J Comp Neu rol,1997,385:149-184.
[18] Peters EM,Stieg litz MG,Liezman C,et al.p75 neu rotrophin recep tor-mediated signaling promotes human hair follicle regression(catagen)[J].Am JPathol,2006,168(1):221-234.
[19] Li J,Fu X,Sheng Z,et al.Ectopia of epidermal stem cells on wound edge during wound healing process[J].Chin JReparat Reconstr wct Surg,2006,20(3):264-267.
[20] Porter RM,Lunny DP,Ogden PH,et al.K 15 expression implies lateral differen tiation within stratified epithelial basal cells[J].Lab Invest,2000,80(11):1701-1710.