我院258例药品不良反应报告回顾性分析
赵陶丽,赵志刚,庄 洁(首都医科大学附属北京天坛医院药剂科,北京市 100050)
近年来,人们对药品不良反应(ADR)的关注与日俱增,国家也加大了对药品不良反应监测和上报的管理。我院 ADR监测网络正逐步得到完善和加强,ADR报告的数量和质量也有了显著提高。本文对我院2009年1月—2009年12月收到的258例ADR报告情况进行回顾性分析,以了解我院ADR发生的规律及特点,促进临床合理用药,以提高医疗质量。
1 资料与方法
对我院2009年1月—2009年12月各科室呈报的有效ADR报告258例进行回顾性分析。包括患者基本情况、家族及既往ADR史与ADR的发生关系、引发ADR的给药途径及ADR出现时间分布、ADR因果关系评定及转归、联合用药与ADR的发生率、引起ADR的药品种类及主要药品分布、ADR累及系统或器官及临床表现。
2 结果
2.1 性别与年龄分布
258例ADR报告中男性128例(49.61%),女性 130例(50.39%);年龄最小者2.5岁,最大者85岁。发生ADR患者的性别与年龄分布见表1。
2.2 家族及既往ADR史与ADR的发生关系
258例ADR中有家族药品不良反应史16例(6.20%),药品不良反应史的58例(22.48%),提示医师开处方之前,应详细询问患者的药品不良反应史和家族药品不良反应史,对有同类药变态反应者禁用,避免药品不良反应的重复发生,见表2。
2.3 引发ADR的给药途径及ADR出现时间分布
药物的剂型决定给药途径,给药途径影响着药物的生物利用度,生物利用度不仅决定疗效也与ADR密切相关。对引发ADR的给药途径及ADR出现时间分布进行统计分析,可以为临床药物剂型的正确选择提供参考[1]。通过统计可知,ADR出现的最短时间为40 s,最长为14 d。静脉注射171例(66.28%),口服 69例(26.74%),肌内注射4例(1.55%),吸入4例(1.55%),静脉推注 4例(1.55%),皮下注射 3例(1.16%),外用 2 例(0.78%),鼻饲 1 例(0.39%),见表3。
2.4 ADR关联性评价及转归
采用国家ADR监测中心制定的六级标准进行评价。因评价为“肯定”的标准必须是“再次使用,反应再现,并可能明显加重”而临床上出于安全角度往往不会再选用该药,有些病例因无重复试验,根据判断标准不能评定为“肯定”,所以“很可能”、“可能”的结果较多。转归结果中治愈 96例(37.21%),好转161例(62.40%),有后遗症 1例(0.39%)(末梢神经炎),死亡0例,见表4。
2.5 联合用药与ADR的发生率
在258例ADR报告中,联合用药152例(58.91%)。联合用药的数量与药物不良反应呈正相关,故而提示医生应尽量避免不必要的联合用药。联合用药与ADR的发生率见表5。
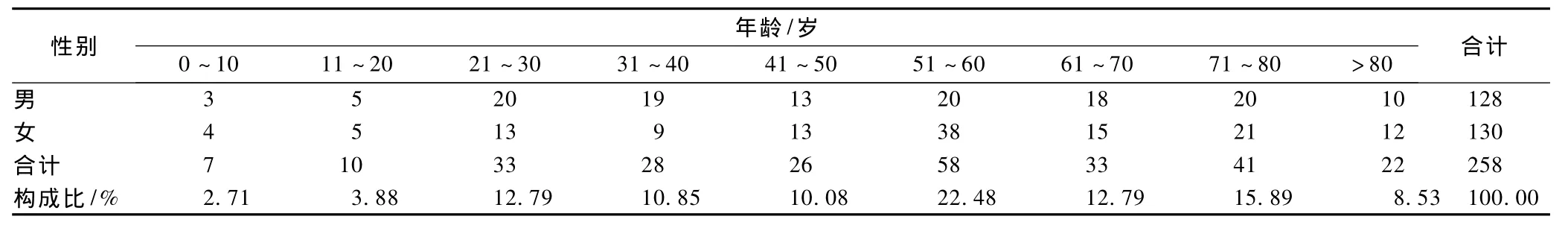
表1 发生ADR患者的性别与年龄分布Tab 1 Distribution of age and sex of ADR cases

表2 家族/既往ADR史与ADR的发生关系Tab 2 Family/Past history of ADR in relation to occurrence of ADR

表3 ADR出现时间及给药途径分布Tab 3 Distribution of onset time and route of administration of ADR cases

表4 ADR关联性评价Tab 4 Evaluation on ADR relevance
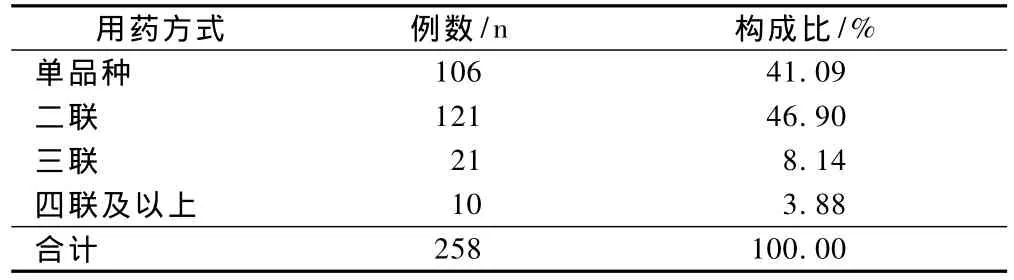
表5 联合用药与ADR的发生率Tab 5 Drug combination and incidences of ADR
2.6 引起ADR的药品种类及主要药品分布
根据《新编药物学》(16版)药品分类方法[2],对所涉及药品进行分类。在引起272例ADR中涉及药品113种。(其中,有些ADR是由2种或2种以上药品共同所致,按所用药物分类统计后有重复病例,故总数大于258例)。引起ADR的药品种类及主要药品分布见表6。
2.7 ADR累及系统或器官及临床表现
皮肤及附件损害居首位,有131例(45.17%),其他较常见的有消化系统、神经系统、心血管系统和全身性损坏。结果见表7(有些药物引起多器官或系统损害,故总数大于258例)。
3 讨论
3.1 ADR发生与性别和年龄的分布
由表1可知,ADR在男女性别上无显著性差异,在各年龄组呈正态分布。>50岁老年患者,有154例(59.69%)与下列因素有关:(1)老年患者脏器功能随年龄增长逐渐减弱,药物在体内的药动学、药效学明显发生变化,药物排泄较慢,药物的血浆消除半衰期延长。(2)老年人的血浆蛋白含量较低,结合药物的能力也有降低,血浆中有活性的游离药物增加,药效增加,易发生不良反应。(3)老年患者常因有多种疾病、合并用药多,用药依从性较差也增加了ADR的发生率[3]。因此,临床医生在给老年患者用药时要重视其生理特点与用药的关系,并加强对老年患者用药的监测。
3.2 引发ADR的给药途径与ADR出现时间的关系
由表3可知,引发ADR的给药途径以静脉注射多见,口服次之。绝大多数ADR出现在用药24 h以前(约70%)且以静脉滴注给药居多,由于静脉给药使药物直接进入血液循环,且无首过效应,生物利用度高,ADR出现也较快较频繁,且静脉给药多用于住院或门诊留观的患者,临床易于发现,因此ADR报告率高于其他给药途径。口服给药引发的ADR大多发生在24 h以后,这与药物经口服后,通过胃肠粘膜吸收再进入血液循环,吸收慢而不规则等特性有关。此外,迟发性过敏反应一般出现在用药后的6~14 d。静脉给药方式也是诱发ADR和并发感染的重要因素,其产生有多方面,包括药物因素、输液操作因素、输液器及患者体质等因素[4]。目前 WHO已将注射剂人均用药次数作为评定合理用药的重要标准。故建议临床医师应遵循“能口服不肌肉注射,能肌内注射不静脉”的用药原则,尽可能地避免或减少ADR的发生,以达到安全、有效、经济用药的目的[5]。
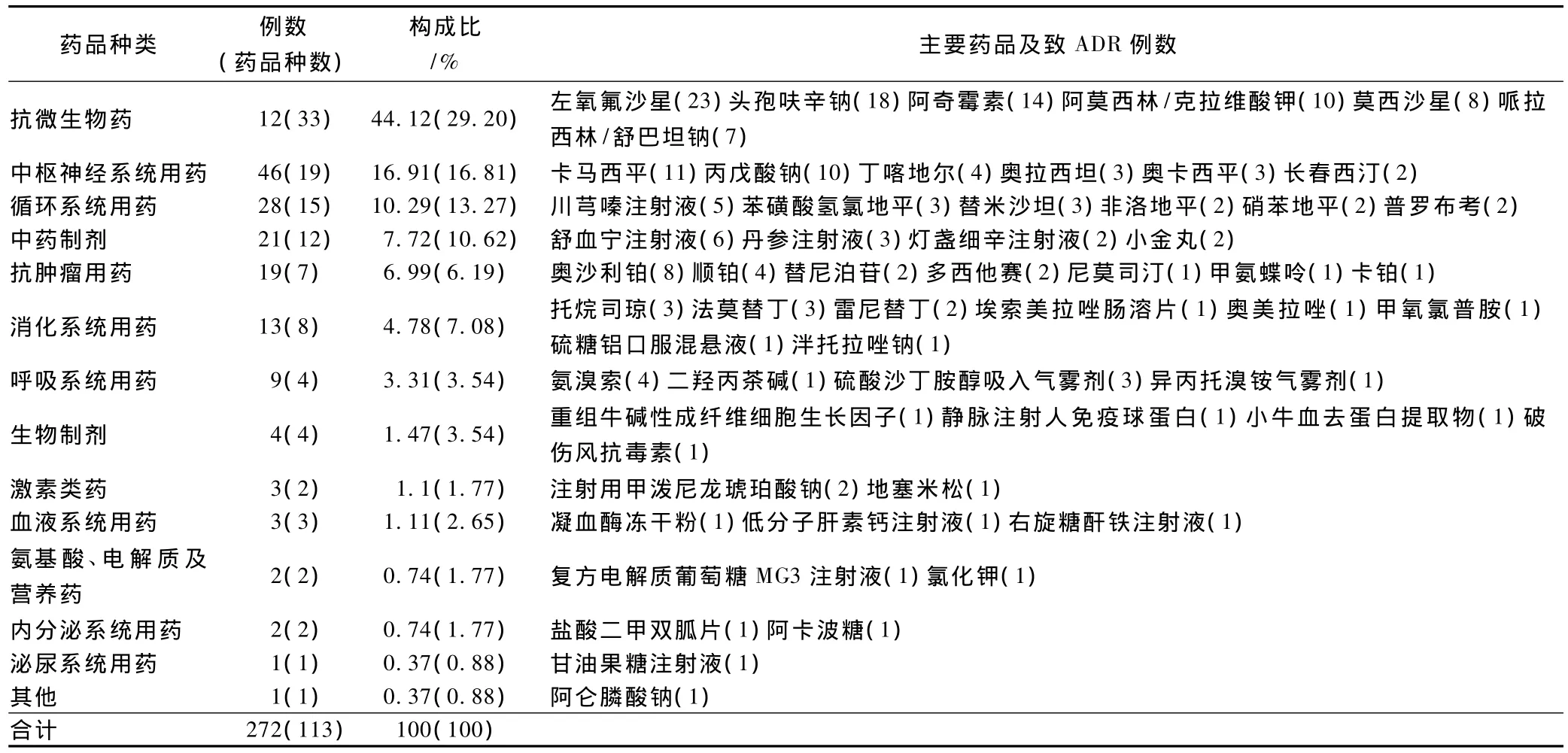
表6 引发ADR的药品种类及主要药品分布Tab 6 Categories of ADR-inducing drugs and distribution of chief drugs

表7 ADR涉及系统或器官及主要临床表现Tab 7 ADR involved systems or organs and clinical manifestations
3.3 加强抗微生物药的临床应用管理,关注联合用药引发的ADR
由表6可见,ADR构成比抗微生物药占首位共120例33种,占总例数的44.12%,这与其临床使用量较大有关。抗微生物药中氟喹诺酮类药物引起ADR例次较多(左氧氟沙星占23例,莫西沙星占8例),这可能与国内的用药趋势及该类药物的特点有关。氟喹诺酮类药具有抗菌谱广、组织通透性好、血药浓度高、不用皮试等特点,故临床应用广泛,由此引发的ADR例次也较多。此外,抗感染药与酶抑制剂的联合制剂引起的ADR例次也较高(阿莫西林/克拉维酸钾占10例、哌拉西林/舒巴坦钠占7例),提示临床上因长期广谱使用抗感染药可能存在许多细菌产生了耐药性而不可避免地选用联合制剂,也提示我们联合制剂因含2种成分其ADR发生率可能大于单一制剂[1]。因此应加强抗微生物药的合理使用和管理,以降低ADR的发生,同时也可减少耐药性的发生。第2位的中枢神经系统药共46例19种占16.91%,与我院是一所以神经科为重点的综合性三级甲等医院,以神经科患者居多、需求量大有关,另外该类药物之间或与其治疗药物之间相互作用较多。例如奥卡西平、苯巴比妥、丙戊酸钠是治疗中枢神经系统疾病的常用药均对肝药酶有影响,奥卡西平为肝药酶诱导剂,但对苯巴比妥则能抑制代谢,提高血药浓度。丙戊酸钠为肝药酶抑制剂,抑制苯巴比妥代谢,此3种药合用时应注意监测苯巴比妥的血药浓度,以免过高引起中毒。苯巴比妥为肝药酶诱导剂,可使丙戊酸钠代谢加快,血浆消除半衰期缩短,肝毒性增加。对于此类药物应尽量减少与之联合用药,以减少ADR的发生。
3.4 慎重使用中药注射剂
中药制剂所致21例ADR占总数的7.72%,涉及12种药物居第4位。近几年国家ADR检测中心发布的《药品不良反应信息通报》中涉及中药ADR的数量和品种逐渐增多,尤其以中药注射剂引起的不良反应为多。目前,中药制剂有效成份的药理、毒理、疗效等方面的机制尚未完全阐明,在炮制、运输、储备过程中理化性质的变化等均有可能引发ADR[6]。另外,中药注射剂与其他药物配伍使用也可导致ADR的发生,建议中药注射剂应单独静脉注射,尽量避免与其他药物合并用药,严格按照药品说明书提供的方法稀释和使用,使用过程中加强用药监测。
3.5 ADR涉及系统/器官与临床表现
从表7看,ADR中以皮肤及附件损害最多,有 131例(45.17%),这与国内其他报道一致[6,7],临床表现为各种药疹和皮肤瘙痒等,各种药疹主要为变态反应所致,ADR症状一般较轻,停药或给予抗组胺药等后症状会逐渐消失。消化系统损害居第2位(36例,12.41%),消化系统 ADR与给药剂量、速度时间、途径、药物遗传学和患者体质等因素影响有关。两者排名居前可能与其临床表现易于观察和诊断,且不易与其他疾病因素相混淆有关。严重的不良反应有5例占1.94%(阿奇霉素、左氧氟沙星引起的过敏性休克3例,卡马西平引起的剥脱性皮炎2例)患者经抢救治疗后恢复正常,严重ADR的出现同药物与用药个体间存在着变态反应、首剂效应、特异质反应有很大关系,其所占比例虽小,但如不及时、合理医治后果会很严重。
4 结论
药品不良反应的发生与多种因素有关,合理用药是减低ADR发生的关键之一。当前,我国药品安全问题多由药品本身质量和使用不当引起,建议临床医生严格掌握用药指征、明确药物之间的相互作用,合理选择药品和给药方式,注意患者既往药物过敏史,减少合并用药种类,加强抗菌药物的合理使用。积极开展ADR监测工作,建立ADR信息网络系统实现资源共享,强化医务人员对 ADR的认识,以最大限度的降低ADR给患者带来的损害,以达到安全、合理的用药目的。
[1] 李 刚,龙恩武.810例药品不良反应报告分析[J].中国药房,2008,19(14):1100.
[2] 陈新谦,金有豫,汤 光.新编药物学[M].16版.北京:人民卫生出版社,2007:1-1004.
[3] 凌春燕,管媛媛.老年人药物不良反应及合理用药干预[J].中国医院药学杂志,2007,27(7):942.
[4] 王 霞.我院2004—2006年266例药品不良反应报告回顾性分析[J].中国药房,2007,18(32):2532.
[5] 杨水英,许 彦,缪 婧.533例药品不良反应报告回顾性分析[J].医药导报,2009,28(6):807.
[6] 杨思芸,王龙飞,李胜前,等.415例药品不良反应报告分析[J].中 国 医 院 用 药 评 价 与 分 析,2009,9(4):316.
[7] 刘佩坚,许沧海.我院药品不良反应上报情况回顾分析[J].中国医院用药评价与分析,2008,8(3):227.

