脲素甲醛树脂铝配合物前驱体热解制备纳米γ-A l2 O3研究
程 芝,杨海玲,甄 远,李 珺,张逢星
(合成与天然功能分子化学教育部重点实验室,西北大学化学与材料科学学院,陕西西安 710069)
脲素甲醛树脂铝配合物前驱体热解制备纳米γ-A l2O3研究
程 芝,杨海玲,甄 远,李 珺,张逢星*
(合成与天然功能分子化学教育部重点实验室,西北大学化学与材料科学学院,陕西西安 710069)
采用聚合物配合物前驱体法,合成了脲醛树脂 R及其铝配合物,对其进行了红外光谱 (IR)、热分析 (TGDSC)等表征;由配合物前驱体热分解制备得到氧化铝粉体,XRD表征表明,制得的氧化铝粉体为粒径 6.72 nm左右的γ-A l2O3.
脲素;甲醛;纳米氧化铝
γ-A l2O3,就是通常所说的活性氧化铝,其属于尖晶石型结构,形成温度较低,粉体颗粒的粒径很小,尤其采用纳米技术制得的颗粒粒度可在数个到数十个纳米,拥有 1 000m2·g-1以上的比表面积,使得γ-A l2O3具有非常广泛的用途,如用作吸附剂、干燥剂、催化剂和催化剂载体等.
纳米氧化铝的制造方法大致分为物理方法和化学方法两类,湿化学合成法发挥了特殊的作用.近年来,由于高分子金属络合物前驱体热解技术的采用,发展了一项金属氧化物纳米粉体制备新工艺,而有关高分子与金属络合热解制得氧化铝的研究见诸报道的则不多.王宏志等[1]用络合物-凝胶法在 A l(NO3)3溶液中加入丙烯酞胺单体 N,N’-亚甲基丙烯酞胺网络剂,在 80℃聚合获得凝胶,经过干燥、煅烧得 10 nm的α-A l2O3粉体.埃及的 D.M.Ibrahim在此方面的研究较多,2008年他通过脲素甲醛凝胶聚合,煅烧后制得 20~30 nm左右的α-氧化铝粉体[2].2009年他们改变反应物的种类用醋酸铝、硫酸铝、磷酸铝作为反应的前驱物,结果表明硫酸铝、磷酸铝可以键合到树脂上,分别制得 26.96 nm和 29.78 nm的α-氧化铝[3].
本文报道了通过配合物的热分解得到纳米氧化铝的方法,并对中间配合物和最终产物氧化铝的性质进行了表征.
1 实验部分
1.1 试剂与仪器
无水乙醇 (A.R.,西安化学试剂厂),脲素 (A.R.,西安化学试剂厂),甲醛 (A.R.,西安化学试剂厂);其它试剂也均系国产 A.R.试剂.
EQU INOX-55型红外光谱仪 (KB r压片,德国 B ruker公司);STA 449C型热分析仪 (德国 NETZSCH公司);X射线衍射仪 (D/MAX-3C,日本理学,Cu靶,Kα辐射线);3300型紫外可见分光光度计 (日本日立公司).
1.2 实验
树脂合成:将 0.1mol脲素溶解到 0.2mol甲醛中,回流搅拌,用氨水调节 pH 8~9,70℃左右反应 0.5 h,产生白色透明溶胶,所得溶胶用蒸馏水抽洗多次,置于烘箱中 75℃烘干 24 h,所得样品为 A.
树脂聚合物 A l配合物原位合成:将 0.1mo l脲素溶解到 0.2mo l甲醛中,回流搅拌,用氨水调节 pH 8~9,70℃左右反应 0.5 h;然后将 0.1molA l(NO3)3·9H2O加入到反应液中,再用氨水调 pH 4~5,产生白色透明溶胶,继续反应 0.5 h.所得溶胶用蒸馏水抽洗多次,置于烘箱中 75℃烘干 24 h,所得样品为 B.
纳米γ-A l2O3制备:将聚合物 A l配合物前驱体在马弗炉中于 800℃煅烧 2 h,得到γ-A l2O3样品 C.
2 结果与讨论
2.1 树脂 A及其 A l配合物的红外光谱
树脂 A及其原位合成的 A l配合物的红外光谱如图 1和图 2所示.

图 1 树脂 A的红外光谱Fig.1 IR spectrum of resin A
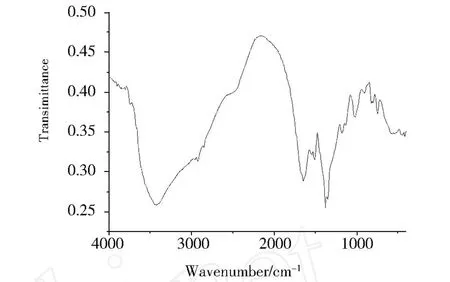
图 2 A l配合物 B的红外光谱Fig.2 IR spectrum of A l com p lex B
由图 1可见,脲醛树脂的红外光谱上,3 340 cm-1处的吸收峰可指派为 -OH、-NH2、-NH伸缩振动,2 958 cm-1处为羟甲基基团 (N-CH2OH)中的 C-H的伸缩振动,1 557 cm-1与 1 507 cm-1吸收峰则为 N-H的面内弯曲振动,C-N的吸收在 1 301 cm-1,1 254 cm-1处,CO-NH-R的吸收峰是 1 455 cm-1处,C=O的吸收是 1 650 cm-1,1 056 cm-1和 996 cm-1,谱图中分别归属为 C-O键伸缩振动和羟甲基 (N-CH2OH)中O-H-伸缩振动,这与文献报道一致[4].
聚合物树脂的铝配合物 B的红外光谱 (图 2)与A的特征吸收比较,可以发现,对应 3 400 cm-1附近的吸收仍然归属于 -OH,-NH2,-NH伸缩振动,但峰形没有原来尖锐,可能起因于其中某些原子与铝的作用;进一步考察指纹区,对应文献 [2]报道的 A l-O的吸收峰 823 cm-1和 490~670 cm-1以及 A l-N的吸收峰911 cm-1也存在,只是强度不大;另外,树脂 A中的 996 cm-1吸收 (图 1)在图 2中显著减弱,对应 1 557 cm-11 507 cm-1处的 N-H的面内弯曲振动在图 2中几乎消失,显然可以证实在 B中 A l原子可能与聚合物分子中的 O和 N原子进行配位.
2.2 配位聚合物 B的 TG-DSC分析
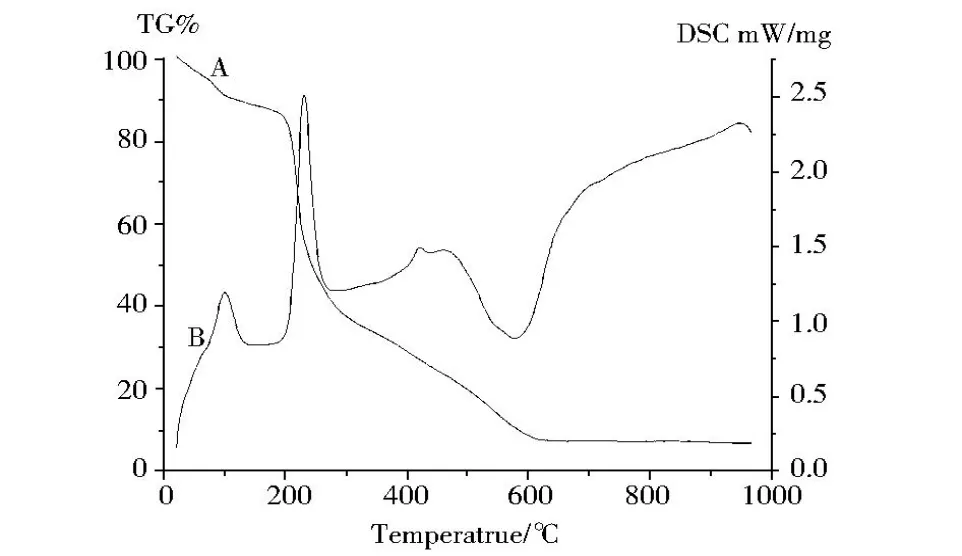
图 3 配位聚合物的 TG-DSC图Fig.3 TG-DSC d iagram of the A l comp lex
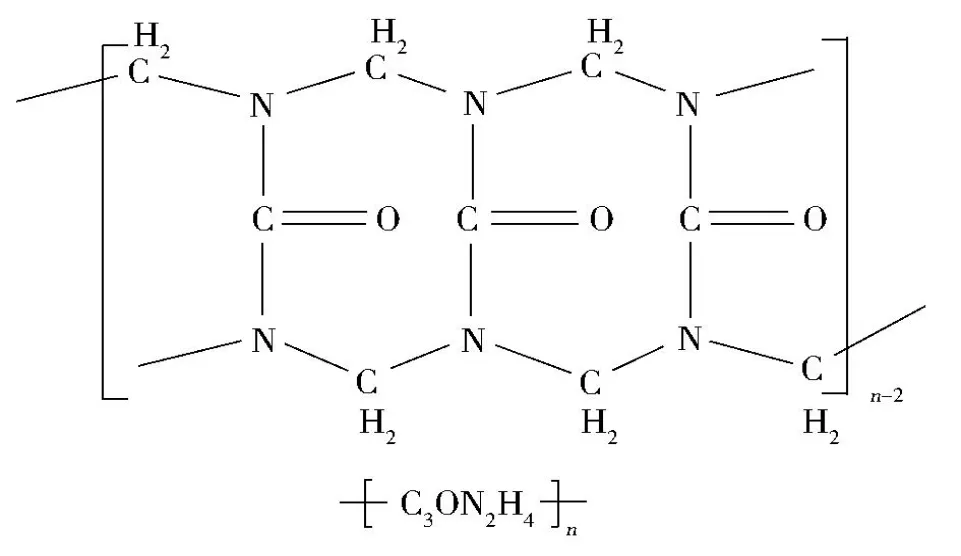
图 4 推测聚合物树脂的结构示意图Fig.4 Structu re of the po lym er resin
聚合物铝络合物前躯体 B的 TG-DSC曲线 (N2气氛,10℃升温速率)如图 3所示.分析 TG曲线,在 100℃之前有逐渐失重过程 (约为 8.2%),推测为失去残留水,对应 DSC曲线出现小的吸热峰;温度升至 209℃左右出现快速失重,这一过程应为聚合物的分解,已知持续到约 600℃.但从 TG曲线的变化趋势看,似乎也是分步的,对应 DSC也有两个峰.温度到 600℃左右出现平台,残留物为 7.1%.
据此分析,假定聚合物三维链接,每个链节的组成计量可写为 -C3ON2H4-(见图 4).折合干聚合物推算,每 5-7个链节才平均键合有 1个 A l原子.或许这是由于 A l原子因空间基团位阻难以进入聚合物内腔内的缘故,也可能与实验合成条件有关系.
2.3 配位聚合物前躯体煅烧产物 C的表征
2.3.1 XRD分析
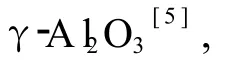
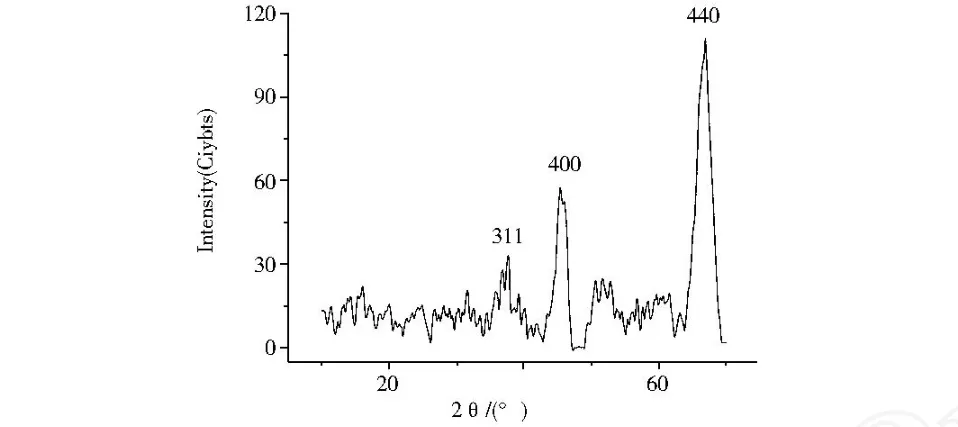
图 5 配位聚合物煅烧粉末 C的 XRD图Fig.5 XRD and charecteristic diffraction data of calcination powders

表 1 配位聚合物煅烧粉末 C的 XRD特征衍射数据Table 1 XRD characteristic diffraction data of calcination powders C from coodiation polymer
根据Scherrer公式D=0.89λ/(B cosθ)(X-线波长λ=1.540 56Å),B为衍射峰半高宽,θ为衍射角),可计算γ-A l2O3原生晶粒的平均粒径[7].取图 5中 (440)晶面衍射峰带入 Scherrer公式,计算得 800℃煅烧2h所得γ-A l2O3原生晶粒的平均粒径φ=6.72 nm.
2.3.2 纳米级γ-A l2O3的红外光谱
煅烧得到的纳米级γ-A l2O3的红外光谱见图 5.可以看出,图谱中 856 cm-1和 1 650 cm-1处出现了非常特征的吸收峰,可以指派为 A l-O键的伸缩振动,按照文献[8],这是γ-A l2O3相的佐证.另外,图谱中 3 425 cm-1处的特征峰归属于 O-H的伸缩振动.据文献报道[9],γ-A l2O3中会存在极少量的 -OH基团,在其结构基元[A lO6]和[A lO4]中,部分 O2-离子可能被 OH-取代,这就是活性γ-A l2O3粉末中存在一定程度的 O-H基团的缘故.

图 6 配位聚合物煅烧粉末 C的红外光谱图Fig.6 IR spectrum of calcination powders C from the polymer resin complex
3 结论
以脲素、甲醛、硝酸铝为原料,通过原位合成制得了铝盐的脲醛树脂聚合物配合物前躯体,通过前躯体的煅烧得到了γ-A l2O3纳米级超细粉末.对前躯体的热分析和 IR光谱进行分析,表明铝离子与树脂的 N原子间有配位作用,但进入聚合物的铝原子只有计量的约 20%;煅烧所得超细粉末经证实为纳米级γ-A l2O3,XRD结果推算产物可达到 6~8 nm.研究结果对于制备小粒度γ-A l2O3的工艺改善有一定参考价值.
[1] 王宏志,高 镰,李炜群,等.高分子网络凝胶法制备纳米α-A l2O3粉体 [J].无机材料学报,2000,15(2):356-360.
[2] IBRAHIM A D M,ABU-AYANA YM.Preparation and Characterization of Ultra fine Alumina Via Sol-gel Polymeric Route[J].Materials Chemistry and Physics,2008,111:326-330.
[3] IBRAHIM D M,ABU-AYANA YM.Preparation of Nano Alumina Via Resin Synthesis[J].Materials Chemistry and Physics,2009,113:579-586.
[4] 李爱萍,阚成友,杜 奕,等.脲醛树脂合成反应过程的 FTIR研究 [J].物理化学学报,2006,22(7):873-877.
[5] LIU Y,MA D,HAN X,eta l.Hydro thermal Synthesis of Microscale Boehmite and Gamma Nano leaves Alumina[J].Materials Letters,2008,62(8-9):1297-1301.
[6] ROOKSBY.X-ray Identification and Crystal Structure of Clay[M].Joint Committee on Powder Diffraction Standards,JCPDS.1951:264.
[7] 南京化工学院,清华大学,华南工学院.陶瓷材料研究方法[M].北京:中国建筑工业出版社,1980:226.
[8] RAM ESH SIVARAJAN,SOM INSKA ELENA,BARUCH C IN.Nanocrystalline γ-Alumina Synthesized by Sonohydrolysis of Alkoxide Precursor in the Presence of Organic Acids:Structure and Morphological Properties[J].J Am Ceram Soc,2000,83(1):89-94.
[9] 田明原,施尔畏,元如林,等.铝氢氧化物和氧化物晶粒的热液法制备及其形成机理[J].中国科学 (E),1998,28(2):113-118.
Preparation of Nanometer γ-alumina Powders by Urea Formaldehyde Resin Synthesis
CHENG Zhi,YANG Hai-ling,ZHEN Yuan,LIJun,ZHANG Feng-xing
(Key Laboratory of Synthetic and Natural Functional Molecular Chemistry of Education Ministry/the College of Chemistry and Materials Science,Northwest University,Xi’an710069,China)
The urea form aldehyde polymer resin and its complex with Al were prepared by the complex precursor method characterized by IR and TG-DSC,The alumina powders were prepared by thermal decomposition of the complex precursor and characterized by X-ray powder diffraction(XRD).The results indicated that the average size of the γ-Al2O3nanoparticles was about6.72 nm.
urea;form aldehyde;nanometer alumina
O614.3
A
0253-2395(2010)04-0573-04
2010-03-12;
2010-04-06
陕西省自然科学基础研究计划项目 (2006B13)
程 芝 (1981-),女,硕士,从事纳米金属氧化物制备与性能研究.*通信联系从 E-m ail:zhangfx@nwu.edu.cn

