2-氨基苯并噻唑配合物的晶体结构及抑菌活性
宋 霜,宋 敏,张怀敏,杨立荣*
(1.河南大学化学化工学院,分子与晶体工程研究所,河南开封475004; 2.河南大学生命科学学院,河南开封475004)
2-氨基苯并噻唑配合物的晶体结构及抑菌活性
宋 霜1,宋 敏2,张怀敏1,杨立荣1*
(1.河南大学化学化工学院,分子与晶体工程研究所,河南开封475004; 2.河南大学生命科学学院,河南开封475004)
合成了2-氨基苯并噻唑与钴和锌的两种金属配合物,利用红外光谱、元素分析、X射线单晶衍射和热重分析等对其结构进行了表征;并研究了两种金属配合物对金黄色葡萄球菌、大肠杆菌、酵母菌的抑菌活性.结果表明,Zn(Ⅱ)和Co(Ⅱ)分别与2个O原子和2个N原子通过4配位形成扭曲的四面体构型;两种配合物对三种菌种均有较强的选择性抑制作用.
2-氨基苯并噻唑;配合物;晶体结构;抑菌活性
含杂原子化合物已被应用于抗菌、抗癌、抗病毒药物以及除草剂等领域,尤其是含硫、含氮等杂原子化合物在形成金属配合物后都表现出很好的生物活性[1-5].2-氨基苯并噻唑具有一定的药理活性[6],被作为抗炎药物、除草剂以及抗生素的结构单元,同时也是调味料和香料的替代品[7].Amnar等研究了此类配体过渡金属配合物的结构[8],但是对其抑菌活性的研究却鲜有报道.作者于非水溶剂中在温和条件下合成了2-氨基苯并噻唑与Zn(Ⅱ)的配合物(CCDC:730017)和Co(Ⅱ)的配合物(CCDC:730018),采用红外光谱、元素分析、X射线单晶衍射和热重分析等手段对其结构进行了表征,并采用扩散法测定了其对三种供试菌种的抑制作用.
1 实验部分
1.1 试剂与仪器
实验中所用试剂均为分析纯.红外光谱使用AVATAR360 FT-IR红外光谱仪,KBr压片,测定范围400 cm-1~4 000 cm-1;C、H和N的元素分析使用Perkin-Elmer 240C型元素分析仪;单晶结构测定使用Bruker Smart CCD型X射线单晶衍射仪;热重分析使用Perkin-Elmer TGA7热重分析仪,程序升温速率10℃/min,氮气流速40 mL/min.
1.2 配合物的合成
将2-氨基苯并噻唑 (0.6 g,4 mmol)溶于10 mL无水乙醇中,向其中加入10 mL溶有乙酸锌 (0.876 g,4 mmol)的甲醇溶液,60℃下反应2 h,反应完成后降至室温,减压过滤,用无水乙醇洗涤,静置滤液,一周后得到淡黄色晶体.钴配合物的合成方法同上.元素分析数据(%,括号内为实测值):C18H18N4O4S2Zn:C 44.68(44.39);H 3.75(3.61);N 11.58(11.43);C18H18N4O4S2Co:C 45.28(45.16);H 3.80(3.70);N 11.74(11.56).
1.3 晶体结构测定
选取适宜尺寸配合物的单晶,以石墨单色化的Mo Kα射线 (λ=0.071 073 nm)为光源,使用Bruker Smart CCD单晶衍射仪在293(2)K下测定晶胞参数并收集衍射点,采用ω/2θ扫描方式,在2.40°≤θ≤25.00°范围内收集到Zn配合物衍射点9 972个,其中独立衍射点3 497个[Rint=0.018 8];在1.48°≤θ≤24.99°范围内收集到Co配合物衍射点10 102个,其中独立衍射点3 571个[Rint=0.041 1].用直接法得到全部非氢原子坐标,对非氢原子坐标和各向异性温度因子进行全矩阵最小二乘法精修.全部计算采用SHELXTL-97程序完成[9].w=1/[σ2(F20)+(0.045 1P)2+0.490 3P],P=(F20+2F2c)/3.配合物的主要晶体学数据列于表1.

表1 配合物的主要晶体学数据Table 1 Crystallographic data for the complexes
1.4 抑菌实验
采用扩散法,在含有供试菌种的琼脂平板上放置若干只内径为6 mm的经灭菌处理的牛津杯,向其中注入不同的供试药剂,于37℃培养箱中培养,24 h后测量抑菌圈直径,据此判断药剂的抑菌效力.供试菌种为金黄色葡萄球菌、大肠杆菌、酵母菌.
使用的培养基为:上层培养基Ⅰ(LB培养基),上层培养基Ⅱ:溶解氯化钾1 g、酵母浸出粉3.0 g、醋酸钠8.2 g、无水葡萄糖1.0 g和琼脂8 g于蒸馏水中,并稀释至950 mL,用1.0 mol·L-1NaOH溶液调节p H值为4.2~5.0,定容至1 000 mL,将培养基分装于500 mL锥形瓶中.下层培养基:溶有15 g琼脂的1 000 mL水溶液.上述培养基均在121℃条件下高压灭菌20 min.
供试原药的配制:原药均用无菌水溶解,用过滤法除菌,在-4℃以下保存.
2 结果与讨论
2.1 红外光谱分析
红外光谱数据表明,2-氨基苯并噻唑中的N-H基团伸缩振动吸收峰ν(N-H)与自由配体ν(N-H)(3 336.5 cm-1)相比,发生了红移,表明配合物中2-氨基苯并噻唑中的N原子参与了配位;两种配合物的羧基特征峰出现在1 612 cm-1和1 618 cm-1,其反对称伸缩振动位于1 378 cm-1和1 372 cm-1,其对称振动峰与反对称伸缩振动峰的差值 (Δν=νasym-νsym)大于200 cm-1,可认为在配合物中羧基采取单齿配位模式[10],这一结果与单晶衍射相一致.
2.2 晶体结构描述
Zn(Ⅱ)配合物和Co(Ⅱ)配合物的晶体结构分别如图1和图2所示,主要键长、键角及氢键数据分别列于表2和表3.
在Zn(Ⅱ)和Co(Ⅱ)配合物中,Zn(Ⅱ)和Co(Ⅱ)配位数均为4,两个2-氨基苯并噻唑配体各提供一个N原子、两个COO-各提供一个O原子分别与中心原子配位,COO-采取单齿配位模式与中心原子结合,形成扭曲的四面体结构,Zn(Ⅱ)和Co(Ⅱ)位于四面体的中心,四个配位原子位于四个顶点.配合物中Zn-N键长 (Zn(1)-N(1)0.201 4(2)nm、Zn(1)-N(3)0.201 9(2)nm)明显长于Zn-O键长(Zn(1)-O(3)0.193 67(18)nm,Zn(1)-O(1)0.194 60(18)nm,见表2).2-氨基苯并噻唑的有关键长与自由配体相比变化不大,两个噻唑环平面之间的二面角为80.6(4)°.由于受到空间位阻的影响,两个2-氨基苯并噻唑的-NH2处于反式位置[11].-NH2通过氢键与COO-中的O原子结合(N(4)-H(4B)…O(4)#1,N(4)-H(4A)…O(1),N(2)-H(2B)…O(2)#3,N(2)-H(2A)…O(3)),氢键的存在使得配合物分子在a轴方向链状伸展,并通过氢键N(4)-H(4B)…O(4)#1进而形成三维网状晶体结构,氢键的存在有利于配合物分子的稳定.

图1 Zn配合物的晶体结构图Fig.1 Crystal structure of Zn(Ⅱ)complex

图2 Co配合物的晶体结构图Fig.2 Crystal structure of Co(Ⅱ)complex
Zn(Ⅱ)原子与两个未参与配位的羧基O原子O(2)和O(4)形成微弱的分子内相互作用 (Zn(1)…O(2)0.275 5(27)nm和 Zn(1)…O(4)0.266 2(19)nm).这种相互作用导致Zn-O-C键角减小 (C(14)-N(3)-Zn(1)124.74(18)°,C(16)-O(1)-Zn(1)108.37(15)°,C(18)-O(3)-Zn(1)112.80(15) °).
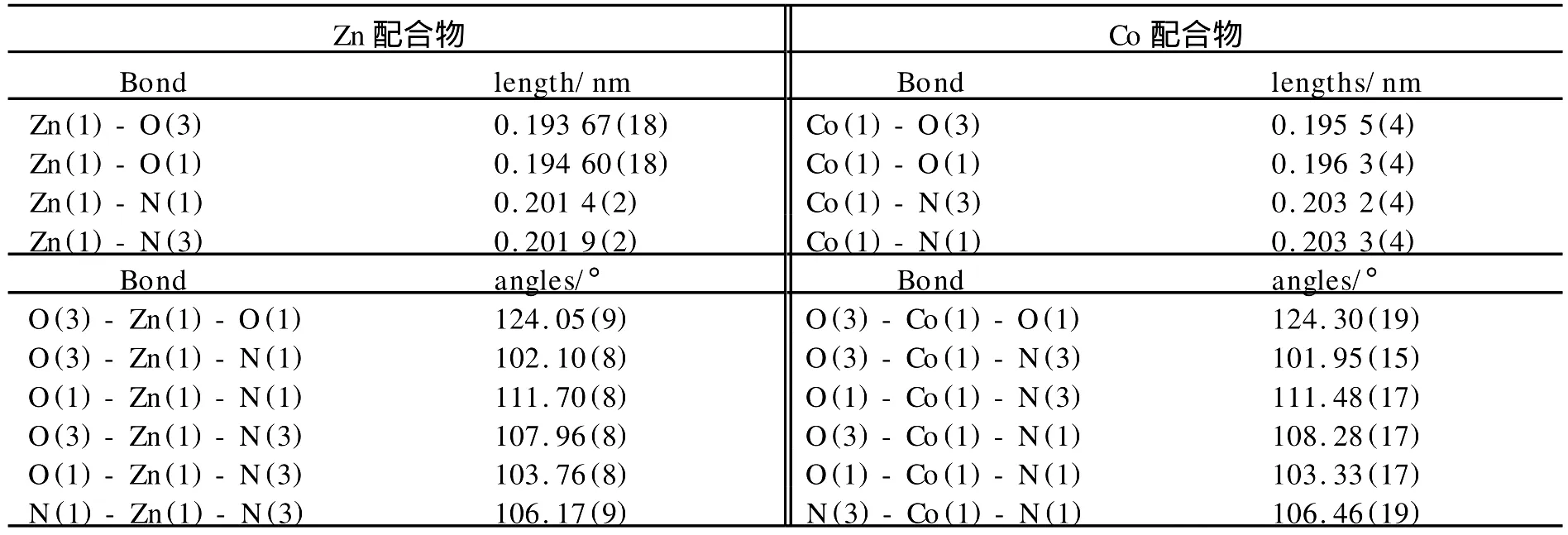
表2 配合物的部分键长和键角Table 2 Selected bond lengths and bond angles of the complexes

表3 Zn和Co配合物部分氢键键长和键角Table 3 Selected hydrogen bond lengths and bond angles of the complexes
2.3 Zn(Ⅱ)配合物的热分析
Zn(Ⅱ)配合物的 TG和DTG曲线如图3所示,配合物的热分解一步完成.Zn(Ⅱ)配合物在200℃以下稳定.200℃~600℃,2-氨基苯并噻唑及醋酸根配体全部失去,残余质量分数16.4%(理论值16.8%),热分解残余物为ZnO.
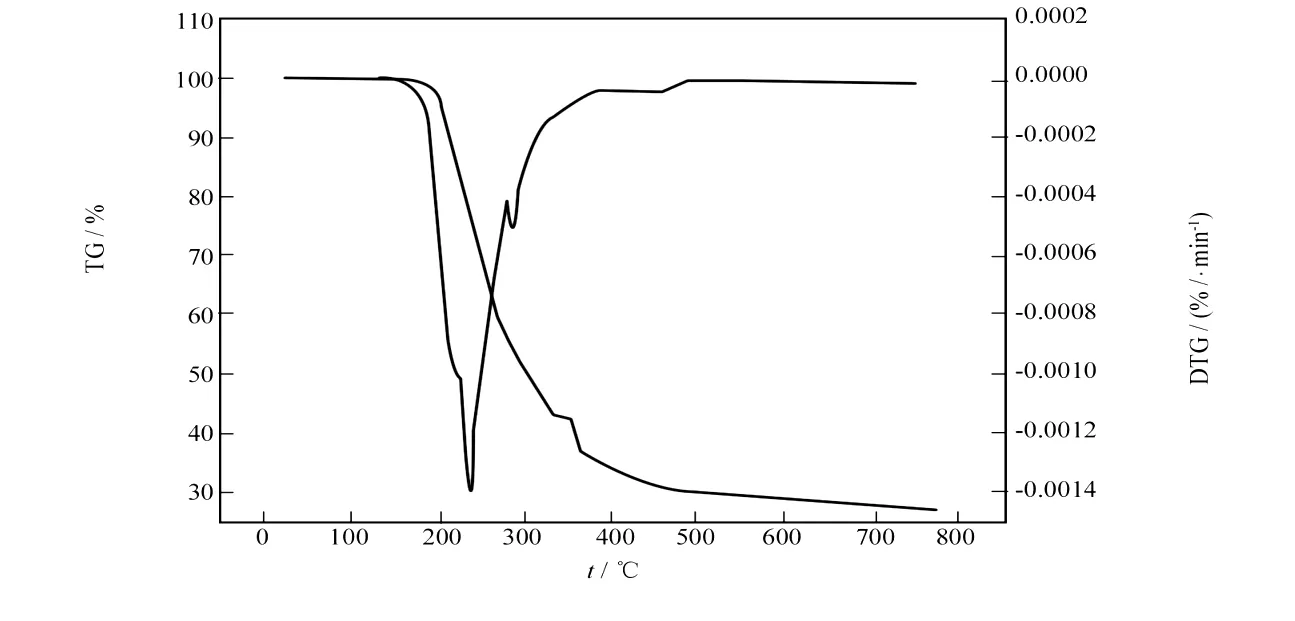
图3 Zn(Ⅱ)配合物的 TG-DTG曲线图Fig.3 TG-DTG curves of the Zn(Ⅱ)complex
2.4 抑菌活性分析
Zn(Ⅱ)和Co(Ⅱ)配合物对金黄色葡萄球菌、大肠杆菌和酵母菌抑制作用结果如表4所示.

表4 配合物对三种菌的抑制作用Table 4 Antibacterial activities of the complex to bacteria
以上数据表明,两种配合物对三种菌种均有不同程度的抑菌活性.Zn(Ⅱ)配合物对金黄色葡萄球菌和大肠杆菌的抑制活性分别低于青霉素钠和庆大霉素钠,对酵母菌的抑制活性略强于抗生素联苯苄唑;Co(Ⅱ)配合物对金黄色葡萄球菌的抑制活性与青霉素钠接近,对大肠杆菌及酵母菌的抑制活性分别优于庆大霉素钠和联苯苄唑,对酵母菌达到高度抑制.Zn(Ⅱ)配合物对酵母菌具有选择性抑制作用,Co(Ⅱ)配合物对大肠杆菌及酵母菌表现出良好的选择性抑制活性.
3 结论
合成了2-氨基苯并噻唑与钴和锌的两种金属配合物,利用红外光谱、元素分析、X射线单晶衍射和热重分析等对其结构进行了表征,抑菌实验表明两种配合物对三种菌种均有不同程度的抑菌活性.
[1]张思行,武现丽,戴志鹏,等.1,2,4-三唑双席夫碱衍生物的合成及表征 [J].有机化学,2008,28(6):1110-1114.
[2]胡卫兵,冯驸,刘红霞.2,4,7-三氨基芴席夫碱的合成及抗菌活性研究 [J].化学试剂,2008,30(6):449-450.
[3]孙国锋,孙晓红,陈邦,等.4-氨基-1,2,4-三唑-3-酮席夫碱合成及毒性 [J].西北大学学报,2002,32(6):647-650.
[4]张淑华,蒋毅民,陈美基.5-氯-N-(2-磺酸基乙基)水杨醛亚胺 Schiff碱的合成及表征 [J].广西师范大学学报,2004,22(2):60-62.
[5]陶艳,孙晓红,刘源发,等.三唑类席夫碱衍生物的研究新进展 [J].应用化工,2009,38(5):722-728.
[6]梁芳珍,郝京诚,黄汝骐,等.2-氨基噻唑缩水杨醛合Zn(Ⅱ)配合物的合成、表征及抑菌活性 [J].化学通报,1997,10:42-44.
[7]Zureima G H,Angelina F P.2-Aminobenzothiazole phosphorus amides:Molecular and supramolecular structures,hydrogen bonds and donor-acceptor interactions[J].Polyhedron,2006,25:1662-1672.
[8]Amnar V,Fun H K,Suchada C,et al.Diacetatobis(2-aminobenzothiazole)zinc(Ⅱ)[J].Acta Cryst E,2003:41-43.
[9]Sheldrick G M.SHELXTL-97.Version 5.1[CP].Bruker AXS Inc,Madison,Wisconsin,USA:1997.
[10]中本一雄.无机和配位化合物红外和拉曼光谱 [M].1997:257-258.
[11]Ren P,Su N B,Qin J G,et al.Synthesis,crystal structure and calculated value of a tetrahedral zinc(Ⅱ)complex-Zn(2-NH2py)2Br2[J].Chin J Struct Chem,2002,21(1):38-41.
Crystal Structure and Antibacterial Activity of 2-Amino-benzothiazole Complexes
SONG Shuang1,SONG Min2,ZHANG Huai-min1,YANG Li-rong1*
(1.Institute of Molecular and Crystal Engineering,College of Chemistry and Chemical Engineering,Henan University,Kaif eng475004,Henan,China; 2.College of Lif e Science,Henan University,Kaif eng475004,Henan,China)
Zinc and cobalt complexes with 2-aminobenzothiazole were synthesized.The chemical feature,composition and thermal stability of resultant complexes were analyzed by means of infrared spectrometry,elemental analysis,and thermogravimetry.The crystal structure of the complexes was determined by means of single crystal X-ray diffraction.Moreover,the antibacterial activities of the complexes against staphylococcus aureus,colibacillus and microzyme were evaluatedviainvitro activity testing.It was found that Zn(Ⅱ)and Co(Ⅱ)atoms were four-coordinated with two O atoms and two N atoms forming a distorted tetrahedral geometry.Both complexes had strong selective antibacterial activities against staphylococcus aureus,colibacillus and microzyme.
2-aminobenzothiazole;complex;crystal structure;antibacterial activity
O 641.4
A
1008-1011(2010)06-0021-05
2010-09-06.
河南省教育厅基金项目(2010B150005).
宋霜 (1987-),女,硕士生,主要从事功能配合物研究.*
,E-mail:lirongyang@henu.edu.cn.

