HPLC法测定蒲公英颗粒中咖啡酸含量
柯 薇
[摘要] 目的:建立高效液相色谱法测定蒲公英颗粒中咖啡酸含量的方法。方法:采用高效液相色谱法,色谱柱为Shim-Pack C18柱(250 mm×4.6 mm,5 μm);以甲醇-水-磷酸(100∶250∶0.1)为流动相;检测波长为320 nm;流速为1.2 ml/min。结果:咖啡酸在0.010 0~0.090 0 mg/ml范围内与峰面积呈良好的线性关系,平均回收率为98.6%,RSD=1.27%(n=6)。结论:本方法简便、快速、灵敏、准确、重现性好,可用于蒲公英颗粒的质量控制。
[关键词] HLPC;蒲公英颗粒;咖啡酸
[中图分类号] R927.2 [文献标识码]A [文章编号]1674-4721(2009)05(a)-005-02
Determination of caffeic acid in pugongying granules by HPLC
KE Wei
(Department of Pharmacy, the Third People's Hospital of Huaihua, Huaihua418000, China)
[Abstract] Objective: To establish a method for the determination of caffeic acid in Pugongying granules by HPLC. Methods: The analysis was carried on a column of Shim-Pack C18(250 mm×4.6 mm, 5 μm) with a mobile phase of methanol-water-phosphoric acid (100∶250∶0.1), and the UV detection wavelength was 320 nm. Rusults: The linear relation of caffeic acid was excellent within the range of 0.010 0~0.090 0 mg/ml (r=0.999 6, n=5), the mean recovery was 98.6% with RSD=1.27% (n=6). Conclusion: The method is simple, quick, sensitive, accurate, reproducible and can be control the quality of Pugongying granules.
[Key words] HLPC;Pugongying granules;Caffeic acid
蒲公英颗粒是由蒲公英加辅料蔗糖制成的颗粒剂,具有清热消炎的功效,用于治疗上呼吸道感染、急性扁桃体炎、疖肿、乳腺炎等,其主要有效成分为咖啡酸。目前有关蒲公英颗粒质量标准仅包括性状、检查、鉴别、浸出物四项,但无定量研究[1-2]。为了提高蒲公英颗粒产品质量控制水平,本文采用高效液相色谱(HPLC)法测定蒲公英颗粒咖啡酸的含量,为蒲公英颗粒的质量标准控制提供理论依据。

1仪器与试药
汉邦高效液相色谱仪 SSI/ Lab Alliance(美国科学系统公司),型号:Series Ⅲ; Model 500型紫外检测器;7725i型进样阀;LGC-1025M型柱温箱;N2000化学工作站;HS3120D型超声仪;电子天平[AL104梅特勒-托利多仪器(上海)有限公司]。咖啡酸对照品(中国药品生物制品检定所,批号为110885-200102);蒲公英颗粒(四川省中药厂有限责任公司,批号:03090,国药准字Z51020895);试验用水为超纯水;甲醇为色谱纯(天津四友生
物医学技术有限公司),磷酸二氢钾、甲酸、磷酸等均为分析纯。
2方法与结果
2.1色谱分析条件及系统适用性试验
色谱柱:Shim-Pack C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水-磷酸(100∶250∶0.1);检测波长:320 nm;流速:1.2 ml/min;柱温:40℃;进样量:20 μl。理论板数按咖啡酸峰计算应不低于6 000。
2.2溶液的制备
对照品溶液的制备:精密称取咖啡酸对照品0.005 0 g,置100 ml棕色容量瓶中,加甲醇适量,使之溶解,再加甲醇至刻度,即得。供试品溶液的制备:取本品研细,精密称取3.671 3 g,置100 ml具塞锥形瓶中,加盐酸0.3 ml,加水30 ml,加热使溶解,用乙醚-乙醇(24∶1)混合溶液萃取4次,每次15 ml,用无水硫酸钠脱水,合并,低温蒸干,残渣加流动相甲醇-水-磷酸(100∶250∶0.1)溶解,置棕色瓶中,并定容至5 ml。用0.45 μm微孔滤膜滤过,取续滤液,即得。阴性对照品溶液的制备:按处方量称取除蒲公英外的阴性样品,照供试品溶液项下操作制成。
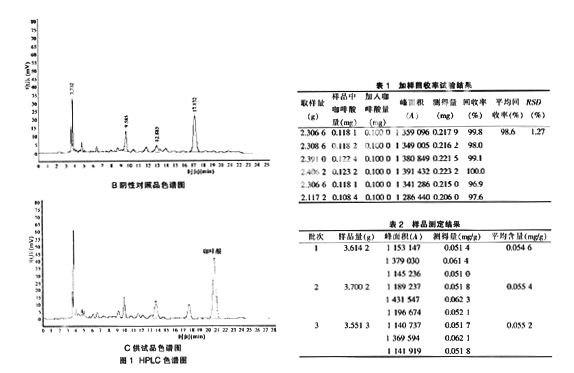
2.3方法学考察
2.3.1干扰试验在上述色谱条件下,取对照品、供试品和阴性对照品溶液各20 μl进样。结果在对照品色谱峰保留时间相应的位置上,阴性对照品溶液在此峰位无吸收,对样品的测定无干扰,分离良好,见图1。
2.3.2 线性关系考察精密称取咖啡酸对照品0.010 0 g,置100 ml棕色容量瓶中,加甲醇适量使之溶解,加甲醇至刻度,摇匀,配成浓度为0.100 0 mg/ml的溶液,分别精密吸取咖啡酸甲醇溶液1.0、3.0、5.0、7.0、9.0 ml分别置10 ml容量瓶中,用甲醇稀释至刻度,摇匀,配成浓度分别为0.010 0、0.030 0、0.050 0、0.070 0、0.090 0 mg/ml的溶液。按前面所述色谱条件,分别精密吸取20 μl注入液相色谱仪,记录色谱图,以对照品溶液浓度(C)为纵坐标,以峰面积(A)为横坐标,得回归方程C=3.28×10-8A-0.001,r=0.999 6(n=5)。结果表明咖啡酸在0.010 0~0.090 0 mg/ml范围内,与峰面积呈良好的线性关系。
2.3.3 精密度试验取线性试验中浓度为0.050 0 mg/ml的咖啡酸对照品溶液,精密吸取20 μl注入液相色谱仪,连续进样6次,得咖啡酸的峰面积计算RSD=0.83%,结果表明本实验精密度良好。
2.3.4 稳定性试验 取同一供试品溶液,分别在0、2、4、6、8 h精密吸取20 μl注入液相色谱仪,测定其峰面积,无显著变化,并计算RSD=1.76%,表明本品溶液在8 h内测定。
2.3.5重现性试验取同一批新生化颗粒样品适量,照供试品溶液的制备方法制备各供试品溶液,分别取20 μl注入液相色谱仪,由峰面积按外标法计算含量,并由含量计算RSD=0.83%,表明本实验结果重现性较好。
2.3.6加样回收率试验精密称取已测含量的样品细粉适量,置100 ml具塞锥形瓶中,加入咖啡酸对照品溶液1 ml(0.100 0 mg/ml),加盐酸0.3 ml,加水30 ml,加热使之溶解,用乙醚-乙醇(24∶1)混合溶液萃取4次,每次15 ml,用无水硫酸钠脱水,合并,低温蒸干,残渣加流动相甲醇-水-磷酸(100∶250∶0.1)溶解,置棕色瓶中,并定容至5 ml,用0.45 μm微孔滤膜滤过,取续滤液,即得。精密吸取20 μl注入液相色谱仪,将测得峰面积代入线性方程,计算供试品中咖啡酸的含量,并计算回收率。结果见表1。
3 讨论
蒲公英颗粒是常用的清热解毒中药,用于咽喉肿痛(急性扁桃体炎)疮疖,乳痈发热,也可用于热淋。现代药学及药理研究表明, 蒲公英所含的咖啡酸具有广谱抗菌和消炎利胆作用。体外试验表明, 蒲公英对金黄色葡萄球菌、变形杆菌、甲型链球菌、乙型链球菌均有明显的抑制作用[3]。因此,本研究将咖啡酸作为蒲公英颗粒质量控制的指标是可行的。
国家食品药品监督管理局部颁中药第三册中收载的《蒲公英颗粒质量标准》对含量未作要求,这对控制药品质量和保障人民用药安全十分不利。为了保证产品质量的均一性和临床用药的安全性及有效性,笔者在对蒲公英颗粒质量研究的基础上制定了蒲公英片中咖啡酸的含量限度[4]。
通过上述研究,建立了蒲公英片剂的定量测定方法,本研究结果表明该法方便、快速、准确,为制剂的质量控制提供了实验依据。该法可用于蒲公英片的质量标准和质量控制,为全面控制产品质量提供了方法。
[参考文献]
[1]国家药典委员会.中华人民共和国药典·一部[M].北京:化学工业出版社,2005:28.
[2]都述虎,金继曙.蒲公英中咖啡酸的含量测定研究[J].中国现代应用药学,2001,18(1):59-60.
[3]陈勇,程智勇,韩凤梅,等.蒲公英注射液的质量探讨[J].湖北大学学报,2000,22(3):278-281.
[4]张旭东,张淑惠,张西如.反相高效液相色谱法测定蒲公英中咖啡酸的含量[J].中国现代药学杂志,2003,20(6):511-512.
(收稿日期:2009-03-06)

