Fenton及臭氧氧化法处理苯胺污染地下水的对比
宋立杰
(上海市环境工程设计科学研究院有限公司,上海 200232)
苯胺是水体的主要污染物之一,主要来源于印染、制药及石油化工企业[1]。苯胺在血液中极易发生反应,可与血红蛋白结合生成高铁血红蛋白,阻止氧气的吸收和传递,因此,具有很强的生物毒性[2-3]。另外,苯胺属于难生物降解的有机物,可抑制微生物的生长,在自然水体中很难被微生物降解去除。苯胺污染地下水体需要进行化学法深度处理[4]。
在去除水中难降解有机物方面,高级氧化技术因其良好的处理效果受到了越来越多的关注。电化学法、Fenton反应、臭氧氧化法及光催化法等为常见的高级氧化方法。Fenton反应由于反应条件温和、设备简单、适用范围广等优点得到广泛应用。该反应是通过H2O2和催化剂反应生成大量的·OH,从而矿化水中的有机物,实现有机污染物的去除。研究表明,Fenton反应可以有效去除水中的苯胺[5],但存在反应pH范围窄、产生铁泥的缺点。臭氧是一种具有较高氧化还原电位的强氧化剂。研究表明,臭氧可以和芳香环中的电子对发生反应,同时,臭氧生成的·OH可以攻击苯胺的氨基部位,因此对水中苯胺有一定的去除效果[6-8]。
本研究考察Fenton和臭氧氧化法处理苯胺污染地下水的处理效果,优化了2种氧化处理的工艺参数,分析了苯胺的代谢途径,并从苯胺去除效率和处理成本两方面对Fenton和臭氧氧化工艺的处理效果进行了比较,为受苯胺污染地下水的治理和修复提供理论和技术选择。
1 材料与方法
1.1 试验用水
试验用污染原水取自上海某工业区受污染地块,TOC、苯胺和腐殖质的浓度如表1所示。

表1 试验原水水质Tab.1 Raw Water Quality for the Experiment
1.2 试验装置和方法
(1)Fenton试验:各取250 mL地下水分别置于4个锥形瓶中,采用2 mol/L硫酸溶液将水样pH值调节至2、3、4、5后,向锥形瓶中加入50、150、200、250 mmol/L H2O2,按照Fe2+和H2O2摩尔比为2∶1、1∶1、1∶3和1∶5投加FeSO4,在室温下放在六联磁力搅拌器上,以40 r/min搅拌强度慢速搅拌30 min。反应结束后,8 000 r/min离心5 min,取上清液待测。
(2)臭氧试验:采用微气泡臭氧法进行间歇性反应试验。反应器为直径55 mm、高85 mm的圆柱体,反应器底部装纯钛曝气头,孔径为0.2 μm。臭氧反应器采用青岛国林生产的小型反应器(10 kg/h臭氧发生器),装置如图1所示。试验过程中,臭氧浓度为45 mg/L,进气量为300 mL/min。在反应器内加入200 mL地下水,采用2 mol/L硫酸和氢氧化钠溶液调节水样pH值为5、7、9,在反应时间为0、5、15、20、25 min时取水样,分析测定TOC、苯胺等指标。
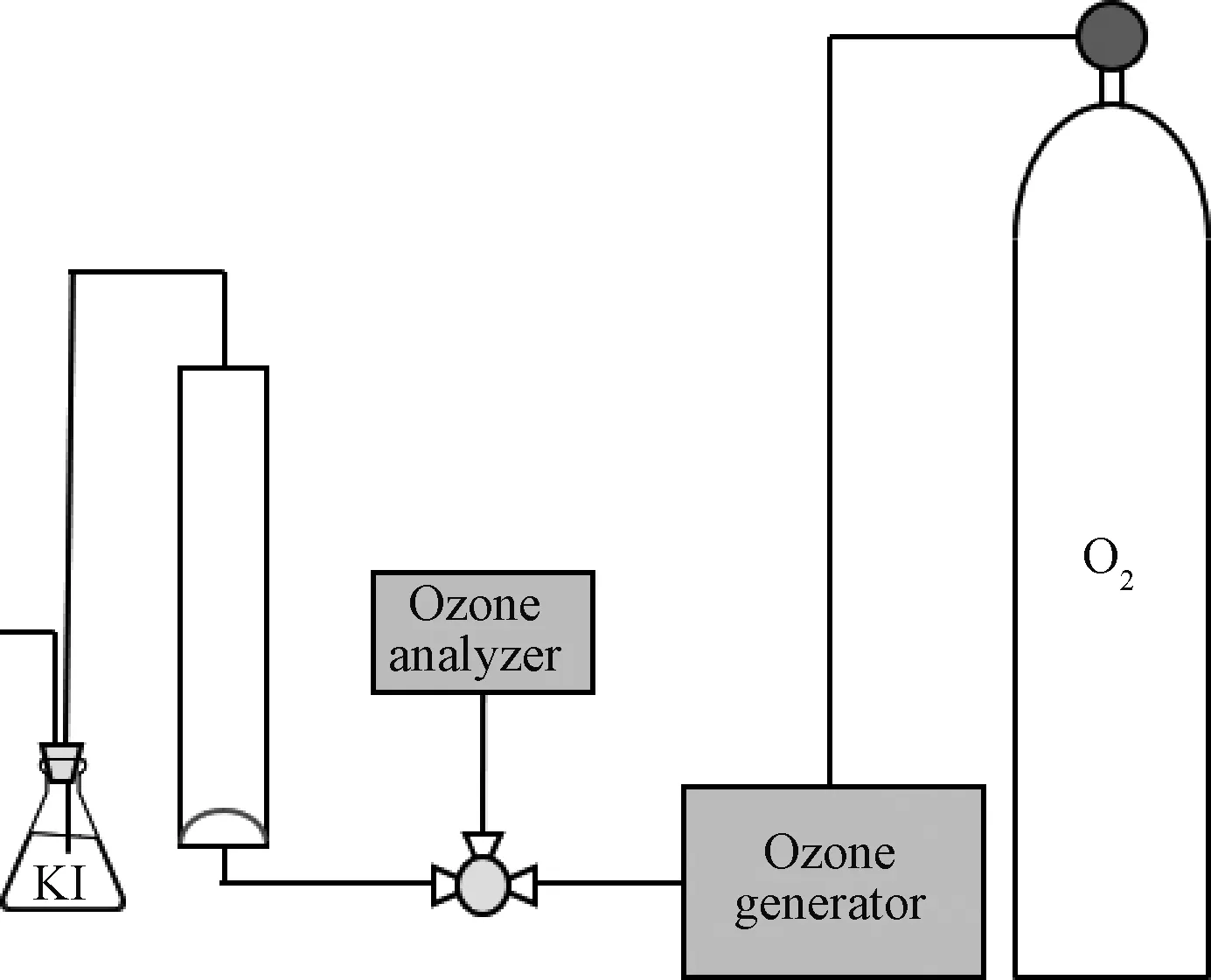
图1 臭氧处理装置Fig.1 Experimental Equipment for Ozonation
1.3 分析方法
TOC浓度由TOC测定仪OI 1030燃烧法检测。苯胺及其代谢产物通过安捷伦7890B-7000D三重四级杆质谱联用仪进行检测。GC以10 ℃/min升温至250 ℃。载气为氦气,流速恒定为1.5 mL/min。采用70 eV电离能进行电子电离,扫描速度为500 amu/s。
2 结果与讨论
2.1 Fenton反应对苯胺的处理效果
2.1.1 初始pH的影响
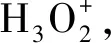
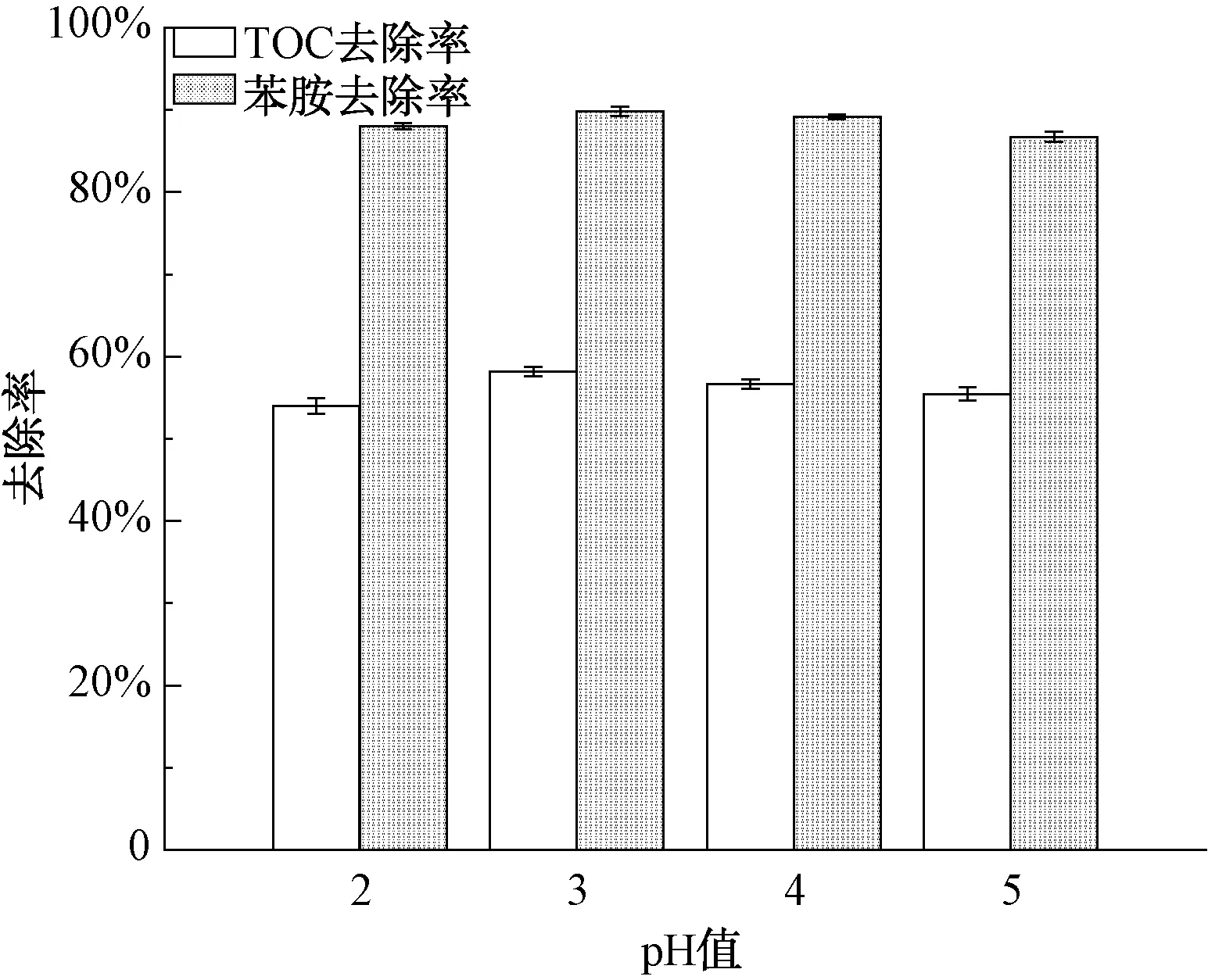
图2 初始pH值对Fenton处理效果的影响Fig.2 Effects of Initial pH Value on the Degradation of Aniline and TOC by Fenton
2.1.2 H2O2投加量的影响
Fenton氧化降解受污染水中有机物的反应中,H2O2的投加量决定了实际应用时的治理成本[9]。在初始pH值为3、Fe2+和H2O2的摩尔比为1∶3时,分别投加100、200、300、400 mmol/L的H2O2,反应30 min,TOC及苯胺的去除率如图3所示。由图3可知,随着H2O2浓度的增加,水样中有机物的去除率呈现先增加后降低的趋势,这表明H2O2在催化氧化水样中有机物时具有双重作用。当H2O2浓度较低时,增加其浓度可以增加·OH的浓度,从而实现强化有机物的去除效率;当H2O2浓度增加至一定程度后,H2O2反而会成为·OH的清除剂,生成过氧化·OH,降低氧化性能。总体来看,最佳H2O2的投加量为300 mmol/L,水样中TOC和苯胺的浓度分别从169.96 mg/L和24.69 mg/L降至66.01 mg/L和2.20 mg/L,去除率分别为61.16%和91.09%。
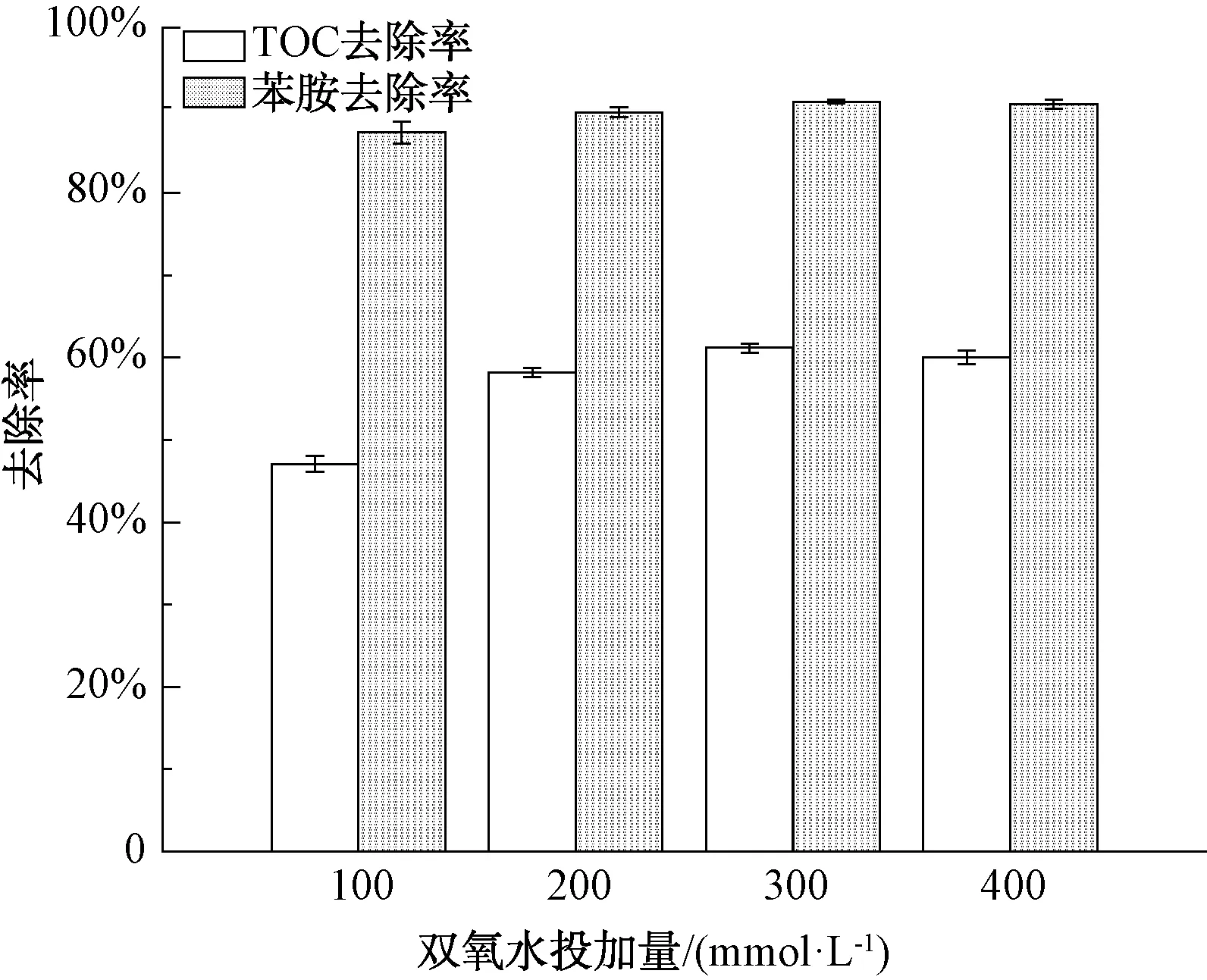
图3 H2O2投加量对Fenton处理效果的影响Fig.3 Effects of H2O2 Concentration on the Degradation of Aniline and TOC by Fenton
2.1.3 Fe2+∶H2O2摩尔比的影响
在Fenton反应过程中,Fe2+是H2O2生成·OH的催化剂,对Fenton催化氧化有机物效果有很大的影响。在初始pH值为3、H2O2的投加量为300 mmol/L时,按照Fe2+和H2O2的摩尔比为2∶1、1∶1、1∶3和1∶5投加FeSO4溶液,反应30 min,TOC及苯胺的去除率如图4所示。结果表明,随着Fe2+投加量的增加,水样中有机物的去除率呈现先增加后降低的趋势。当Fe2+和H2O2的摩尔比为1∶3时,水中剩余有机物最少,TOC和苯胺浓度分别从169.96 mg/L和24.69 mg/L降至为71.97 mg/L和4.23 mg/L,去除率分别为57.65%和82.87%。这是因为,当Fe2+浓度低时,随着Fe2+浓度升高,H2O2产生的·OH增加,而当Fe2+的浓度过高时,H2O2发生无效分解,释放出O2,同时也会同·OH反应生成Fe3+。
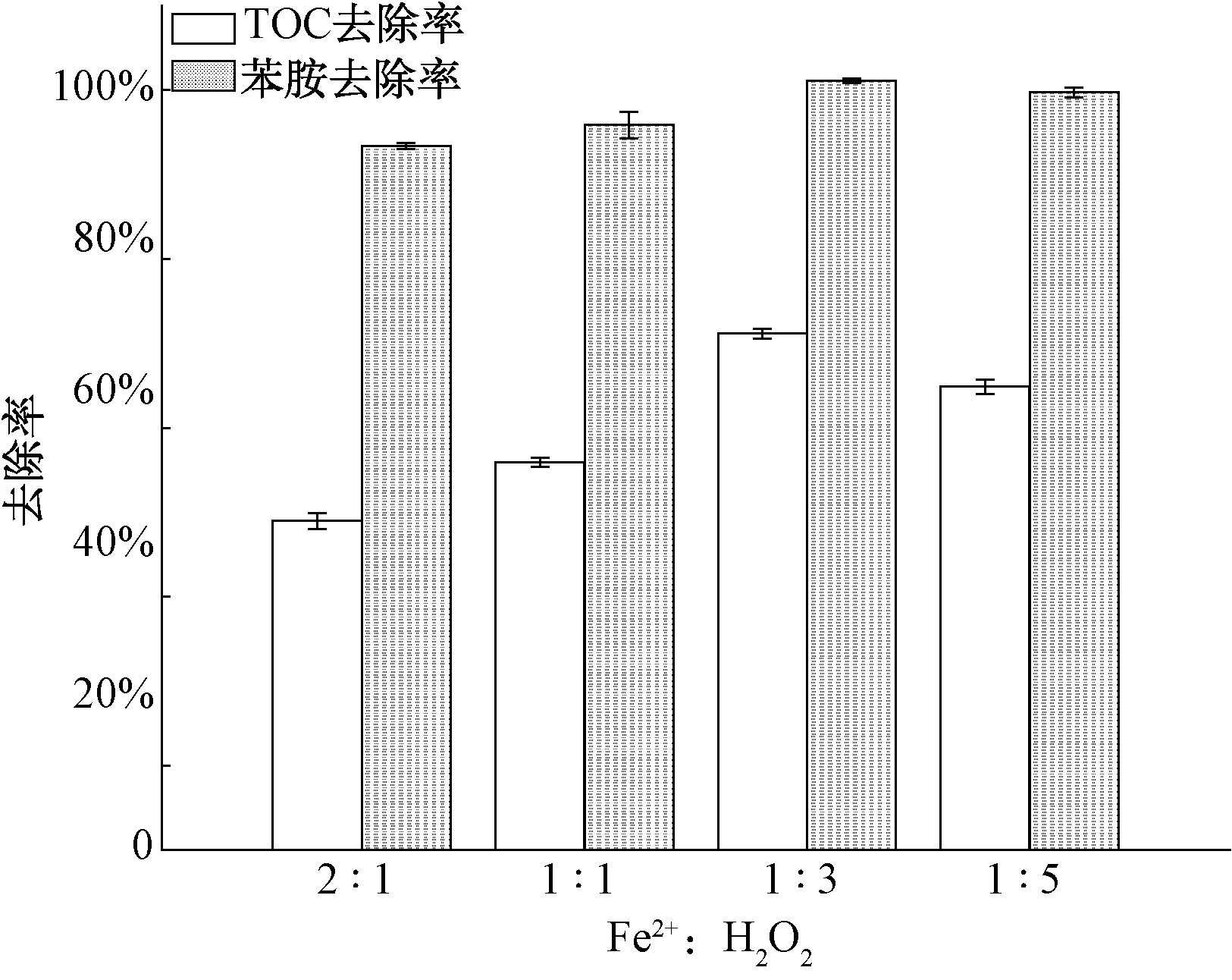
图4 Fe2+∶H2O2 摩尔比对Fenton处理效果的影响Fig.4 Effects of Molar Ratios of Fe2+ and H2O2 on the Degradation of Aniline and TOC by Fenton
2.2 臭氧对苯胺的处理效果
2.2.1 初始pH的影响
在不同pH条件下,臭氧对有机物的氧化存在直接氧化和自由基氧化两种途径[10]。在臭氧浓度为60 mg/L、进气量为1 L/min、臭氧通入量为450 mg/L、反应体系初始pH值分别为5、7和9时,臭氧氧化对污染物的去除效果如图5所示。由图5可知,当其他工艺参数保持不变的情况下,水样初始pH对有机物的去除效果有着重要的影响,TOC的去除率随着pH的升高而增大,在51.42%~64.13%。然而,从苯胺的去除率来看,在不同初始pH时,苯胺的去除率均在95%以上,无明显差异。根据文献[6-8,10],酸性条件下,臭氧在水中主要以臭氧分子形式存在,臭氧分子易与不饱和的芳香、脂肪化合物以及一些含有特殊基团的化合物如酚类、胺类等发生亲电取代反应或偶极加成反应,与含有氯、硝基、羧基等取代基团的难降解污染物几乎不反应,是一种有选择性的直接氧化反应;碱性条件下,OH-与臭氧反应生成·OH,·OH与有机物发生加成反应或夺电子反应,实现对有机物的降解和矿化,是一种非选择性的间接氧化反应。这与本研究的结果一致,碱性条件下生成的具有强氧化性的·OH,不仅能氧化苯胺,还能降解苯胺分解产生的中间产物,pH值为9时,TOC和苯胺都有很高的去除率;但在酸性条件下,臭氧分子选择性地与苯胺发生反应,对中间产物作用不大,从而对苯胺的去除率影响不大,但TOC的去除率降低。因此,初始pH为碱性时更有利于有机污染物的完全降解。
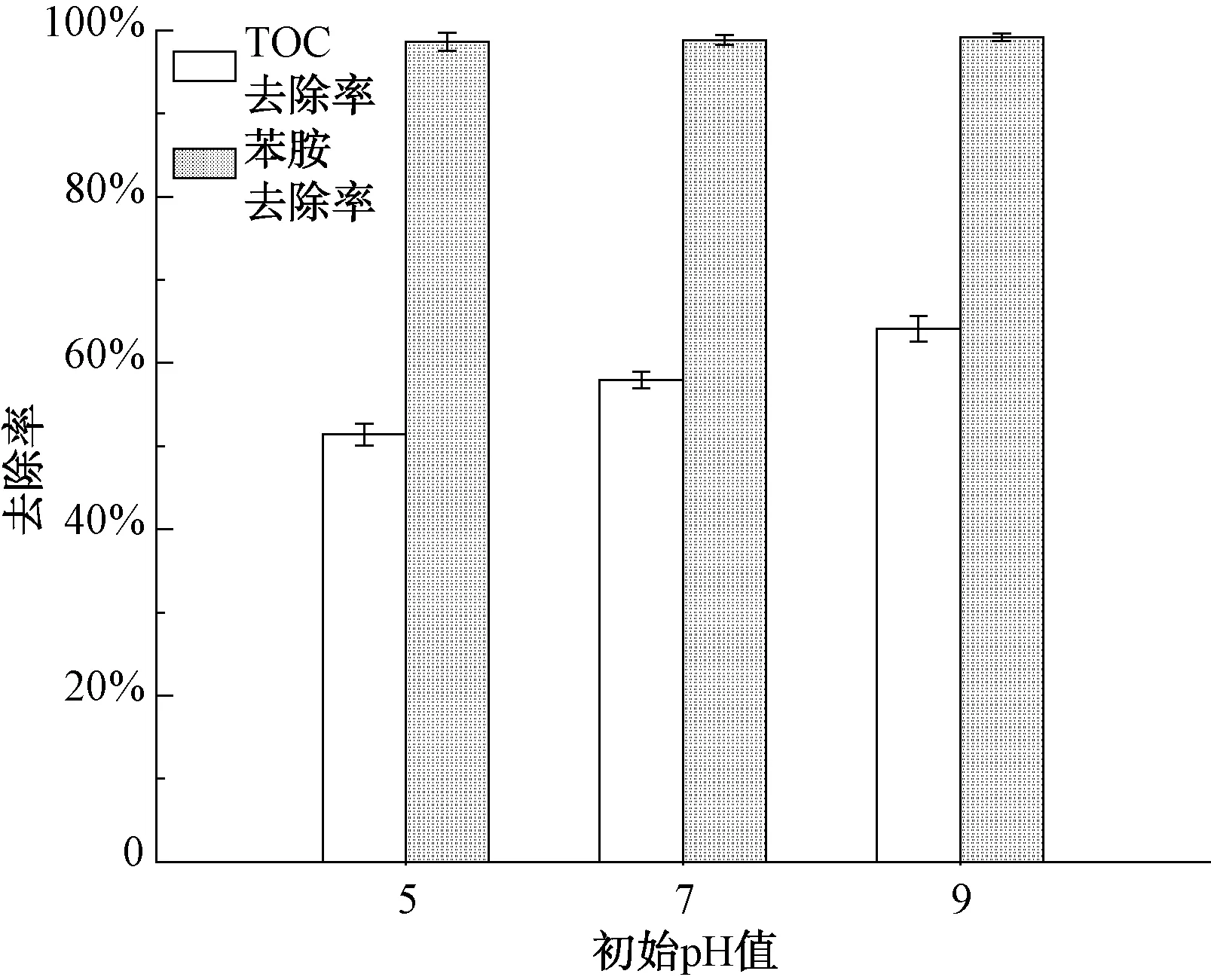
图5 初始pH值对臭氧处理效果的影响Fig.5 Effects of Initial pH Value on the Degradation of Aniline and TOC by Ozonation
2.2.2 曝气速率和进气中臭氧浓度的影响
在臭氧法处理水中有机污染物时,曝气速率及进气中臭氧浓度决定了水中溶解臭氧的浓度。在不控制水样pH、臭氧通入量为450 mg/L时,考察进气中臭氧浓度为30、60、90 mg/L,曝气量为0.25、0.5、1、2 L/min条件下,对有机污染物的去除效果,结果如图6所示。由图6可知:当其他参数维持不变的情况下,随着曝气速率的增加,有机污染物的去除率呈现先增加后降低的趋势;随着进气中臭氧浓度的增加,有机污染物的去除率也增大。
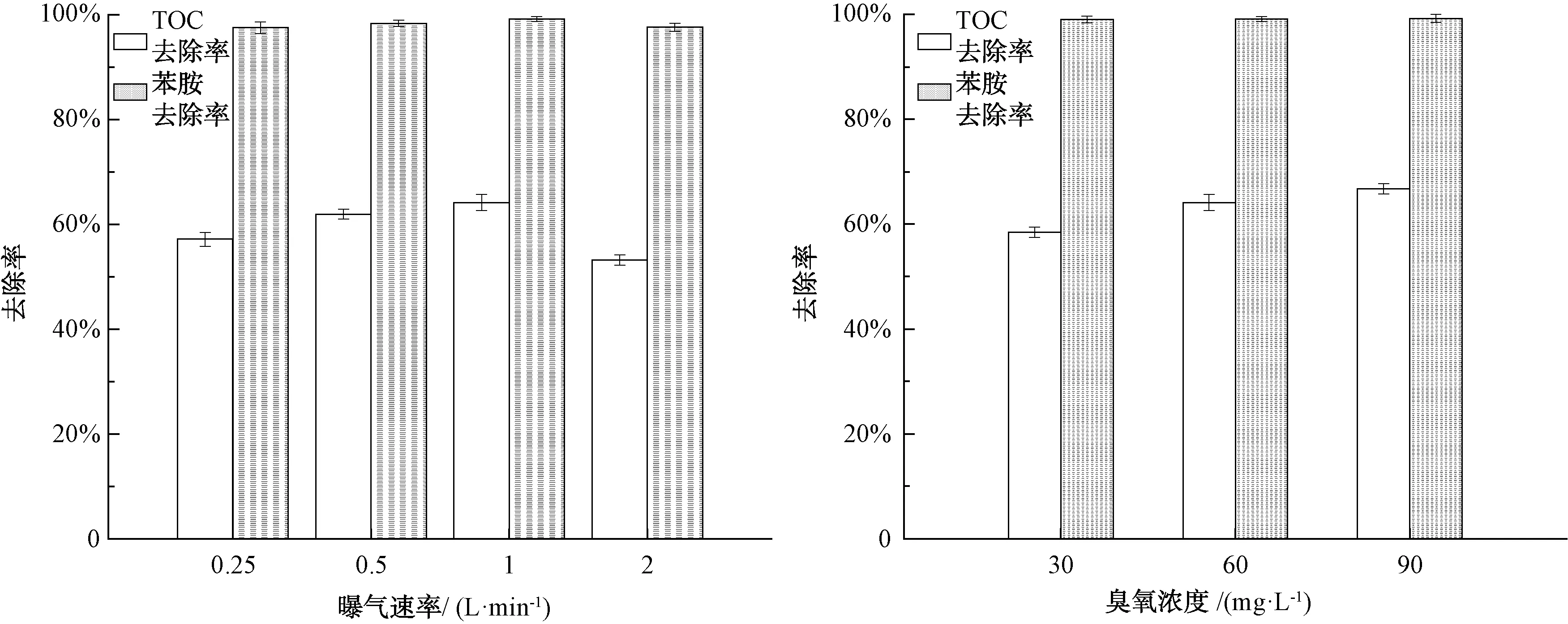
图6 曝气速率和进气中臭氧浓度对臭氧处理效果的影响Fig.6 Effects of Aeration Rate and Ozone Concentration in Air Inflow on the Degradation of Aniline and TOC by Ozone
在本试验过程中,臭氧装置内未设置搅拌装置,当曝气速率增加时,曝气扰动对水样的搅拌作用加强,强化了臭氧对有机污染物的去除效果。当曝气速率增加到2 L/min后,过高的气体流速导致臭氧在水中的停留时间过短,臭氧由气相进入液相的效率降低,导致臭氧的利用率大大降低。因此,在相同臭氧投加量的情况下,有机污染物的去除率降低。对于苯胺来说,曝气速率对其去除效果无明显影响。增大进气中臭氧浓度可以促进臭氧从气相传递至液相,从而提高有机物的去除效率。然而,单纯地提高气相中的臭氧浓度并不会使水中溶解的臭氧量线性增加,且当水中的臭氧浓度超过一定值后,过多的·OH会发生自猝灭,从而使臭氧的利用率降低。当臭氧浓度从30 mg/L增加至60 mg/L时,TOC去除率由58.45%提高至64.13%。但是,当臭氧浓度增加至90 mg/L时,TOC去除率为66.78%,仅提高了2.65%。因此,在本试验中,曝气速率为1 L/min,进气中臭氧浓度为60 mg /L为最佳值。
2.2.3 臭氧投加量的影响
在不控制水样pH、曝气量为1 L/min,臭氧浓度为60 mg/L,臭氧通入量为0、90、270、360、450 mg/L时,臭氧氧化后污染物的去除效果如图7所示。由图7可知,当其他参数维持不变的情况下,随着臭氧投加量的增加,水样中有机污染物的去除率呈上升趋势。在臭氧投加量为270 mg/L时,苯胺去除率达到94%,而TOC的去除率只有46.29%。当臭氧投加量为360 mg/L时,TOC和苯胺的去除率分别达到60.95%和99.15%。
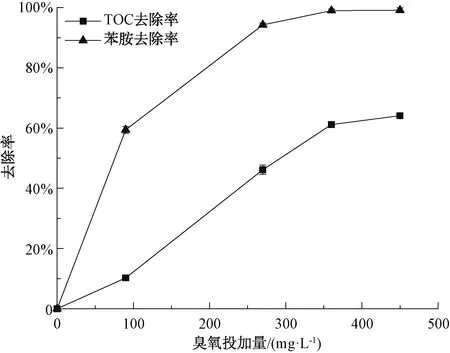
图7 臭氧投加量对臭氧处理效果的影响Fig.7 Effects of Ozone Dosage on the Degradation of Aniline and TOC by Ozone
苯胺与臭氧的·OH反应速率常数较其中间产物要高,水中的氧化剂优先与苯胺反应,因而,臭氧氧化前期,苯胺浓度降低很快,而TOC浓度变化较低。随着反应的进行,中间产物进一步矿化成小分子物质,TOC去除率大大增加。当臭氧投加量由360 mg/L增加至450 mg/L时,水样中有机物的剩余浓度基本维持一致。受污染水样中存在一定量的腐植酸类物质,臭氧对其氧化处理效果不佳,因此,进一步增加臭氧投加量对有机物的去除效果提升不大。综合TOC及目标污染物去除效果,选择最佳臭氧投加量为360 mg/L。
2.3 Fenton及臭氧氧化法对苯胺的处理效果比较分析
在由2.1及2.2得到的最佳Fenton和臭氧处理工艺条件下,对二者处理苯胺污染地下水效果进行比较分析。从苯胺的处理效果来看,臭氧比Fenton的去除率高。臭氧处理对苯胺的去除率可以达到99%以上,比Fenton反应高8%左右,而TOC去除率高3%左右。Fenton反应过程中,水样中苯酚主要依靠H2O2与Fe2+反应生成的·OH氧化去除,提高Fenton试剂的投加量可以强化苯胺的去除。然而,当H2O2浓度达到一定程度后,H2O2与苯胺形成竞争关系,阻碍了苯胺的去除。在臭氧反应过程中,臭氧分子及臭氧生成的·OH均可以与苯胺发生反应,从而强化了对水样中苯胺的去除效果。臭氧分子对苯胺分解后中间产物的矿化程度不高,因此,对于TOC的去除率,臭氧及Fenton反应基本相同。从成本角度分析,H2O2投加量为300 mmol/L,Fe2+投加量为100 mmol/L,FeSO4的价格及H2O2的价格按照130元/t和1 000元/t计算,Fenton氧化法处理每t苯胺污染地下水的成本为13.81元。臭氧处理中,最佳投加量为360 mg/L、功率为12 kW·h的工业臭氧发生器的臭氧产量为1 kg/h,电费按照0.6元/(kW·h)计算,则处理每t受污染地下水费用为2.59元。因此,与Fenton反应相比,臭氧处理具有更低的处理成本和更高的去除效率。
2.4 反应机理分析
Fenton及臭氧氧化反应过程中,苯胺降解中间产物通过GC-MS分析,结果如图8所示。因为本试验采用原水进行,含腐植酸、小分子有机物等多种物质,2种氧化处理结果的GC图中出现许多物质的峰。通过文献查找,图谱中与苯胺氧化相关的中间产物为硝基苯,其MS图谱如图8上方小图框所示。具体反应过程:在Fenton试验及碱性条件下,臭氧氧化均是以·OH为氧化主体;氨基中的H原子被具有较高电子亲和能力的·OH吸引,从而发生夺氢反应;苯胺在氨基失去H原子后会生成亚胺醌和羟基苯胺,并在氧化剂的氧化作用下迅速生成硝基苯,进而生成对苯醌,最终矿化为CO2和H2O[11-12]。在Fenton和臭氧处理过程中,观察到水样颜色由无色到棕红色至浅红色的转化,这和硝基苯浓度的先增加后降低有着密切关系。结合文献报道,推断苯胺氧化降解的可能途径如图9所示[8]。

图8 GC-MS图谱Fig.8 GC-MS Spectrum
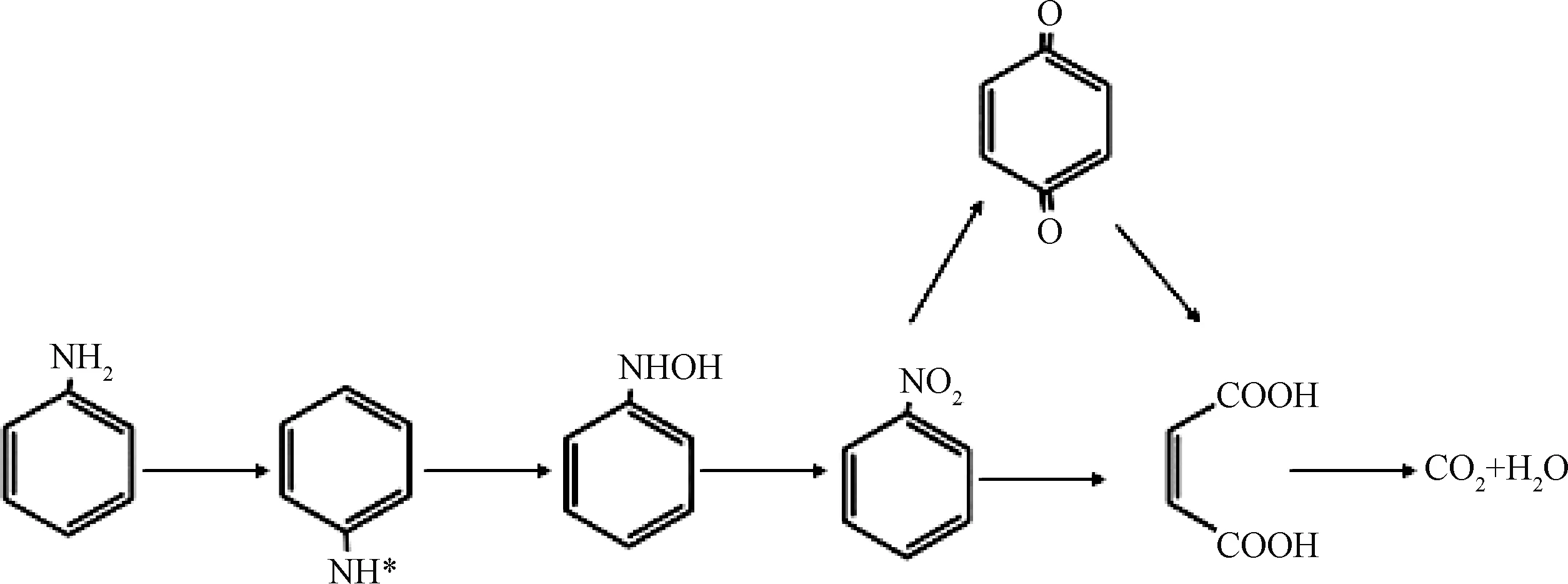
图9 氧化处理过程中苯胺降解机理Fig.9 Aniline Degradation Mechanism in Process of Oxidation
3 结论
针对苯胺污染地下水的异位修复问题,以TOC及苯胺的去除率为指标,对Fenton及臭氧氧化2种方法进行了对比研究。对Fenton及臭氧反应过程中,初始pH、H2O2投加量、Fe2+和H2O2的摩尔比、臭氧浓度、曝气速率及臭氧投加量等参数进行了优化,并对其降解途径进行了探讨,得出的主要结论如下。
(1)Fenton试验去除苯胺的最佳试验条件:当初始pH值为3.0、H2O2投加量为300 mmol/L、Fe2+和H2O2的摩尔比为1∶3时,苯胺的去除率可以达到91.07%。
(2)臭氧试验去除苯胺的最佳试验条件:当初始pH值为9、曝气速率为1 L/min、臭氧的投加量为360 mg/L、进气中臭氧浓度为60 mg/L时,苯胺的去除率可以达到99.15%。
(3)臭氧反应比Fenton反应有着更好的苯胺去除效率,但是,对苯胺的矿化效果,两者基本相同。
(4)Fenton反应及碱性条件下,臭氧反应过程中,硝基苯为苯胺氧化过程中的主要中间产物。

