胺化羧甲基改性磁性壳聚糖的制备及吸附性能研究
崔丽,陈一新,梁吉艳,王新,王慧,孙晓航
(沈阳工业大学化学与环境系,辽宁沈阳110870)
胺化羧甲基改性磁性壳聚糖的制备及吸附性能研究
崔丽,陈一新,梁吉艳,王新,王慧,孙晓航
(沈阳工业大学化学与环境系,辽宁沈阳110870)
采用交联法制备了磁性壳聚糖,并在此基础上使用柠檬酸及二乙烯三胺对其进行化学改性,得到了磁性能良好、颗粒分布均匀、平均孔径为4.37 nm的胺化羧甲基改性磁性壳聚糖。将其用于模拟废水中进行静态吸附实验。结果表明,改性后的磁性壳聚糖在保证机械强度与回收率的基础上,提高了磁性壳聚糖的吸附性能,在最适pH= 6的条件下,对Cu2+、Cd2+、Ni2+的吸附容量分别达到76.82、54.15、62.64mg/g。
磁性壳聚糖;化学改性;吸附
壳聚糖是甲壳素的脱乙酰化产物,是一种比活性炭更廉价,环境友好型的天然无毒高分子吸附剂,是水处理领域的研究热点之一。但是壳聚糖在实际应用中也存在不足,它受限于废水的酸碱度,从而造成吸附剂流失并且不易进行快速分离回收。近年来学者们将具有磁响应性的Fe3O4和壳聚糖复合制备出磁性壳聚糖微球,这使得壳聚糖在水处理领域的应用前景更加广阔〔1-3〕。
磁性壳聚糖微球不仅提高了吸附剂的稳定性〔4-6〕,同时还具备快速分离回收的特点,然而在其制备过程中,由于壳聚糖分子链上对重金属离子具有稳定配位作用的部分—NH2和—OH被交联剂占据,因而相比壳聚糖,磁性壳聚糖对多种金属离子的选择吸附性能有所下降〔7-9〕。为此,笔者在保证磁性壳聚糖磁性能的前提下,通过加入柠檬酸和二乙烯三胺对其进行交联改性,制备出一种性能更优良的胺化羧甲基改性磁性壳聚糖,提高了吸附性能。
1 材料与方法
1.1 材料
壳聚糖粉末,脱乙酰度95%;Fe3O4粉末,纳米级;柠檬酸;二乙烯三胺;液体石蜡;Span-80;戊二醛,质量分数25.0%~27.0%;冰乙酸,质量分数≥99.5%;氢氧化钠;乙醇,质量分数≥99.7%;盐酸,质量分数36%~38%。实验所用试剂均为分析纯。
1.2 仪器
novAA®400P原子吸收分光光度计,德国耶拿分析仪器股份公司;WSZ-100调速多用振荡器,哈尔滨东明医疗仪器厂;501超级恒温水浴锅,上海市实验仪器厂;D-8401W多功能磁力搅拌器,天津市华兴科学仪器厂;SEM扫描电子显微镜,德国卡尔蔡司公司;V-Sorb2800比表面积及孔径分析测试仪,北京金埃普科技有限公司;WQF-410傅里叶变换红外光谱仪,日本岛津公司;DZF6000真空干燥
箱,上海精密仪器仪表有限公司;BS223S电子天平,北京赛多利斯天平有限公司。
1.3 实验方法
1.3.1 磁性壳聚糖的制备
取0.5 g壳聚糖置于烧杯中,加入质量分数为2%的醋酸溶液20mL,加热溶解2 h后形成水相,之后加入一定量的Fe3O4〔10〕,并对该溶液进行超声分散。分别将50mL液体石蜡与一定量的Span-80加入到经超声分散后的溶液中,在恒温水浴升温至60℃、快速机械搅拌的条件下加入戊二醛交联剂,用氢氧化钠调节溶液pH在9~11,继续恒温水浴反应2 h,得到磁性壳聚糖微球溶液。用磁铁将微球与溶液分离,再用去离子水、无水乙醇洗涤微球至滤出液为中性,抽滤,70℃下置于真空干燥箱干燥24 h,制得磁性壳聚糖微球。将制得的磁性壳聚糖微球研磨成粉后,真空保存备用。
1.3.2 胺化羧甲基改性磁性壳聚糖的制备
前面与磁性壳聚糖的制备相同,只是在超声分散后,分别加入一定量的柠檬酸和二乙烯三胺,并依次加入50mL液体石蜡和一定量的Span-80,常温搅拌1 h,滴加3mL戊二醛,快速搅拌下50℃水浴反应一段时间。用氢氧化钠溶液调节pH在9~10,升温至70℃,水浴反应4 h,抽滤,得到产物用无水乙醇、蒸馏水洗涤至中性,60℃真空干燥至恒重,研磨成粉末,真空保存备用。
1.3.3 样品性能表征及磁性能测定
利用扫描电镜观测改性磁性壳聚糖微粒的形貌,比表面积测定法分析改性磁性壳聚糖微粒的孔径,X-射线衍射检测磁性颗粒中四氧化三铁的晶型,红外光谱定性分析表征产品,并在有无磁场的条件下,考察改性磁性壳聚糖的沉降性能。
1.3.4 静态吸附实验
(1)pH对吸附的影响。称取9份质量均为0.05g的改性磁性壳聚糖分别加入到100 m LCu2+、Cd2+、Ni2+各50mg/L的三元离子溶液中,用盐酸溶液和氢氧化钠溶液调节溶液pH,pH以0.5为梯度分别从2.0提高到6.0,振荡吸附8 h,用原子吸收分光光度计测定溶液离子浓度,计算吸附剂对Cu2+、Cd2+、Ni2+的吸附容量。
(2)投加量对吸附的影响。分别称取改性磁性壳聚糖0.01、0.02、0.03、0.05、0.07、0.10、0.15 g,投加到7份配制好的100mL含Cu2+、Cd2+、Ni2+各50mg/L的三元离子溶液中,调节溶液pH=6。20℃条件下振荡反应8 h,测定吸附后溶液的离子浓度,计算相应的去除率。
(3)金属离子初始浓度对吸附的影响。取5份0.05 g改性磁性壳聚糖加入到100mL含Cu2+、Cd2+、Ni2+各初始质量浓度分别为10、50、100、200、300mg/L的三元离子溶液中,调节溶液pH=6。20℃室温条件下,振荡吸附4 h,测定吸附后离子浓度,计算相应的吸附容量及去除率。
2 结果与讨论
2.1 吸附剂的表征
2.1.1 SEM表征及BET分析
对改性磁性壳聚糖进行SEM表征,可以看出,改性磁性壳聚糖颗粒粒径分布均匀,粒径大小在250~350μm左右,平均粒径290μm。而单个改性磁性壳聚糖表面形貌显示,其表面呈团聚的颗粒状,同时根据BET孔径检测仪测定结果,可知改性磁性壳聚糖表面有大量介孔存在,单点吸附平均孔径在4.37 nm。吸附能力较磁性壳聚糖明显提高,物理吸附能力增强;改性磁性壳聚糖与离子的接触机会增多,为离子的配位螯合提供更多机会,因此化学吸附能力得到提高。
2.1.2 FT-IR表征分析
对比改性磁性壳聚糖(MACTS)和未改性磁性壳聚糖(MCTS)的红外光谱,结果见图1。
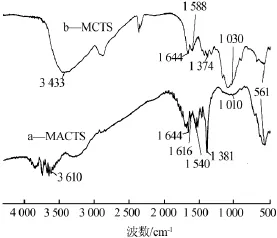
图1 改性磁性壳聚糖与磁性壳聚糖的FT-IT谱图
561 cm-1处为Fe3O4的特征吸收峰,由图1可以明显看到,改性后的磁性壳聚糖在此处的吸收峰不仅没有减弱,反而变强。此外由于交联改性增加了羟基和氨基,导致改性磁性壳聚糖在3 433 cm-1处由O—H和N—H的伸缩振动及分子间氢键引起的吸收峰已偏移至3 610 cm-1处,并且1 010 cm-1处的C6
羟基发生偏移,峰宽明显变小;同时在1 616、1 540 cm-1处也出现了羧基的反对称振动,证明柠檬酸已成功修饰到磁性壳聚糖结构上;δ(CH2)+ δ(CH3)的对称变角吸收峰已从1 374 cm-1偏移到1 381 cm-1,同时峰变得很强,证明有较多的烷基链修饰到磁性壳聚糖上,而在1 644 cm-1处酰胺羰基的伸缩振动,由于引入了羧基,羧基会与磁性壳聚糖链上的伯胺发生反应,使得酰胺羰基增多,峰变强,但是在1 644 cm-1处的峰却增强,这两点证明了二乙烯三胺中的氨基参与了反应,已成功与磁性壳聚糖交联。
2.1.3 XRD表征分析
Fe3O4的XRD图显示,Fe3O4的特征吸收峰2θ分别为30.095°、35.422°、43.052°、53.391°、56.942°、62.515°,所对应的晶型分别为〔220〕、〔311〕、〔400〕、〔422〕、〔511〕、〔440〕,而在改性磁性壳聚糖的XRD图谱中也出现了同样的峰,虽然峰强有所下降,是有机层的包覆导致,但这足以证明磁性物质为Fe3O4,所以改性磁性壳聚糖并未改变Fe3O4晶型。
2.1.4 磁性能测定
在磁场强度为0.2 T的条件下,对改性磁性壳聚糖的沉降性能进行实验对比分析。结果表明,无外加磁场下,吸附剂自然沉降完毕需要180 s,而在有外加磁场条件下,利用改性磁性壳聚糖的磁性,吸附剂在25 s内即可完全沉降,使分离回收操作时间大幅缩短。与磁性壳聚糖相比,改性后并没有使吸附剂的磁性沉降性能下降,说明改性仅发生在微球表面,没有改变磁性材料内部的结构。
2.2 吸附条件的选择
2.2.1 pH对改性磁性壳聚糖吸附容量的影响
pH对改性磁性壳聚糖吸附Cu2+、Cd2+、Ni2+三元离子的影响见图2。

图2 pH对改性磁性壳聚糖吸附容量的影响
由图2可知,pH小于3时,Cu2+、Cd2+、Ni2+的吸附容量极低,随着pH增大,吸附容量很快提高;对3种离子的吸附量均随着pH的升高而增大,不存在明显的选择性差异,并都在pH=6处达到最大,考虑到pH>7时,金属离子会与氢氧根生成沉淀,所以吸附的最适pH=6。
2.2.2 改性磁性壳聚糖投加量对去除率的影响
改性磁性壳聚糖投加量对Cu2+、Cd2+、Ni2+三元金属离子溶液去除率的影响见图3。
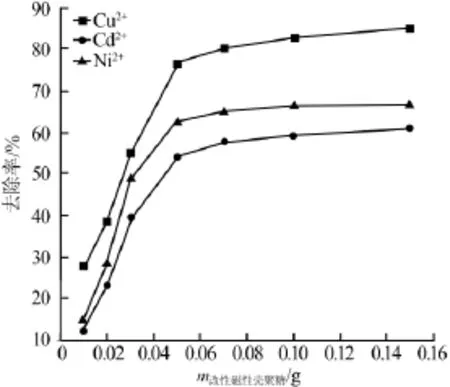
图3 改性磁性壳聚糖投加量对金属离子去除率的影响
由图3可知,改性磁性壳聚糖对Cu2+、Cd2+、Ni2+的去除率随着投加量的增大而增大,尤其在投加质量小于0.05 g之前,去除率增长尤为迅速。这是因为改性磁性壳聚糖的投加量增大使反应体系中有效活性基团增多,更多的活性位点与重金属离子相结合,最终使吸附剂对重金属离子的吸附率增大。当改性磁性壳聚糖投加质量达到0.05 g之后,对重金属离子的去除率趋于稳定,增长变化不大。因此,在本实验条件下,对Cu2+、Cd2+、Ni2+混合溶液的吸附,改性磁性壳聚糖的最佳投加质量为0.05 g。
2.2.3 溶液初始浓度对吸附性能的影响
磁性壳聚糖初始浓度对3种离子吸附性能的影响见图4。
Cu2+、Cd2+、Ni2+溶液初始质量浓度由10mg/L升高为300mg/L的过程中,改性磁性壳聚糖的吸附容量呈现先升高然后趋于稳定的趋势,而去除率则呈现下降的趋势。虽然重金属离子Cu2+、Cd2+、Ni2+初始浓度增大,使得其与活性基团的接触的几率增大,有利于吸附反应的进行,然而由于改性磁性壳聚糖的投加量一定,使其含有的活性吸附位点数一定,当溶液中的金属离子与活性位点充分结合后,金属离子初始浓度越高,溶液中残留的量就会相应增多,最终
导致其吸附率下降。
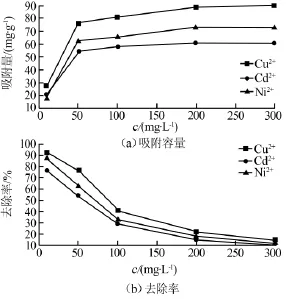
图4 溶液初始浓度对改性磁性壳聚糖吸附性能的影响
2.2.4 壳聚糖及其衍生物的吸附性能对比
为了进行壳聚糖及其衍生物吸附剂吸附性能的对比,分别称取壳聚糖、磁性壳聚糖、胺化羧甲基改性磁性壳聚糖0.05 g,投加到Cu2+、Cd2+、Ni2+各含50 mg/L的金属离子溶液中,进行吸附性能测定实验,结果见表1。
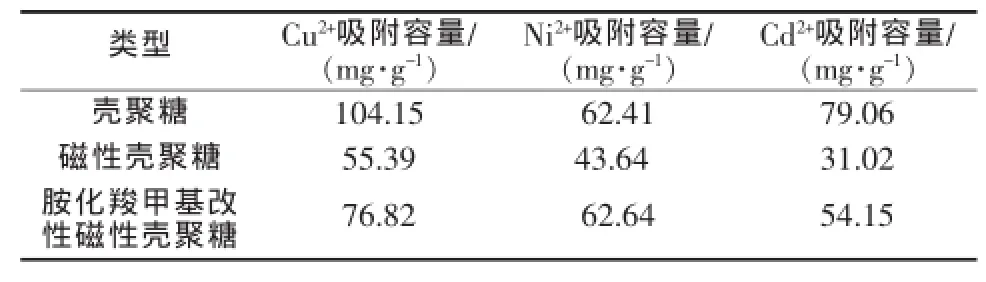
表1 3种壳聚糖吸附性能对比
由表2可知,壳聚糖对金属离子同样具有很好的吸附性能,但其易溶于酸性溶液,造成吸附剂流失,难以从溶液中分离进行回收利用。笔者制备的磁性壳聚糖微粒将磁核经过交联赋予壳聚糖磁性,回收方便,但由于交联剂占据吸附位点等原因导致吸附性能下降。而胺化羧甲基改性磁性壳聚糖在赋予壳聚糖磁性,提高了机械强度与回收效率的基础上,提高了磁性壳聚糖的吸附性能。
3 结论
(1)用柠檬酸及二乙烯三胺成功与磁性壳聚糖交联,得到了颗粒分布均匀、磁性能良好、平均孔径为4.37 nm的胺化羧甲基改性磁性壳聚糖。在最适pH=6的条件下,针对质量浓度分别为50 mg/L的 Cu2+、Cd2+、Ni2+三元离子共同吸附,改性磁性壳聚糖最佳投加质量为0.05 g。
(2)胺化羧甲基改性磁性壳聚糖在赋予壳聚糖磁性、提高了机械强度与回收率的基础上,还提高了磁性壳聚糖的吸附性能,对Cu2+、Cd2+、Ni2+3种离子同时存在的溶液,改性磁性壳聚糖的吸附容量均达到50mg/g以上。
[1]张海真,孙小梅,李步海.磁性壳聚糖微球的制备及其对脱落酸的吸附[J].武汉大学学报:理学版,2007,53(6):669-673.
[2]LiBaoqiang,Jia Dechang,Zhou Yu,etal.In situ hybridization tochitosan/magnetite nano-composite induced by themagnetic field[J]. Journal of Magnetism and Magneic Materials,2006,306(2):223-227.
[3]秦秋香,郭祀远.壳聚糖的成膜性及其工业应用进展[J].现代食品科技,2007,23(4):93-96.
[4]HirokiA,Tran HT,Nagasawa N.Metal adsorption of carboxy-methyl cellulose/carboxymethylchitosan blendhydrogelspreparedbyGamma irradiation[J].Radiation Physics and Chemistry,2009,78(12):1076-1080.
[5]NitayaphatW,Jiratumnukul N,Charuchinda S.Mechanical properties of chitosan/bamboo charcoal composite filmsmadewith normal and surface oxidized charcoal[J].Carbohydrate Polymers,2009,78(3):444-448.
[6]Hameed BH,El-KhaiaryM I.quilibrium,kinetics andmechanism of malachite green adsorption on activated carbon prepared from bamboo by K2CO3activation and subsequent gasification with CO2[J]. JournalofHazardousMaterials,2008,157(2/3):344-351.
[7]Wan Mengwei,Kan CC,Rogel B D,etal.Adsorption of copper(Ⅱ)and lead(Ⅱ)ions from aqueoussolution on chitosan-coated sand[J]. Carbohydrate Polymers,2010,80(3):891-899.
[8]Ng JCY,CheungW H,McKay G.Equilibrium Studiesof the Sorption of Cu(Ⅱ)Ions onto Chitosan[J].Journal of Colloid and Interface Science,2002,255(1):64-74.
[9]Chen A H,Liu Shengchang,Chen CY.Comparative adsorption of Cu(Ⅱ),Zn(Ⅱ),and Pb(Ⅱ)ions in aqueous solution on the crosslinked chitosan with epichlorohydrin[J].Journal of HazardousMaterials,2008,154(1/2/3):184-191.
[10]Vieira E FS,CestariA R,de BSantos E.Interaction ofAg(Ⅰ),Hg(Ⅱ),and Cu(Ⅱ)with 1,2-ethanedithiolimmobilized on chitosan:Thermochemical data from isothermal calorimetry[J].Journal of Colloid and Interface Science,2005,289(1):42-47.
Study on the preparation ofam ination carboxymethylmodified magnetic chitosan and its adsorption capability
Cui Li,Chen Yixin,Liang Jiyan,Wang Xin,Wang Hui,Sun Xiaohang
(Chemicaland EnvironmentalDepartment,Shenyang University of Technology,Shenyang 110870,China)
Magnetic chitosan has been prepared by cross-linking process,and on basis of this,it ismodified chemicallywith citric acid and diethylenetriamine.Asa result,amination carboxymethylmodifiedmagnetic chitosanwhich has good magnetic capacity and evenly distributed particles with average pore size of 4.37 nm has further been prepared.It is used for static adsorption experiments in simulated wastewater.The results show that themodified magnetic chitosan has improved the adsorption capacity of magnetic chitosan on basis of ensuring mechanical strength and recovery rates.When the optimum pH condition is6,itsadsorption capacities for Cu2+,Cd2+and Ni2+are 76.82,54.15,and 62.64mg/g,respectively.
magnetic chitosan;chemicalmodification;adsorption
TQ424
A
1005-829X(2016)11-0066-04
崔丽(1978—),博士,副教授。电话:13889845776,E-mail:sutcuili@163.com。
2016-09-05(修改稿)

